
25℃、101 kPa下,2g氢气燃烧生成液态水,放出285.8kJ热量,表示该反应的热化学方程式正确的是( )
A.2H2(g)+O2(g) == 2H2O(1) △H= ―285.8kJ/mol
B.H2(g)+ O2(g) == H2O(1) △H= ―285.8kJ/mol
O2(g) == H2O(1) △H= ―285.8kJ/mol
C.2H2 (g)+O2(g) == 2H2O(g) △H= ―571.6 kJ/mol
D.2H2(g)+ O2(g) == 2H2O(1) △H= +571.6 kJ/mol
 阶梯计算系列答案
阶梯计算系列答案科目:高中化学 来源: 题型:
NA表示阿伏加德罗常数的值,下列说法正确的是
A.25℃时,pH=2的1.0L H2SO4溶液中含有的H+数目为0.02NA
B.电解精炼铜时,当电路中转移NA个电子,阳极溶解32g铜
C.2.24LNH3中含共价键数目一定为0.3NA
D.向含有FeI2的溶液中通入适量氯气,当有1mol Fe2+被氧化时该反应转移电子的数目至少为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
工业废水中常含有一定量的Cr2O ,会对人类及生态系统产生很大损害,电解法是一种行之有效的除去铬的方法之一。该法用Fe和石墨作电极电解含Cr2O
,会对人类及生态系统产生很大损害,电解法是一种行之有效的除去铬的方法之一。该法用Fe和石墨作电极电解含Cr2O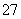 的酸性废水,最终将铬转化为Cr(OH)3沉淀,达到净化目的。某科研小组利用以上方法处理污水,设计了熔融盐电池和污水电解装置如下图所示。
的酸性废水,最终将铬转化为Cr(OH)3沉淀,达到净化目的。某科研小组利用以上方法处理污水,设计了熔融盐电池和污水电解装置如下图所示。
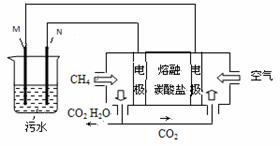
(1)Fe电极为 (填“M”或“N”);电解时 (填“能”或“不能”)否用Cu电极来代替Fe电极,理由是 。
(2)阳极附近溶液中,发生反应的离子方程式是 ;阴极附近的沉淀有 。
(3) 图中熔融盐燃料电池是以熔融碳酸盐为电解质、CH4为燃料、空气为氧化剂、稀土金属材料为电极的新型电池。已知,该熔融盐电池的负极的电极反应是CH4–8e–+4CO32–==5CO2+2H2O,则正极的电极反应式为 。
(4)实验过程中,若电解池阴极材料质量不变,产生4.48L(标准状况)气体时,熔融盐燃料电池消耗CH4的体积为 L(标准状况)。
(5) 已知某含Cr2O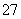 的酸性工业废水中铬元素的含量为104.5 mg·L-1,处理后铬元素最高允许排放浓度为0.5 mg·L-1。处理该废水1 000 m3并达到排放标准至少消耗铁的质量为 kg。
的酸性工业废水中铬元素的含量为104.5 mg·L-1,处理后铬元素最高允许排放浓度为0.5 mg·L-1。处理该废水1 000 m3并达到排放标准至少消耗铁的质量为 kg。
查看答案和解析>>
科目:高中化学 来源: 题型:
对于在一定条件下进行的化学反应:2SO2+O2⇌2SO3,改变下列条件,可以提高反应物中的活化分子百分数的是( )
|
| A. | 升高温度 | B. | 增大压强 |
|
| C. | 压缩使容器体积变小 | D. | 增大反应物浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在NH3•H2O ⇌ NH4++OH﹣形成的平衡中,要使NH3•H2O的电离程度及c(OH﹣)都增大,可采取的措施是( )
|
| A. | 通入HCl | B. | 加少量NaOH固体 |
|
| C. | 加少量氯化铵固体 | D. | 加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应A+B(s)⇌ C达到平衡后,无论加压或降温,B的转化率都增大,则下列结论正确的是( )
|
| A. | 正反应为放热反应 | B. | 正反应为吸热反应 |
|
| C. | A为气体,C为固体 | D. | A为固体,C为气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
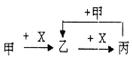
已知甲、乙、丙、X是4种中学化学中常见的物质,其转化关系如右图。
则甲和X不可能是
A.甲-Na、X-O2 B.甲-NaOH溶液、X-CO2溶液
C.甲-C、X-O2 D.甲-AlCl3溶液、X-NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.硫粉在过量的纯氧中燃烧可以生成大量的SO2
B.可以用品红溶液鉴别SO2和CO2
C.SO2能使品红溶液、酸性KMnO4溶液褪色,但褪色原理不同
D.少量SO2通过CaCl2的溶液能生成白色沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com