
【题目】某温度下,CO(g) + H2O (g)![]() CO2(g)+ H2(g)的平衡常数K=1。该温度下在体积均为1 L的甲、乙两个恒容密闭容器中,投入CO(g) 和 H2O (g)的起始浓度及5min时的浓度如下表所示。
CO2(g)+ H2(g)的平衡常数K=1。该温度下在体积均为1 L的甲、乙两个恒容密闭容器中,投入CO(g) 和 H2O (g)的起始浓度及5min时的浓度如下表所示。
甲 | 乙 | |||
起始浓度 | 5min时浓度 | 起始浓度 | 5min时浓度 | |
c(CO)/mol/L | 0.1 | 0.08 | 0.2 | x |
c(H2O)/mol/L | 0.1 | 0.08 | 0.2 | y |
下列判断不正确的是
A.x = y = 0.16
B.反应开始时,乙中反应速率比甲快
C.甲中0~5min的平均反应速率: v(CO)=0.004"mol/(L·min)
D.平衡时,乙中H2O的转化率是50%,c(CO)是甲中的2倍
【答案】A
【解析】
A、乙容器中反应物的起始浓度是甲容器中起始浓度的2倍,反应速率快但不一定是甲容器中速率2倍,故x = y 不一定为 0.16,错误;B、乙容器中反应物的浓度是甲容器反应物浓度的2倍,反应开始时,乙中反应速率比甲快,正确;C、根据表中数据计算,甲中0~5min的平均反应速率: v(CO)=△c(CO)/△t=0.004 mol/(L·min),正确;D、设平衡时乙中H2O的转化浓度为x,则K=[CO2][ H2]/[ CO][ H2O]=x2/(0.2—x)2=1解得x=0.01,故乙中水的转化率是50%,根据等效平衡知识判断达平衡时c(CO)是甲中的2倍,正确。
故选A。


 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案科目:高中化学 来源: 题型:
【题目】Ⅰ物质的类别和核心元素的化合价是研究物质性质的两个重要角度。
下图所示是硫及其部分化合物的“价类二维图”, 根据图示回答下列问题:
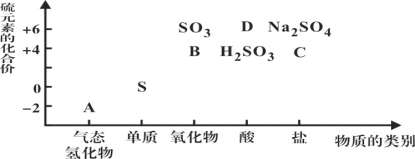
(1)图中A、B、C、D四种物质中,属于非电解质的是__________(用化学式表示)。
(2)足量B通入紫色石蕊溶液的现象是__________________________;用一个化学方程式说明B具有还原性_____________________________。
(3)C在反应中既可作氧化剂,又可作还原剂。当它作氧化剂时,理论上其可被还原为__________(填标号)。
A.Na2S B.S C.H2SO3 D.Na2SO4 E.H2SO4
(4)将A与SO2混合,可生成淡黄色固体。该反应的氧化剂与还原剂的物质的量之比为_____。
(5)D的浓溶液与铜单质在加热条件下可以发生化学反应,反应的化学方程式为__________________________________,反应中D显示酸性和______________。
Ⅱ.如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。

(1)硫酸具有A-D所示的性质,以下过程主要表现了浓硫酸的那些性质?
请将选项字母填在下列各小题的横线上:
A强酸性 B 吸水性 C 脱水性 D 强氧化性
①浓硫酸使木条变黑__________
②热的浓硫酸与铜片反应__________
(2)现用该浓硫酸配制100mL 1mol/L的稀硫酸。
可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④ 药匙;⑤量筒;⑥托盘天平。请回答下列问题:
配制稀硫酸时,上述仪器中不需要使用的有__________(选填序号),还缺少的仪器有__________(写仪器名称);
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A. 酸化NaIO3和NaI的混合溶液:I +IO3+6H+![]() I2+3H2O
I2+3H2O
B. 饱和Na2CO3溶液与CaSO4固体反应:CO32+CaSO4![]() CaCO3+SO42
CaCO3+SO42
C. KClO碱性溶液与Fe(OH)3反应:3ClO+2Fe(OH)3![]() 2FeO42+3Cl+4H++H2O
2FeO42+3Cl+4H++H2O
D. 电解饱和食盐水:2Cl+2H+![]() Cl2↑+ H2↑
Cl2↑+ H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在通风橱中进行下列实验:
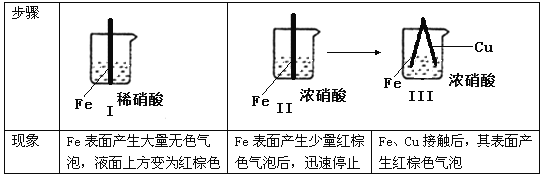
下列说法中不正确的是:
A. Ⅰ种气体有无色变红棕色的化学方程式为:2NO+O2=2NO2
B. Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应
C. 对比Ⅰ、Ⅱ中现象,说明稀HNO3的氧化性强于浓HNO3
D. 针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电浮选凝聚法处理酸性污水的工作原理如图所示,下列说法不正确是( )
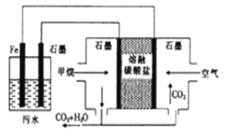
A. 铁电极的电极反应式为Fe-2e-=Fe2+
B. 通入甲烷的石墨的电极反应式为:CH4+4CO32-—8e- ==5CO2+2H2O
C. 为了增强的污水的导电能力,可向污水中加入适量食盐
D. 若左池石墨电极产生44.8L气体,则消耗0.5mol甲烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中科院一项最新成果实现了甲烷高效生产乙烯,甲烷在催化作用下脱氢,在气相中经自由基偶联反应生成乙烯,其反应如下:![]()
化学键 |
|
|
|
|
| a | b | c | d |
(1)已知相关化学键的键能如上表,甲烷制备乙烯反应的![]() ______
______![]() 用含a、b、c、d的代数式表示
用含a、b、c、d的代数式表示![]() 。
。

![]() 温度时,向1L的恒容反应器中充入2
温度时,向1L的恒容反应器中充入2![]() ,仅发生上述反应,反应过程中
,仅发生上述反应,反应过程中![]() min
min![]() 的物质的量随时间变化如图1,测得
的物质的量随时间变化如图1,测得![]() min时
min时![]() 的浓度为
的浓度为![]()
![]() min内
min内![]() 表示的反应速率为______
表示的反应速率为______![]()
![]()
![]() 若图1中曲线a、曲线b分别表示在温度
若图1中曲线a、曲线b分别表示在温度![]() 时,使用质量相同但表面积不同的催化剂时,达到平衡过程中n
时,使用质量相同但表面积不同的催化剂时,达到平衡过程中n![]() 的变化曲线,其中表示催化剂表面积较大的曲线是______(填“a“或“b”)。
的变化曲线,其中表示催化剂表面积较大的曲线是______(填“a“或“b”)。
![]() min时,若改变外界反应条件,导致
min时,若改变外界反应条件,导致![]() 发生图中所示变化,则改变的条件可能是_______
发生图中所示变化,则改变的条件可能是_______![]() 任答一条即可
任答一条即可![]() 。
。
![]() 实验测得:
实验测得:![]() ,
,![]() ,其中
,其中![]() 、
、![]() 为速率常数仅与温度有关,
为速率常数仅与温度有关,![]() 温度时
温度时![]() 与
与![]() 的比值为______(填数值)。若将温度由
的比值为______(填数值)。若将温度由![]() 升高到
升高到![]() ,则反应速率增大的倍数
,则反应速率增大的倍数![]() ______V逆 (选填“
______V逆 (选填“![]() ”、“
”、“![]() ”或“<”)。
”或“<”)。
![]() 科研人员设计了甲烷燃料电池并用于电解。如图2所示,电解质是掺杂了
科研人员设计了甲烷燃料电池并用于电解。如图2所示,电解质是掺杂了![]() 与
与![]() 的固体,可在高温下传导
的固体,可在高温下传导![]()
![]() 极为______极(选填“阳”或“阴”)。
极为______极(选填“阳”或“阴”)。
![]() 该电池工作时负极反应方程式为________。
该电池工作时负极反应方程式为________。
![]() 用该电池电解饱和食盐水,一段时间后收集到标况下气体总体积为11.2L,则透过阳离子交换膜的离子的物质的量为_________ mol
用该电池电解饱和食盐水,一段时间后收集到标况下气体总体积为11.2L,则透过阳离子交换膜的离子的物质的量为_________ mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 键角:BF3>CH4>H2O>NH3
B. CO2、HClO、HCHO分子中一定既有σ键又有π 键
C. 已知反应N2O4(l)+2N2H4(l) = 3N2(g)+4H2O(l),若该反应中有4 mol N—H键断裂,则形成的π键数目为1.5NA
D. 在硅酸盐中,SiO44-四面体通过共用顶角氧离子形成一种无限长单链结构的多硅酸根如图,其中Si原子的杂化方式与图中S8单质中S原子的杂化方式相同


查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中浓度关系正确的是( )
A. 小苏打溶液中:c(Na+)+c(H+)=c(HCO)+c(CO![]() )+c(OH-)
)+c(OH-)
B. CH3COONa溶液中:c(CH3COO-)>c(Na+)
C. 物质的量浓度相等的CH3COOH溶液和CH3COONa溶液等体积混合:c(CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH)
D. 0.1 mol/L的NaHA溶液,其pH=4,则c(HA-)>c(H+)>c(H2A)>c(A2-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com