
【题目】中科院一项最新成果实现了甲烷高效生产乙烯,甲烷在催化作用下脱氢,在气相中经自由基偶联反应生成乙烯,其反应如下:![]()
化学键 |
|
|
|
|
| a | b | c | d |
(1)已知相关化学键的键能如上表,甲烷制备乙烯反应的![]() ______
______![]() 用含a、b、c、d的代数式表示
用含a、b、c、d的代数式表示![]() 。
。

![]() 温度时,向1L的恒容反应器中充入2
温度时,向1L的恒容反应器中充入2![]() ,仅发生上述反应,反应过程中
,仅发生上述反应,反应过程中![]() min
min![]() 的物质的量随时间变化如图1,测得
的物质的量随时间变化如图1,测得![]() min时
min时![]() 的浓度为
的浓度为![]()
![]() min内
min内![]() 表示的反应速率为______
表示的反应速率为______![]()
![]()
![]() 若图1中曲线a、曲线b分别表示在温度
若图1中曲线a、曲线b分别表示在温度![]() 时,使用质量相同但表面积不同的催化剂时,达到平衡过程中n
时,使用质量相同但表面积不同的催化剂时,达到平衡过程中n![]() 的变化曲线,其中表示催化剂表面积较大的曲线是______(填“a“或“b”)。
的变化曲线,其中表示催化剂表面积较大的曲线是______(填“a“或“b”)。
![]() min时,若改变外界反应条件,导致
min时,若改变外界反应条件,导致![]() 发生图中所示变化,则改变的条件可能是_______
发生图中所示变化,则改变的条件可能是_______![]() 任答一条即可
任答一条即可![]() 。
。
![]() 实验测得:
实验测得:![]() ,
,![]() ,其中
,其中![]() 、
、![]() 为速率常数仅与温度有关,
为速率常数仅与温度有关,![]() 温度时
温度时![]() 与
与![]() 的比值为______(填数值)。若将温度由
的比值为______(填数值)。若将温度由![]() 升高到
升高到![]() ,则反应速率增大的倍数
,则反应速率增大的倍数![]() ______V逆 (选填“
______V逆 (选填“![]() ”、“
”、“![]() ”或“<”)。
”或“<”)。
![]() 科研人员设计了甲烷燃料电池并用于电解。如图2所示,电解质是掺杂了
科研人员设计了甲烷燃料电池并用于电解。如图2所示,电解质是掺杂了![]() 与
与![]() 的固体,可在高温下传导
的固体,可在高温下传导![]()
![]() 极为______极(选填“阳”或“阴”)。
极为______极(选填“阳”或“阴”)。
![]() 该电池工作时负极反应方程式为________。
该电池工作时负极反应方程式为________。
![]() 用该电池电解饱和食盐水,一段时间后收集到标况下气体总体积为11.2L,则透过阳离子交换膜的离子的物质的量为_________ mol
用该电池电解饱和食盐水,一段时间后收集到标况下气体总体积为11.2L,则透过阳离子交换膜的离子的物质的量为_________ mol
【答案】![]()
![]() b 升高温度或减小压强
b 升高温度或减小压强 ![]()
![]() 阳
阳 ![]() 0.5
0.5
【解析】
ΔH=反应物总键能-生成物总键能;
⑴ΔH=反应物总键能-生成物总键能=[2×4b-(c+4b)-2a]kJ·mol-1=+(4b-c-2a)kJ·mol-1,故答案:+(4b-c-2a)kJ·mol-1;
⑵①2 mol 甲烷放入1 L容器中,其浓度为2 mol·L-1,其甲烷的速率为
![]()
故答案为0.16mol·L-1·min-1
②催化剂表面积越大,催化效果越好,速率越快,达到平衡所需的时间越短,所以曲线b的催化剂表面积较大,故答案为b;
③15 min时,改变外界反应条件,导致n(CH4)减小,说明平衡向消耗CH4的方向移动,所以改变的条件可能是升高温度或减小压强,故答案为升高温度或减小压强;
⑶ 2CH4(g) ![]() C2H4(g) +2H2(g)
C2H4(g) +2H2(g)
c始(mol/L) 2 0 0
Δc(mol/L) 1.6 0.8 1.6
c末(mol/L) 0.4 0.8 1.6
T1温度时,该反应的平衡常数![]() ,且达到平衡时有v正=v逆,即k正c2(CH4)=k逆c(C2H4)·c2(H2),则
,且达到平衡时有v正=v逆,即k正c2(CH4)=k逆c(C2H4)·c2(H2),则
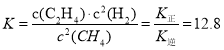
故答案为12.8;
该反应为吸热反应,升高温度,平衡正向移动,v正>v逆。
故答案为>;
⑷①甲烷燃料电池,通燃料一极为负极,通氧气一极为正极,连原电池正极的C极为电解池的阳极,连原电池负极的D极为电解池的阴极;
故答案:阳;
②根据图示,电解质为传导的O2-,燃料电池的负极是甲烷与O2-反应生成H2O和CO2的反应,所以电极反应为CH4-8e-+4O2-==CO2+2H2O,
故答案为CH4-8e-+4O2-= CO2+2H2O;
③根据离子方程式2Cl-+2H2O = 2OH-+Cl2↑+H2↑;可知,电解一段时间后,共收集到标准状况下气体11.2 L,即气体的物质的量为0.5mol,由于产生0.5 mol气体生成了0.5 mol氢氧根,根据电荷守恒原理,透过阳离子交换膜的钠离子物质的量为0.5 mol;
故答案为0.5 。


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
【题目】常温时,下列溶液中微粒的物质的量浓度关系正确的是( )
A. 0.1mol/L![]() 与0.1mol/L HCl等体积混合:
与0.1mol/L HCl等体积混合:![]()
B. 0.1mol/L的![]() 溶液,其pH=4,则
溶液,其pH=4,则![]()
C. ![]() 溶液:
溶液:![]()
D. 将0.1mol/L的![]() 溶液和0.1mol/L
溶液和0.1mol/L![]() 溶液等体积混合后,则:
溶液等体积混合后,则:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上的描述合理的是( )
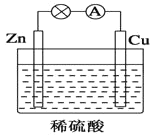
实验后的记录:
①Cu为负极,Zn为正极
②Cu极上有气泡产生,发生还原反应
③SO42-向Cu极移动
④若有0.5mol电子流经导线,则可产生0.25mol气体
⑤电子的流向是:Cu-→Zn
⑥正极反应式:Cu+2e-═Cu2+,发生氧化反应
A.①②③B.②④
C.②④⑥D.③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如右,电解总反应为:2Cu+H2O![]() Cu2O+H2↑。下列说法正确的是
Cu2O+H2↑。下列说法正确的是
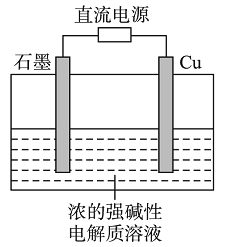
A. 石墨电极上产生氢气
B. 铜电极发生还原反应
C. 铜电极接直流电源的负极
D. 当有0.1 mol电子转移时,有0.1 mol Cu2O生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,CO(g) + H2O (g)![]() CO2(g)+ H2(g)的平衡常数K=1。该温度下在体积均为1 L的甲、乙两个恒容密闭容器中,投入CO(g) 和 H2O (g)的起始浓度及5min时的浓度如下表所示。
CO2(g)+ H2(g)的平衡常数K=1。该温度下在体积均为1 L的甲、乙两个恒容密闭容器中,投入CO(g) 和 H2O (g)的起始浓度及5min时的浓度如下表所示。
甲 | 乙 | |||
起始浓度 | 5min时浓度 | 起始浓度 | 5min时浓度 | |
c(CO)/mol/L | 0.1 | 0.08 | 0.2 | x |
c(H2O)/mol/L | 0.1 | 0.08 | 0.2 | y |
下列判断不正确的是
A.x = y = 0.16
B.反应开始时,乙中反应速率比甲快
C.甲中0~5min的平均反应速率: v(CO)=0.004"mol/(L·min)
D.平衡时,乙中H2O的转化率是50%,c(CO)是甲中的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D、E五种阴阳离子均不相同的化合物,五种阳离子为![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() ,五种阴离子为
,五种阴离子为![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 现将它们分别配成
现将它们分别配成![]() 的溶液,进行如下实验
的溶液,进行如下实验
![]() 测得溶液A、B呈碱性,且碱性为
测得溶液A、B呈碱性,且碱性为![]() ;
;
![]() 向C溶液中滴加稀盐酸,有气体生成;
向C溶液中滴加稀盐酸,有气体生成;
![]() 向D溶液中滴加NaOH溶液,先岀现沉淀,继续滴加,沉淀消失
向D溶液中滴加NaOH溶液,先岀现沉淀,继续滴加,沉淀消失
请根据上述实验现象,回答下列问题
![]() 实验
实验![]() 中发生反应的化学方程式为______________;向C中滴加NaOH溶液,出现的现象为_________。
中发生反应的化学方程式为______________;向C中滴加NaOH溶液,出现的现象为_________。
![]() 分两步写出实验
分两步写出实验![]() 中发生反应的离子方程式______________。
中发生反应的离子方程式______________。
![]() 写出下列四种化合物的化学式:A______________;B______________。
写出下列四种化合物的化学式:A______________;B______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,密闭可变容器中发生可逆反应N2+3H2![]() 2NH3能说明反应已达到平衡状态的是
2NH3能说明反应已达到平衡状态的是
A.以上三种物质的浓度相等B.压强恒定
C.2v正(H2)=3v逆(NH3)D.v正(N2)=3v逆(H2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法不正确的是
A. 1,3-二甲苯也称间二甲苯
B. 乙烷和新戊烷分子中所含甲基数之比为1∶2
C. 苯与溴水不能发生加成反应,所以两者混合后无明显现象
D. ![]() 和C4H10的二氯代物的数目不同(不含立体异构)
和C4H10的二氯代物的数目不同(不含立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,正确的是
A.所有的硅酸盐都难溶于水,可用带玻璃塞的玻璃瓶盛放
B.SiO2和CO2都是酸性氧化物,既能与水反应,又能与NaOH溶液反应
C.SiO2与纯碱在高温条件下反应生成CO2,说明硅酸的酸性比碳酸强
D.石灰石是工业制备普通玻璃和水泥的共同原料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com