
【题目】某同学查询资料后得到如下信息:柠檬烯(![]() )的沸点为177℃,熔点为-74.3℃,密度为0.84 g/mL,具有良好的镇咳、祛痰、抑菌作用,广泛存在于天然的植物精油中。
)的沸点为177℃,熔点为-74.3℃,密度为0.84 g/mL,具有良好的镇咳、祛痰、抑菌作用,广泛存在于天然的植物精油中。
(一)粗精油的提取。该同学利用如图所示装置(加热、夹持及冷凝管内管均省略)从植物组织中获取粗精油,实验步骤如下:
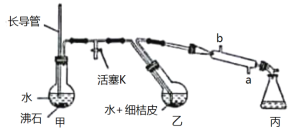
i.将几片桔子皮剪成细碎的碎片,投入乙装置中,加入约30 mL水;
ii.打开活塞K,加热甲至K处的支管口有大量水蒸气冒出时旋紧,再打开冷凝水,水蒸气蒸馏即开始进行。可观察到在馏出液的水面上有一层很薄的油层。
(1)甲中长导管的作用是___________。蒸馏结束时,应先将_____________,再停止加热。
(2)冷凝管的内管应是_________(填“蛇”“球”或“直”)形的。若冷却水从b口进入,则对提取到精油量的影响情况是____________。
(二)柠檬烯的提取。
i.将馏出液加入到仪器A中,然后加入适量的CH2Cl2(沸点为40℃)萃取3次,最后将萃取液置于干燥的锥形瓶中,并加入适量的试剂A干燥半个小时。
ii.将干燥好的溶液加入蒸馏烧瓶中,通过一系列操作,最后烧瓶中剩下的橙黄色液体就是柠檬烯。
(3)仪器A是_________,试剂A可以是_______(写出两种)。若将一定量的橙黄色液体滴入溴的CCl4溶液中,溶液褪色,由此现象可得出的恰当结论是____________。
(4)若桔皮总质量为a g,最后得到V mL柠檬烯,实验过程中柠檬烯的总损失率为b% ,则枯皮中柠檬烯的质量分数为_____________%。
【答案】平衡压强 乙中的导气管从溶液中移出 直 收集到的精油量减少 分液漏斗 无水Na2SO4、无水CaCl2 柠檬烯中含有碳碳不饱和键 ![]()
【解析】
(一)装置甲产生热的水蒸气通入装置乙中桔子皮与水的混合物中,在热蒸气作用下,使桔子皮中的植物精油挥发,经冷凝器冷凝后收集在装置丙中;
(二)将馏出液放入分液漏斗中,用适量的CH2Cl2进行萃取作用后置于干燥的锥形瓶中,并加入适量干燥剂进行充分,将干燥好的溶液加入蒸馏烧瓶中,通过一系列操作,最后烧瓶中剩下的橙黄色液体就是柠檬烯。先根据其利用率及产生柠檬烯的体积和密度计算其质量,结合桔子皮质量计算出枯皮中柠檬烯的质量分数。
(1)甲中长的玻璃导管一端与空气相通,其作用是安全管,能起到平衡压强的作用;蒸馏结束时为防止倒吸现象的发生,应先将乙中的导气管从溶液中移出液面;
(2)因蒸馏实验中冷凝管是倾斜的,为减少蒸馏液的积留,冷凝管内管应是直形。若冷却水从b口进入,会导致冷凝效果较差,会有少量精油不能液化而损失掉,这样会导致收集到的精油量减少;
(3)加入CH2Cl2的目的是进行萃取作用,故操作应在分液漏斗中进行,仪器A是分液漏斗。干燥的目的是除去残留的水分,故试剂A可以是无水CaCl2或无水Na2SO4等。将一定量的橙黄色液体滴入溴的CCl4溶液中,溶液褪色,由此可知发生了加成反应,故可证明柠檬烯中含有碳碳不饱和键;
(4)柠檬烯密度为0.84 g/mL收集到的柠檬烯体积为V mL,则其质量为0.84Vg,设桔子皮中柠檬烯的质量分数为x,则ax(1-b%)=0.84V,解得x=![]() ×100%=
×100%=![]() %。
%。


科目:高中化学 来源: 题型:
【题目】某强酸性溶液X,可能含有Al3+、Ba2+、NH4+、Fe2+、Na+、CO32﹣、SO42﹣、SiO32﹣、NO3﹣中的一种或几种离子,取该溶液进行实验,其现象及转化如下图所示。

请回答下列问题:
(1)由整体的实验过程可判断溶液X中一定不存在的阴离子有______。
(2)产生气体A的离子方程式为____________。
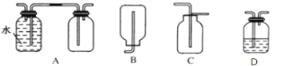
(3)在实验室中收集气体A,可选择如图装置中的______。
(4)写出④反应中生成溶液H的离子方程式____________。
(5)对不能确定是否存在的离子,请简述检测实验方案__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知酸性K2Cr2O7溶液可与FeSO4溶液反应生成Fe3+和Cr3+。现将硫酸酸化的K2Cr2O7溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系如图所示,下列说法中不正确的是
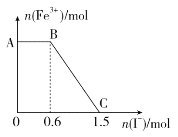
A. 图中AB段的氧化剂为K2Cr2O7
B. 开始加入的K2Cr2O7为0.25 mol
C. K2Cr2O7与FeSO4反应的物质的量之比为1∶3
D. 图中BC段发生的反应为2Fe3++2I-===2Fe2++I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值。下列说法错误的是
A.3.6 g C60与C50组成的混合物中。含有的电子数目为1.8NA
B.6.72 L(标准状况)Cl2与足量乙烷反应时,断裂的C-H键数目为0.3NA
C.0.1 L浓度均为2 mol/L的(NH4)2SO4、NH4Cl溶液中,NH4+数目前者比后者多0.2 NA
D.0.1 mol H3BO3[电离方程式:H3BO3+H2O![]() H++B(OH)4-]消耗OH-数目最多为0.1 NA
H++B(OH)4-]消耗OH-数目最多为0.1 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于蔗糖属于非还原型糖,而其水解产物具有还原性的实验方案的说法中,正确的是
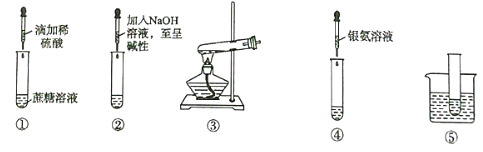
A. 验证蔗糖属于非还原型糖的操作顺序:④③
B. 验证蔗糖属于非还原型糖的操作顺序:③⑤
C. 验证蔗糖水解产物具有还原性的操作顺序:①④⑤
D. 验证蔗糖水解产物具有还原性的操作顺序:①⑤②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锑(Sb)是第VA族元素,其单质主要用于制造合金、半导体。三氧化二锑俗称锑白,是白色粉末,不溶于水,是一种两性氧化物,主要用于白色颜料、油漆和塑料、石油化工等。某工厂用羽毛矿(主要成分为Pb4FeSb6S14)制取锑白的工艺流程如图所示:

(1)Pb4FeSb6S14中的锑元素只显一种化合价,则其化合价是______。X是一种固体单质,其成分是___(填化学式)。
(2)氯化浸出中,除铅与X外,被氧化的元素反应后均显高价,写出相应的化学方程式:______________。操作1为加水稀释,写出生成SbOCl的离子方程式:___________。
(3)试剂1通常选用氨水而不是NaOH溶液,最可能的原因是_______。操作2的内容是_________、干燥。
(4)在强碱性条件下电解Na3SbS3溶液(原理如图)可得到单质锑。

写出阴极的电极反应式:_______,B电极应接电源的______极,当有2 mol Sb生成时,通过阳离子交换膜的离子数为_________(设NA为阿伏加德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在容积为2 L的密闭容器内, 某一反应中气体M和气体N的物质的量随反应时间变化的曲线如图所示, 请根据图示回答下列问题。
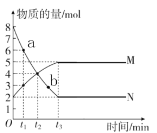
(1)写出该反应的化学方程式:____________。
(2)t1~t3时间段,以M的浓度变化表示的平均反应速率为________(用含t1、t3的式子表示)。
(3)比较a点与b点反应速率大小,Va___Vb(填“>”“=” 或 “< ”)。
(4)如图所示的三个时刻中,___________(填t1、t2或t3)时刻处于平衡状态。
(5)下列叙述中,能说明该反应达到平衡状态的是________。
A.容器内M与N的物质的量相等
B.容器内M与N的浓度不随时间变化
C.单位时间内每消耗1 mol N,同时生成0.5 mol M
D.容器内压强不随时间变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z原子半径的顺序为![]() ,基态X原子p能级上的电子数是Y原子质子数的3倍,它们可以形成离子化合物
,基态X原子p能级上的电子数是Y原子质子数的3倍,它们可以形成离子化合物![]() ,其中阳离子
,其中阳离子![]() (已知
(已知![]() 水合物的
水合物的![]() 为
为![]() 、
、![]() 为
为![]() )的结构如图所示。下列叙述错误的是( )
)的结构如图所示。下列叙述错误的是( )

A.![]() 的阴、阳离子均含有18个电子
的阴、阳离子均含有18个电子
B.常温下,![]() 的水溶液呈碱性
的水溶液呈碱性
C.三种元素中Y的电负性最小
D.简单气态氢化物的还原性:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】兴趣小组在实验室中模拟利用甲烷和氯气发生取代反应制取副产品盐酸,设计如图装置,下列说法错误的是( )
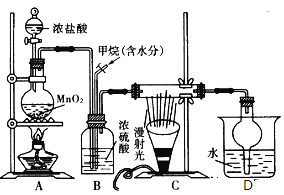
A. 实验时先点燃A处酒精灯再通甲烷
B. 装置B有均匀混合气体、控制气流速度、干燥混合气体等作用
C. 装置C经过一段时间的强光照射后,生成的有机物有4种
D. 从D中分离出盐酸的方法为过滤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com