
【题目】甲醇是一种重要的化工原料,广泛应用于化工生产,也可直接用作燃料.已知: CH3OH(l)+O2(g)═CO(g)+2H2O(g)△H1=﹣443.64kJmol﹣1;
2CO(g)+O2(g)═2CO2(g)△H2=﹣566kJmol﹣1 .
下列说法或热化学方程式正确的是( )
A.CO的燃烧热为566kJmol﹣1
B.2 mol CO和1 mol O2的总能量比2 mol CO2的总能量低
C.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=﹣1453.28 kJmol﹣1
D.完全燃烧16g甲醇,生成一氧化碳和水时放出的热量为221.82 kJ
【答案】C
【解析】解:A.1mol可燃物完全燃烧生成稳定氧化物放出的热量为燃烧热,2CO(g)+O2(g)=2CO2(g)△H2=﹣566.0kJmol﹣1 , 则CO的燃烧热为283.0 kJmol﹣1 , 故A错误;B.放热反应中反应物的总能量大于生成物的总能量,所以2 mol CO和1mol O2的总能量比2 mol CO2的总能量高,故B错误;
C.已知:①CH3OH(l)+O2(g)=CO(g)+2H2O(g)△H1=﹣443.64kJmol﹣1 ②2CO(g)+O2(g)=2CO2(g)△H2=﹣566.0kJmol﹣1根据盖斯定律①+②× ![]() 得CH3OH(l)+
得CH3OH(l)+ ![]() O2(g)=CO2(g)+2H2O(g)△H1=﹣726.64kJmol﹣1 , 方程式的计量数加倍,则反应热也加倍则2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=﹣1453.28 kJmol﹣1 , 故C正确;
O2(g)=CO2(g)+2H2O(g)△H1=﹣726.64kJmol﹣1 , 方程式的计量数加倍,则反应热也加倍则2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=﹣1453.28 kJmol﹣1 , 故C正确;
D.CH3OH(l)+ ![]() O2(g)=CO2(g)+2H2O(g)△H1=﹣726.64kJmol﹣1 , 完全燃烧16g甲醇,生成一氧化碳和水时放出的热量为726.64kJ,故D错误;
O2(g)=CO2(g)+2H2O(g)△H1=﹣726.64kJmol﹣1 , 完全燃烧16g甲醇,生成一氧化碳和水时放出的热量为726.64kJ,故D错误;
故选C.
【考点精析】通过灵活运用反应热和焓变,掌握在化学反应中放出或吸收的热量,通常叫反应热即可以解答此题.


科目:高中化学 来源: 题型:
【题目】根据下列转化关系(反应条件略去),A、B、C、D中均含有同一种元素,回答下头问题:
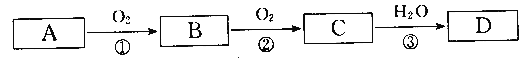
(1)若A为Na,写出反应③的化学方程式___________________________
(2)若A为N2,写出反应③的离子方程式___________________________
(3)若A为S,写出D的浓溶液与Cu在加热情况下反应的化学方程式_________________
(4)若A为NH3,写出过量Fe与D的稀溶液反应(还原产物只有B)的离子方程式_____________________________,将14 g铜、银合金与一定量某浓度的D溶液完全反应,将放出的气体与1.12 L(标准状况)氧气混合通入水中,恰好全部被水吸收,则合金中铜的质量是________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一个甲烷燃料电池工作时的示意图.M、N两电极的质量相同,其中一个为银电极一个为铁电极.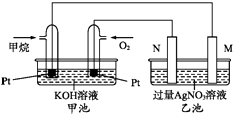
(1)写出通入甲烷的铂电极上的电极反应式为 .
(2)若一段时间后M与N两电极的总质量不变,则N电极是 . 此时两电极质量差为5.4g,甲池中理论上消耗氧气mL(标准状况)
(3)若一段时间后M与N两电极的总质量增加4g,N电极质量变化为克.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“碳是生命的核心元素”这种说法的依据是( )
A.蛋白质、核酸等生物大分子中都含有C、H、O三种元素
B.组成一些重要生物大分子的单体均以碳链为基本骨架
C.脂质、糖类及蛋白质等生物大分中的碳元素含量均最高
D.糖类是生物体内的主要能源物质,又称“碳水化合物”
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式书写及说法正确的是( )
A.CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=﹣890 kJ
B.C(s)+ ![]() O2(g)=CO(g)△H=﹣101.5 kJ?mol﹣1 , 该方程式的△H可表示碳的燃烧热
O2(g)=CO(g)△H=﹣101.5 kJ?mol﹣1 , 该方程式的△H可表示碳的燃烧热
C.Ba(OH)2(aq)+H2SO4(aq)=BaSO4(s)+2H2O(l)△H=﹣2a kJ?mol﹣1 , 则任何强酸和强碱发生中和反应生成1mol H2O(l)的反应热均为﹣a kJ?mol﹣1
D.2mol氢气燃烧得水蒸气放热484 kJ,则H2O(g)=H2(g)+ ![]() O2(g)△H=+242 kJ?mol﹣1
O2(g)△H=+242 kJ?mol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项操作中,错误的是( )
A. 用酒精萃取溴水中的溴单质的操作可选用分液漏斗,而后静置分液
B. 进行萃取操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
C. 萃取分液前需对分液漏斗检漏
D. 为保证分液漏斗内的液体顺利流出,需将上面的塞子拿下
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业炼铁用一氧化碳还原氧化铁时会发生如下一系列反应:
3Fe2O3+CO→2Fe3O4+CO2
Fe3O4+CO→3FeO+CO2
FeO+CO→Fe+CO2
某次实验中,用CO还原4.80g氧化铁,当固体质量变成4.56g时,测得此固体中只存在2种氧化物.则此固体成分和它们的物质的量之比可能的是( )
A.n(FeO):n(Fe3O4)=1:1
B.n(Fe2O3):n(FeO)=2:1
C.n(Fe2O3):n(FeO)=1:2
D.n(Fe2O3):n(Fe3O4)=1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 硫酸钡不溶于水,所以硫酸钡是非电解质
B. 铜可以导电,所以铜是电解质
C. 氯化钠溶液能导电,所以氯化钠溶液是电解质
D. 液态氯化氢不能导电,但氯化氢是电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列可以用来鉴别SO2和CO2的方法是()
①通入紫色石蕊试液中 ②闻气味 ③通入澄清石灰水中 ④通入品红溶液中 ⑤通入氯水中,再滴加Ba(NO3)2溶液。
A.①②
B.②③
C.②④⑤
D.③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com