
【题目】在通常条件下,下列各组物质的性质排列正确的是( )
A.熔点:Na>MgO>SiO2
B.水溶性:SO2>H2S>HCl
C.热稳定性:HF>H2O>NH3
D.沸点:HF>HCl>HBr
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】为减小和消除过量CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究。
(1)最近有科学家提出“绿色自由”构想:先把空气吹入饱和碳酸钾溶液,然后再把CO2从溶液中提取出来,并使之变为可再生燃料甲醇。“绿色自由”构想技术流程如下:
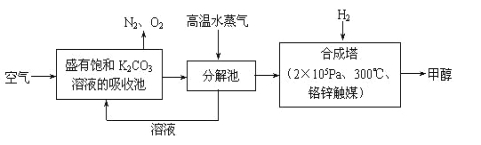
写出分解池中反应的化学方程式 。在合成塔中,当有4.4 kg CO2与足量H2完全反应,可放出热量4947 kJ,写出合成塔中反应的热化学方程式 。
(2)以CO2为碳源还可以制备乙醇,反应如下:
2CO2(g) + 6H2(g)=== CH3CH2OH(g) + 3H2O(g) △H=-173.6kJ/mol
写出由CH3OH(g)合成CH3CH2OH(g)的反应的热化学方程式 。
(3)某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置。

①该电池正极的电极反应为 。
②工作一段时间后,测得溶液的pH减小,该电池总反应的化学方程式为 。当电子转移 mol时,参加反应的氧气的体积是6.72L(标准状况下)。
(4)以甲醇为燃料还可制作新型燃料电池,电池的正极通入O2,负极通入甲醇,用熔融金属氧化物MO作电解质(可传导O2-)。该电池负极发生的电极反应是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W四种短周期元素在周期表中的位置关系如右图所示,其中Z元素原子的最外层电子数是其电子层数的2倍。
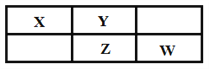
请回答下列问题:
(1)元素Z位于周期表中第_______周期,________族;
(2)这些元素的最高价氧化物对应的水化物中,水溶液酸性最强的是_______(写化学式);
(3)Y和Z组成的化合物的化学式为_______;
(4)W的单质和过量的X的氢化物可发生氧化还原反应,所得两种产物的电子式分别为____________、___________;
(5)W的最高价氧化物对应的水化物的浓溶液不稳定,受热可分解,产物之一是黄绿色气体,且当有28 mol 电子转移时,共产生9 mol 气体,写出该反应的化学方程式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,体积不变的密闭容器中,对可逆反应A(g) + 2B(g)![]() 3C(g) + D(s) 的下列叙述中,能说明反应已达到平衡的是:
3C(g) + D(s) 的下列叙述中,能说明反应已达到平衡的是:
A. 单位时间内消耗a mol A,同时生成3a mol C
B. C的生成速率与C的分解速率相等
C. 混合气体的总物质的量不再变化
D. 容器内的压强不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能在溶液中大量共存的一组离子是
A.NH4+ 、Ag+、PO43-、Cl- B.Fe3+、H+、I-、HCO3-
C.K+、Na+、NO3- 、MnO4- D.Al3+、Mg2+ 、SO42- 、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物A含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化:

据此回答下列问题:
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是____________。
(2)根据上述框图反应关系,写出下列B、D、E所含物质的化学式
固体B_________________;沉淀D __________________;
溶液E_________________________________________。
(3)写出①、④两个反应的化学方程式
①__________________________________;④_____________________________。
(4)写出②、③两个反应的离子方程式
②_________________________________;③______________________________。
(5)设计实验检验溶液F中所含溶质:______________________________________
(6)分别写出Al2O3和Fe2O3在工业上的一种主要用途:
Al2O3__________________________Fe2O3____________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 含金属元素的离子一定是阳离子
B. 金属阳离子被还原一定得到金属单质
C. 共价化合物中只含共价键
D. 1H、2H、3H互为同素异形体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com