
【题目】随着科学技术的不断进步,研究物质的手段和途径越来越多,H3、O4、C60、N5+等已被发现。下列有关说法中,正确的是( )
A.H2与H3中不存在氢键B.O2 与O4互为同位素
C.C60 分子中有范德华力D. N5+中含有35个电子
 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:
【题目】铁铬氧化还原液流电池是一种低成本的储能电池,电池结构如图一所示,工作原理为Fe3++Cr2+![]() Fe2++Cr3+。图二为利用H2S废气资源回收能量并得到单质硫的质子膜燃料电池。下列说法一定正确的是
Fe2++Cr3+。图二为利用H2S废气资源回收能量并得到单质硫的质子膜燃料电池。下列说法一定正确的是

A. 图一电池放电时,C1-从负极穿过选择性透过膜移向正极
B. 图一电池放电时,电路中每通过0.1mol电子,Fe3+浓度降低0.1mol/L
C. 用图二电池给图一装置充电时,图二中电极a接图一的正极
D. 用图二电池给图一装置充电时,每生成1molS2(s),图一装置中就有4molCr3+被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,分别改变相同物质的量浓度的H2CO3和氨水的pH,H2CO3、HCO3-、CO32-物质的量分数 (δ)及NH3·H2O、NH4+的物质的量分数(δ)如下图所示(不考虑溶液中的CO2和NH3分子):

[已知δ=![]() 、δ=
、δ=![]() ]
]
下列说法正确的是
A. NH4HCO3溶液显酸性
B. pH=5时,c(HCO3-)>c(H2CO3) >c(CO32-)
C. lgK1(H2CO3)=6.38
D. HCO3-+ NH3·H2O=NH4++CO32-+H2O的lgK=-0.95
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中属于氧化还原反应的是( )
A.CaCO3 ![]() CaO+CO2↑
CaO+CO2↑
B.Na2O+H2O=2NaOH
C.Na2CO3+2HCl=2NaCl+H2O+CO2↑
D.4HNO3(浓) ![]() 4NO2↑+O2↑+2H2O
4NO2↑+O2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中甲—戊分别为下述五种物质中的一种:CuSO4、H2SO4、Fe、Na2CO3和Ca(OH)2,且图中相连两个环对应的物质(或其溶液)在常温条件下能发生化学反应。

(1)上述五种物质中:
①可用于农业生产改良酸性土壤的是_________________。
②能相互发生置换反应的一个化学方程式为_________________________。
(2)若图中乙为H2SO4:
①甲或丙能否为CuSO4?答:_____________(填“可以”或“不可以”)。
②若乙与丁发生中和反应,则丙为_________________。
(3)若丙为铁,则甲与戊反应的离子方程式为___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一个蛋白质分子由四条肽链组成,364个氨基酸形成,则这个蛋白质分子含有的-COOH和-NH2 数目分别为 ( )
A. 366、366 B. 362、362 C. 4、 4 D. 无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用Pt作电极电解MgCl2溶液,下列关于电解装置正确的是( )
A. 总反应式:Mg+2H2O= Mg(OH) 2↓+H2↑
B. 负极反应式:Mg2+-2e-= Mg
C. 总反应式:Mg+2H2O= Mg(OH) 2+H2↑
D. 阴极电极反应式:2H++2e-= H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)某研究小组制备氯气并对产生氯气的条件进行探究。
(1)装置A中用MnO2与浓盐酸反应制取Cl2,利用了浓HCl的______(填“氧化性”或“还原性”)。
(2)A中产生的气体不纯,含有的杂质可能是______。
(3)B用于收集Cl2,请完善装置B并用箭头标明进出气体方向。____________
(4)C用于吸收多余的Cl2,C中发生反应的离子方程式是______。
(5)该小组欲研究盐酸的浓度对制Cl2的影响,设计实验进行如下探究。
实验 | 操作 | 现象 |
I | 常温下将MnO2和12 mol·L-1浓盐酸混合 | 溶液呈浅棕色,略有刺激性气味 |
II | 将I中混合物过滤,加热滤液 | 生成大量黄绿色气体 |
III | 加热MnO2和4 mol·L-1稀盐酸混合物 | 无明显现象 |
①已知MnO2呈弱碱性。I中溶液呈浅棕色是由于MnO2与浓盐酸发生了复分解反应,化学方程式是________。
②II中发生了分解反应,反应的化学方程式是________。
③III中无明显现象的原因,可能是c(H+)或c(Cl-)较低,设计实验IV进行探究:
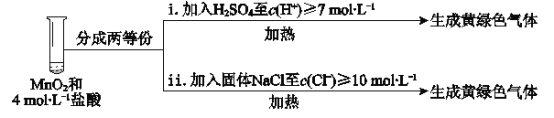
将实验III、IV作对比,得出的结论是________;将i、ii作对比,得出的结论是_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com