
【题目】用酸式滴定管准确移取25.00mL某未知浓度的盐酸溶液于一洁净的锥形瓶中,然后用0.2000mol·L-1的氢氧化钠溶液(指示剂为酚酞)滴定。滴定结果如下所示:
NaOH溶液起始读数 | NaOH终点读数 | |
第一次 | 0.10mL | 18.60mL |
第二次 | 0.30mL | 19.00mL |
(1)准确配制0.2000mol·L-1的氢氧化钠溶液250mL,需要的主要仪器除量筒、烧杯、玻璃棒外,还必须用到的玻璃仪器有___。
(2)根据以上数据可以计算出盐酸的物质的量浓度为___ mol·L-1。(保留4位有效数字)
(3)用0.2000mol·L-1标准氢氧化钠溶液滴定待测盐酸溶液,滴定时左手控制碱式滴定管的玻璃球,右手不停摇动锥形瓶,眼睛注视___,直到滴定终点。
(4)达到滴定终点的标志是___。
(5)以下操作造成测定结果偏高的原因可能是___ (填字母代号)。
A.未用标准液润洗碱式滴定管
B.滴定终点读数时,俯视滴定管的刻度,其他操作均正确
C.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
【答案】250mL容量瓶、胶头滴管 0.1448mol/L 锥形瓶内溶液颜色的变化 滴入最后一滴NaOH溶液,溶液颜色由无色变为浅红色,且半分钟不恢复原色 AD
【解析】
(1)中和滴定操作有:检漏、洗涤、润洗、装液、滴定等顺序,据此分析使用仪器;
(2)计算出消耗标准液的平均体积,然后根据c(待测)=![]() 计算;
计算;
(3)滴定时眼睛需要注视锥形瓶中溶液颜色变化,以便及时判断滴定终点;
(4)滴定结束前溶液为无色,滴定结束时溶液变为浅红色,据此判断的滴定终点现象;
(5)根据滴定操作方法对c(待测)=![]() 中V(标准)的影响分析滴定误差。
中V(标准)的影响分析滴定误差。
(1)中和滴定按照检漏、洗涤、润洗、装液、滴定等顺序操作,使用的仪器除量筒、烧杯、玻璃棒外,还必须选用250mL容量瓶、胶头滴管;
(2)第一次滴定消耗NaOH溶液体积为:18.60mL-0.10mL=18.50mL,第二次滴定消耗NaOH溶液体积为:19.00mL-0.30mL=18.70mL,两次滴定消耗NaOH溶液的平均体积为:![]() =18.60mL,则c(HCl)=
=18.60mL,则c(HCl)=![]() =
=![]() =0.1448mol/L;
=0.1448mol/L;
(3)用0.20molL-1标准氢氧化钠溶液滴定待测盐酸溶液,滴定时左手控制碱式滴定管的玻璃球,右手不停摇动锥形瓶,眼睛注视锥形瓶中溶液颜色变化,便于及时判断滴定终点;
(4)本实验是用NaOH滴定盐酸溶液,用酚酞作指示剂,所以终点时的现象是当溶液由无色变为浅红色,且在半分钟内不褪色;
(5)A.未用标准液润洗滴定管,会造成V(碱)偏大,根据c(待测)=![]() 可知,测定结果偏高,故A正确;
可知,测定结果偏高,故A正确;
B.滴定终点读数时,俯视滴定管的刻度,造成V(碱)偏小,根据c(待测)=![]() 可知,测定结果偏小,故B错误;
可知,测定结果偏小,故B错误;
C.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗,对实验结果无影响,故C错误;
D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液,造成V(碱)偏大,根据c(待测)=![]() 可知,测定结果偏大,故D正确;
可知,测定结果偏大,故D正确;
故答案选:AD。


科目:高中化学 来源: 题型:
【题目】草酸晶体(H2C2O4·2H2O)无色,熔点为101℃,易溶于水,受热脱水、升华,170℃以上分解。某学生拟用下图装置做草酸晶体的分解实验并验证部分产物,下列说法错误的是
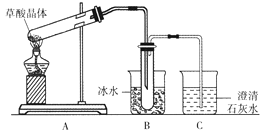
A. 装置A中的大试管口应略向下倾斜,是因为加热草酸晶体时会产生水
B. 装置B的主要作用是冷凝(水蒸气、草酸)等,防止草酸进入装置C中,干扰CO2的检验
C. 装置C中可观察到的现象是有气泡冒出,澄清石灰水变浑浊
D. 本实验能证明草酸晶体的分解产物有二氧化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向等物质的量浓度的NaOH和Na2CO3的混合溶液中加入稀盐酸.下列离子方程式可能与事实相符的是
A.OH﹣+2CO32﹣+3H+→2HCO3﹣+H2O
B.2OH﹣+CO32﹣+3H+→HCO3﹣+2H2O
C.2OH﹣+CO32﹣+4H+→CO2↑+3H2O
D.OH﹣+CO32﹣+3H+→CO2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国化学家侯德榜根据在相同的温度下NaHCO3溶解度比NaCl、Na2CO3、NH4HCO3和NH4Cl的溶解度都小的性质,运用CO2+NH3+H2O+NaCl→NaHCO3↓+NH4Cl的反应原理制备纯碱。下面是在实验室进行模拟实验的生产流程示意图:
![]()
则下列叙述正确的是( )
A.A气体是CO2,B气体是NH3
B.第Ⅲ步得到的晶体是难溶于水的
C.第Ⅲ步操作用到的主要玻璃仪器是烧杯、漏斗、玻璃棒
D.第Ⅳ步操作的主要过程有溶解、蒸发、结晶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L密闭容器内,800℃时反应2NO(g)+O2(g)![]() 2NO2(g)体系中,n(NO)随时间变化如下表:
2NO2(g)体系中,n(NO)随时间变化如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)写出该反应的平衡常数表达式:K=_____。已知:K(300℃)>K(350℃),则该反应正反应是_________热反应。升高温度,正反应速率_______(填“增大”、“减小”或“不变”)。
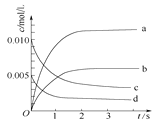
(2)下图中表示NO2的变化的曲线是____。用O2表示从0~2 s内该反应的平均速率v(O2)=______。
(3)能说明该反应已达到平衡状态的是__________。
A.v(NO2)=2v(O2) B.容器内压强保持不变
C.v逆(NO)=2v正(O2) D.容器内密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是_________。
A.及时分离出NO2气体 B.适当升高温度 C.增大O2的浓度 D.选择高效催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学实验课用KCl和NaNO3来制备KNO3的实验要用到减压过滤,下图是减压过滤的装置,请回答下列问题:

(1)写出图中A、B两种仪器的名称,
A_________________;B ___________________
(2)该装置图有几处错误,请指出B仪器处关键性的错误_____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机物中含有少量杂质![]() 括号中是杂质
括号中是杂质![]() ,除杂方法正确的是
,除杂方法正确的是
A.乙醇![]() 乙酸
乙酸![]() :加入碳酸钠溶液,振荡,静置,分液
:加入碳酸钠溶液,振荡,静置,分液
B.硝基苯![]() 硫酸
硫酸![]() :将其加入NaOH溶液中,振荡,静置,分液
:将其加入NaOH溶液中,振荡,静置,分液
C.乙醛![]() 乙酸乙酯
乙酸乙酯![]() :加入氢氧化钠溶液,振荡,静置,分液
:加入氢氧化钠溶液,振荡,静置,分液
D.溴乙烷![]() 溴
溴![]() :加入四氯化碳,振荡,静置,分液
:加入四氯化碳,振荡,静置,分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了得到比较纯净的物质,使用的方法恰当的是
A.向Na2CO3饱和溶液中,通入过量的CO2后,在加热的条件下,蒸发得NaHCO3晶体
B.向FeCl3溶液里加入足量NaOH溶液,经过滤、洗涤沉淀,再充分灼烧沉淀得Fe2O3
C.向FeBr2溶液中加入过量的氯水,加热蒸发得FeCl3晶体
D.加热蒸发AlCl3饱和溶液得纯净的AlCl3晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】滴定实验是化学学科中重要的定量实验。请回答下列问题:
Ⅰ.酸碱中和滴定——已知某NaOH试样中含有NaCl杂质,为测定试样中NaOH的质量分数,进行如下实验:
①称量1.00 g样品溶于水,配成250 mL溶液;
②准确量取25.00 mL所配溶液于锥形瓶中;
③滴加几滴酚酞溶液;
④用0.10 mol/L的盐酸标准液滴定三次,每次消耗盐酸的体积记录如下:
滴定序号 | 待测液体积mL | 所消耗盐酸标准液的体积/mL | |
滴定前读数 | 滴定后读数 | ||
1 | 25.00 | 0.50 | 20.60 |
2 | 25.00 | 6.00 | 26.00 |
3 | 25.00 | 1.10 | 21.00 |
(1)用__________滴定管(填“酸式”或“碱式”)盛装0.10 mol/L的盐酸标准液
(2)试样中NaOH的质量分数为__________
(3)若出现下列情况,测定结果偏高的是________
A.滴定前用蒸馏水冲洗锥形瓶
B.在振荡锥形瓶时不慎将瓶内溶液溅出
C.若在滴定过程中不慎将数滴酸液滴在锥形瓶外
D.酸式滴定管滴至终点时,俯视读数
E.酸式滴定管用蒸馏水洗后,未用标准液润洗
Ⅱ.氧化还原滴定
(4)取草酸溶液置于锥形瓶中,加入适量稀硫酸,用浓度为0.1 mol·L-1的高锰酸钾溶液滴定,发生的反应为2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O滴定时,KMnO4溶液应装在酸式滴定管中,滴定终点时现象是__________
(5)用0.01 mol/L的I2标准溶液滴定未知浓度的Na2S2O3溶液,选用的指示剂是__________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com