
【题目】下列各组混合中,用分液漏斗不能分离的是( )
A.苯和水B.乙酸乙酯和水C.乙酸和乙醇D.硝基苯和水
科目:高中化学 来源: 题型:
【题目】(1)某同学设计如下实验方案探究影响锌与稀硫酸反应速率的因素,有关数据如下表所示:
序号 | 纯锌粉(g) | 2.0 mol·L-1 硫酸溶液(mL) | 温度 (℃) | 硫酸铜固体(g) | 加入蒸馏水(mL) |
Ⅰ | 2.0 | 50.0 | 25 | 0 | 0 |
Ⅱ | 2.0 | 40.0 | 25 | 0 | 10.0 |
Ⅲ | 2.0 | 50.0 | 25 | 0.2 | 0 |
Ⅳ | 2.0 | 50.0 | 25 | 4.0 | 0 |
①本实验待测数据可以是________________________,实验Ⅰ和实验Ⅱ可以探究________________对锌与稀硫酸反应速率的影响。
②实验Ⅲ和实验Ⅳ的目的是________________,写出有关反应的离子方程式
_______________________________________________________________。
(2)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:

表中Vx=________mL,理由是_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为FeO·Cr2O3,还含有硅、铝等杂质。实验室由铬铁矿粉制备重酪酸流程如图所示:

已知步骤①的主要反应为:
![]()
(未配平)。有关物质的溶解度如图所示。

回答下列问题:
(1)滤渣2的主要成分是_________及含硅杂质。
(2)步骤④调滤液2的pH最合适的试剂是______________。
A.H2SO4溶液 B.KOH溶液 C.浓盐酸 D.K2CO3粉末
如何最简单的方法粗略判断pH已调至合适范围_________________。
(3)向“滤液3”中加入适量KCl,蒸发浓缩至_____________________,停止加热,然后冷却结晶,得到的K2Cr2O7固体产品。
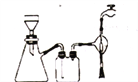
(4)本实验过程中多次用到抽滤的装置,下列关于抽滤的说法正确的是_______。
A.抽滤时,先用倾析法转移溶液,开大水龙头,待溶液快流尽时再转移沉淀
B.右图抽滤装置中只有2处错误
C.抽滤得到的滤液应从吸滤瓶的支管口倒出
D.洗涤沉淀时,应开大水龙头,使洗涤剂快速通过沉淀,减小沉淀的损失。
(5)某同学用mg铬铁矿粉(含Cr2O3 40%)制备K2C r2O7,为了测定产率,该同学设计了以下实验:将所有产品加水溶解并定容于500mL容量瓶中,移取25.00mL于碘量瓶(一种带塞的锥形瓶)中,加入过量2mol·L-1H2SO4,再加1.1KI,加塞摇匀,充分反应后铬完全以Cr3+存在,于暗处静置5min后,加指示剂,用0.0250mol·L-1标准Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液20.00mL。(已知:2 Na2S2O3+I2=Na2S4O6+2NaI)若滴定时振荡不充分,刚看到局部变色就停止滴定,则会使产量的测量结果__________(填“偏高”“偏低”或“无影响”)。计算该同学的产量_____________x100%(用含是m的式子表示,要求化简,m的系数保留两位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙酸钠是常用的防腐剂之一,该物质可以由丙酸与烧碱反应制得。下列有关丙酸的说法中不正确的是 ( )
A. 丙酸遇紫色石蕊溶液变红 B. 丙酸与烧碱的反应是取代反应
C. 丙酸与乙酸互为同系物 D. 丙酸与钠反应比丙醇与钠反应快得多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质的叙述不正确的是
A. 常温下,铝遇浓硝酸发生钝化 B. 钠在空气中燃烧生成白色的Na20粉末
C. 二氧化硫可以使品红溶液褪色 D. 葡萄糖与银氨溶液在适当条件下可发生银镜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“绿色化学实验”进课堂,某化学教师为“氯气与金属钠反应”设计了如下装置与操作以替代相关的课本实验.实验操作:钠与氯气反应的装置可作如图改进,将一根玻璃管与氯气发生器相连,玻璃管内放一块黄豆粒大的金属钠(已吸净煤油),玻璃管尾部塞一团浸有NaOH溶液的棉花球.先给钠预热,到钠熔融成圆球时,撤火,通入氯气,即可见钠着火燃烧,生成大量白烟.以下叙述错误的是( ) 
A.反应生成的大量白烟是氯化钠晶体
B.玻璃管尾部塞一团浸有NaOH溶液的棉球是用于吸收过量的氯气,以免其污染空气
C.钠着火燃烧产生苍白色火焰
D.若在棉球外沿滴一滴淀粉碘化钾溶液,可根据其颜色变化判断氯气是否被碱液完全吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于元素周期表和元素周期律的说法正确的是()
A. 由于F元素的最低化合价为-1价,故F元素的最高化合价为+7价
B. 第二周期元素从Li到F,非金属性逐渐减弱
C. 由于K比Na容易失去电子,所以K比Na的还原性强
D. 由于H2S的相对分子质量大于H2O的相对分子质量,所以沸点前者大于后者
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com