
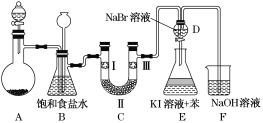
【题目】如图是实验室制备氯气并进行一系列相关实验的装置(夹持装置已略)。
(1)制备氯气选用的试剂为漂粉精固体和浓盐酸,则相关反应的化学方程式为________________。
(2)装置B中饱和食盐水的作用是__________________________________;
同时装置B也是安全瓶,监测实验进行时装置C是否发生堵塞,请写出发生堵塞时装置B中的现象: __________________________________________。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此装置C中Ⅰ、Ⅱ、Ⅲ处依次放入________(填字母)。
a | b | c | d | |
Ⅰ | 干燥的 有色布条 | 干燥的 有色布条 | 湿润的 有色布条 | 湿润的 有色布条 |
Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
Ⅲ | 湿润的 有色布条 | 湿润的 有色布条 | 干燥的 有色布条 | 干燥的 有色布条 |
(4)设计装置D、E的目的是比较氯、溴、碘的非金属性。当向D装置中缓缓通入一定量氯气时,可以看到无色溶液逐渐变为______色,说明氯的非金属性强于溴。
(5)打开活塞,将装置D中少量溶液加入装置E中,振荡后静置。观察到的现象是________。
【答案】Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O 除去Cl2中的HCl 长颈漏斗中液面上升,形成水柱 d 棕黄 装置E中液体分为两层,上层(苯层)为紫红色
【解析】
A装置来制备Cl2,制得的Cl2中含有HCl气体,利用饱和食盐水除去HCl,B中的长颈漏斗平衡内外压强,可以防倒吸,也可以判断后面的装置中是否发生了堵塞。装置C用于进行Cl2的性质实验。在D中Cl2与NaBr反应置换出Br2,Br2再与KI溶液反生置换出I2,I2被苯萃取,上层为紫红色;利用NaOH处理尾气。
(1)根据氧化还原反应的规律,次氯酸钙与浓盐酸反应生成氯化钙、氯气与水,反应的化学方程式为Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O;
(2)浓盐酸易挥发,反应制取的氯气中含有HCl,装置B中饱和食盐水的作用是除去Cl2中的HCl;
若装置C发生堵塞,装置B中的压强会增大,长颈漏斗中液面上升,形成水柱;
(3)验证氯气是否具有漂白性,要对比验证干燥氯气和湿润氯气有无漂白性,因此Ⅰ处应为湿润的有色布条,Ⅱ处应为干燥剂,Ⅲ处应为干燥的有色布条,U形管中应用固体干燥剂,综上d符合;
(4)当向装置D中缓缓通入少量氯气时,可以看到无色溶液逐渐变为棕黄色,发生反应:Cl2+2NaBr=2NaCl+Br2;
(5)打开活塞,将装置D中含Br2的少量溶液加入装置E中,发生反应:Br2+2KI=2KBr+I2,碘单质溶于苯,呈紫红色,振荡后静置,观察到的现象是装置E中液体分为两层,上层(苯层)为紫红色。


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:
【题目】有下列几种物质:A.石墨和金刚石 B. 35Cl和37Cl C.CH3CH=CHCH3和(CH3)2C=CH2 D.丁烷和新戊烷E. 
(1)属于同素异形体的是__________________
(2)属于同位素的是__________________
(3)属于同分异构体的是__________________
(4)属于同系物的是__________________
(5)属于同种物质的是__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验符合操作要求且能达到实验目的的是( )
A.I可用于制备氢气并检验其可燃性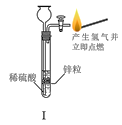
B.II可用于除去CO2中的HCl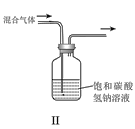
C.Ⅲ可用于配制一定物质的量浓度的NaOH溶液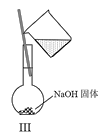
D.IV可用于制备氢氧化亚铁并长时间保存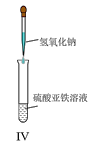
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃在标准状况下的密度为3.215 g/L,现取3.6 g该烃完全燃烧,将全部产物依次通入足量的浓硫酸和碱石灰,浓硫酸增重5.4 g,碱石灰增重11 g,求:
(1)该烃分子的摩尔质量。
(2)确定该烃的分子式。
(3)已知该烃的一氯代物只有一种,写出该烃的结构简式。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图装置制取并收集气体,对应的装置和试剂均正确的是( )
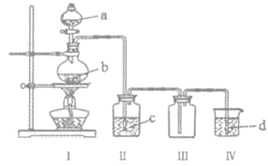
Ⅲ收集气体 | Ⅰ中试剂a,b | Ⅱ中试剂c | Ⅳ中试剂d | |
A | SO2 | 稀硫酸与铜片 | 浓硫酸 | NaOH溶液 |
B | Cl2 | 浓盐酸与二氧化锰 | 饱和氯化钠溶液 | NaOH 溶液 |
C | HBr | 浓硫酸与溴化钠 | 浓硫酸 | 水 |
D | CO | 甲酸与浓硫酸 | 浓硫酸 | 酸性KMnO4溶液 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究Na2SO3溶液的性质,在白色点滴板的a、b、c、d四个凹槽中滴入Na2SO3溶液,再分别滴加如图所示的试剂。
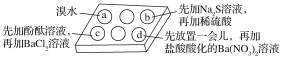
对实验现象的“解释或结论”错误的是( )
实验现象 | 解释或结论 | |
A | a中溴水褪色 | 还原性:SO32->Br- |
B | b中加硫酸后产生淡黄色沉淀 | SO32-和S2-在酸性条件下发生反应 |
C | c中滴入酚酞溶液变红,再加BaCl2溶液后产生白色沉淀且红色褪去 | SO32-+H2O Ba2++SO32-=BaSO3↓,水解平衡向左移动,红色褪去 |
D | d中产生白色沉淀 | Na2SO3溶液已变质 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.1mol有机化合物A与标准状况下5.6L氧气混合,一定条件下两者完全反应,只有CO、CO2和H2O三种产物,将全部产物依次通入足量的浓硫酸和碱石灰中,浓硫酸增重5.4克,碱石灰增重4.4克,还有标准状况下2.24L气体的剩余,求:
(1)有机化合物A的分子式_______(要求写出推理过程);
(2)若有机化合物A能与钠反应放出氢气,请写出A的结构简式_________;
(3)写出所有比A多一个—CH2—原子团的同系物的结构简式_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不能正确表示下列变化的离子方程式是
A.用醋酸除去水垢:2H++CaCO3=Ca2++CO2↑+H2O
B.用氢氧化钠溶液除去镁粉中的杂质铝:2Al+2OH-+2H2O =2AlO![]() +3H2↑
+3H2↑
C.室温下,测得小苏打溶液pH>7,证明碳酸是弱酸:HCO![]() +H2O
+H2O![]() H2CO3+OH-
H2CO3+OH-
D.将0.10 mol·L-1 NH4Fe(SO4)2溶液与0.40 mol·L-1 NaOH溶液等体积混合: ![]() +Fe3++4OH-=Fe(OH)3↓+NH3·H2O
+Fe3++4OH-=Fe(OH)3↓+NH3·H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将足量的CO2不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀的物质的量与所通入CO2的体积关系如图所示。下列关于整个反应过程中的叙述错误的是

A. Oa段反应的化学方程式是Ba(OH)2+CO2 =BaCO3↓+H2O
B. bc段与cd段所消耗CO2的体积相同
C. bc段反应的离子方程式是2AlO2-+3H2O+CO2 = 2Al(OH)3↓+CO32-
D. de段沉淀减少是由于BaCO3固体的消失
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com