
【题目】向稀硫酸中逐滴加入氢氧化钡溶液过程中的电导率如图,下列说法不正确的是:

A.A点硫酸浓度最大
B.B点溶液中离子浓度小于A点
C.C点的导电率不为零是因为硫酸有剩余
D.D点溶液中的主要离子为Ba2+和OH-
 一线名师提优试卷系列答案
一线名师提优试卷系列答案科目:高中化学 来源: 题型:
【题目】已知A,B,C,D,E、F六种元素的原子序数依次增大,其中A元素的原子半径在短周期元素中最小;B原子核外电子有6种不同的运动状态;D原子L层上有2对成对电子。E元素在地壳中含量居第二位,F 与E位于同一周期,且是该周期元素中电负性最大的元素。
根据以上信息回答下列问题:
(1)E元素可分别与D元素、F元素形成两种常见化合物,这两种化合物的熔沸点高低顺序为____________(用化学式表示),原因是_____________________。
(2)C的氢化物比下周期同族元素的氢化物沸点还要高,其原因是____________。
(3)1 mol B2A2分子中含σ键的数目是____________。
(4)图(Ⅰ)是B元素的单质晶体的一个晶胞,该晶胞中含有_____个原子,该晶体类型为________。
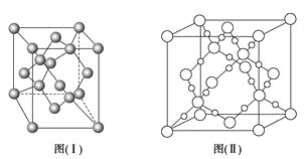
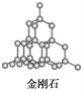
(5)E单质存在与金刚石结构类似的晶体,晶体中原子之间以_________相结合,其晶胞中共有8个原子,其中在面心位置贡献______个原子。
(6)BD2在高温高压下所形成的晶体其晶胞如图(Ⅱ)所示。该晶体的类型属于_______(填“分子”、“原子”、“离子”或“金属”)晶体,该晶体中B原子轨道的杂化类型为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四溴乙烷(CHBr2-CHBr2)是一种无色透明液体,密度2.967 g/mL,难溶于水,沸点244 ℃,可用作制造塑料的有效催化剂等。用电石(主要成分CaC2,少量CaS、Ca3P2、Ca3As2等)和Br2等为原料制备少量四溴乙烷的装置(夹持装置已省略)如图所示。
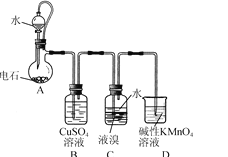
(1)装置A中CaC2能与水剧烈发生反应:CaC2+2H2O→Ca(OH)2+HC≡CH↑。为了得到平缓的C2H2气流,除可用饱和食盐水代替水外,还可采取的措施是________。
(2)装置B可除去H2S、PH3及AsH3,其中除去PH3的化学方程式为________(生成铜、硫酸和磷酸)。
(3)装置C中在液溴液面上加入一层水的目的是________;装置C中反应已完成的现象是________;从装置C反应后的体系得到并纯化产品,需要进行的操作有________。
(4)一种制备Ca10(PO4)6(OH)2的原理为10Ca(OH)2+6H3PO4=Ca10(PO4)6(OH)2↓+18H2O。请设计用装置A得到的石灰乳等为原料制备Ca10(PO4)6(OH)2的实验方案:向烧杯中加入0.25 L含0.5 mol/LCa(OH)2的石灰乳,________,在100 ℃烘箱中烘干1 h。
已知:
① Ca10(PO4)6(OH)2中![]() 比理论值为1.67。影响产品
比理论值为1.67。影响产品![]() 比的主要因素有反应物投料比及反应液pH。
比的主要因素有反应物投料比及反应液pH。
②在95 ℃,pH对![]() 比的影响如图所示。
比的影响如图所示。
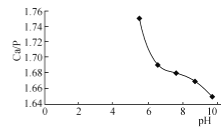
③实验中须使用的试剂:含0.5mol/LCa(OH)2的石灰乳、0.3mol/L磷酸及蒸馏水。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,有两种溶液:①0.01 mol·L-1 NH3·H2O溶液、②0.01 mol·L-1 NH4Cl溶液,下列操作可以使两种溶液中c(NH4+)都增大的是
A.通入少量HCl气体 B.加入少量NaOH固体
C.加入少量H2O D.适当升高温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如图所示装置,探究氯碱工业原理,下列说法正确的是

A. 石墨电极与直流电源负极相连
B. 铜电极的反应式为:2H2O+2e-![]() 2OH-+H2↑
2OH-+H2↑
C. 氢氧化钠在石墨电极附近产生, Na+ 向石墨电极迁移
D. 用湿润KI淀粉试剂在铜电极附近检验气体,试纸变蓝色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请将下列物质与其对应的性质或用途连线。
物质与性质 | 物质与用途 |
SO2 黄色固体 NO2 黄绿色气体 Cl2 红棕色气体 S 无色气体 | 氨气 发酵粉 过氧化钠 漂白粉 碳酸氢钠 制冷剂 次氯酸钙 供氧剂 |
__________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释相关的离子方程式错误的是
A. H2S溶于水:H2S+H2O![]() HS-+H3O+
HS-+H3O+
B. 向Na2S2O3溶液中加入稀硫酸:S2O3-+2H+=S↓+SO2↑+H2O
C. NH4Cl溶液呈酸性:NH4++H2O=NH3·H2O+H+
D. K2Cr2O7溶于水:Cr2O7-+H2O![]() 2CrO42-+2H+
2CrO42-+2H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.1mol/LCH3COOH溶液中存在如下电离平衡:CH3COOH![]() CH3COO-+H+对于该平衡,下列叙述正确的是( )
CH3COO-+H+对于该平衡,下列叙述正确的是( )
A. 加入水时,平衡向逆反应方向移动
B. 加入少量NaOH固体,平衡向正反应方向移动
C. 加入少量0.1mol·L-1 HCl溶液,溶液中c(H+)减小
D. 加入少量CH3COONa固体,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式如下:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。将15.8gKMnO4与足量的浓盐酸充分反应,产生气体的体积均在标准状况下测定,请计算:
(1)高锰酸钾的物质的量是___mol。
(2)产生的Cl2的体积是___L。
(3)若用MnO2与足量的浓盐酸反应制取相同体积的Cl2,理论上需要MnO2的质量是___克。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com