
【题目】如图表示组成细胞的元素、化合物及其作用,a、b、c、d代表小分子物质,A、B、C代表大分子物质,下列叙述正确的有 ( )。
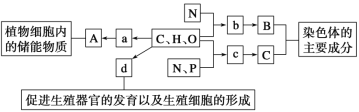
①物质A是淀粉和纤维素,在动物细胞内与其具有相似功能的物质是糖原
②物质a、b、c分别为葡萄糖、氨基酸、脱氧核糖
③物质d进入细胞时不需要消耗ATP,也不需要载体的协助
④若构成两个大分子物质B的小分子物质b的种类和数量相同,则这两个大分子物质B一定相同
A. 0项B. 1项C. 2项D. 3项
科目:高中化学 来源: 题型:
【题目】(1)800℃时,某密闭容器中存在如下反应:2NO2(g) ![]() 2NO(g) + O2(g) △H>0,若开始向容器中加入1mol/L的NO2,反应过程中NO的浓度随时间的变化如图曲线I所示
2NO(g) + O2(g) △H>0,若开始向容器中加入1mol/L的NO2,反应过程中NO的浓度随时间的变化如图曲线I所示
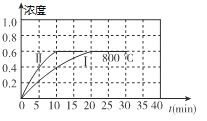
①反应Ⅱ相对于反应I而言,改变的条件可能是_______________.
②800℃时,若开始时向容器中同时加入1mol/LNO、0.2mol/LO2、0.5mol/L NO2,则v正____________v逆(填“<”、“>”或“=”)
(2)己知N2O4(g) ![]() 2NO2(g) △H=+57.20kJ/mol,t min时,将一定量的NO2、N2O4,充入一个容器为2L的恒容密闭容器中,浓度随时间变化关系如下表所示:
2NO2(g) △H=+57.20kJ/mol,t min时,将一定量的NO2、N2O4,充入一个容器为2L的恒容密闭容器中,浓度随时间变化关系如下表所示:
时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
c(X)/(mol/L) | 0.2 | c | 0.6 | 0.6 | 1.0 | c1 | c1 |
c(Y)(mol/L) | 0.6 | c | 0.4 | 0.4 | 0.4 | c2 | c2 |
①c(X)代表__________(填化学式)的浓度,该反应的平衡常数K=_____________。
②前10min内用NO2浓度变化表示的反应速率为___________,20min时改变的条件是_____________;重新达到平衡时,NO2的质量分数___________________。
a.增大 b.减小
c.不变 d.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 石油的催化重整可以得到芳香烃,说明石油中含有芳香烃
B. 煤的干馏和石油裂解得到的产物相同
C. 石油分馏得到的产物可用来萃取溴水中的溴
D. 聚丙烯塑料的结构简式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应3Fe(s)+4H2O(g)![]() Fe3O4(s)+4H2(g) △ H﹥0,在一容积可变的密闭容器中进行,试回答:
Fe3O4(s)+4H2(g) △ H﹥0,在一容积可变的密闭容器中进行,试回答:
(1)增加Fe的量,其正反应速率__________(填“增大”“不变”或“减小”,下同),平衡__________移动(填“不”“向正反应方向”或“向逆反应方向”,下同)。
(2)将容器的体积缩小一半,其正反应速率__________,平衡__________移动。
(3)升高温度,其正反应速率__________,平衡__________移动。
(4)保持体积不变,充入水蒸气,其正反应速率________,平衡________移动。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如下:


可能用到的有关数据如下:
相对分子质量 | 密度/g·cm-3 | 沸点/℃ | 溶解性 | |
环己醇 | 100 | 0.961 8 | 161 | 微溶于水 |
环己烯 | 82 | 0.810 2 | 83 | 难溶于水 |
合成反应:
在a中加入20 g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1 mL浓硫酸。b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90 ℃。
分离提纯:
反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙。最终通过蒸馏得到纯净环己烯10 g。
回答下列问题:
(1)装置b的名称是________。
(2)加入碎瓷片的作用是_____________________________________________________;
如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是________(填字母,下同)。
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(3)本实验中最容易产生的副产物的结构简式为____________________________________。
(4)分液漏斗在使用前须清洗干净并_____;在本实验分离过程中,产物应该从分液漏斗的_____(填“上口倒出”或“下口放出”)。
(5)分离提纯过程中加入无水氯化钙的目的是______________________________。
(6)在环己烯粗产物蒸馏过程中,不可能用到的仪器有________。
A.接收器 B.温度计 C.吸滤瓶 D.球形冷凝管
(7)本实验所得到的环己烯产率是________。
A.41% B.50% C.61% D.70%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,向圆底烧瓶中加入1 molC2H5OH和含1molHBr的氢溴酸,溶液中发生反应:C2H5OH+HBr![]() C2H5Br+H2O,充分反应后达到平衡。已知常压下,C2H5Br和C2H5OH的沸点分别为38.4℃和78.5℃。下列有关叙述错误的是( )
C2H5Br+H2O,充分反应后达到平衡。已知常压下,C2H5Br和C2H5OH的沸点分别为38.4℃和78.5℃。下列有关叙述错误的是( )
A. 加入NaOH溶液,可增大乙醇的物质的量
B. 增大氢溴酸的浓度,有利于生成C2H5Br
C. 若反应物均增大至2 mol,则两种反应物平衡转化率之比变大
D. 若起始温度提高至60℃,有利于提高C2H5Br的产量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为铜锌原电池示意图,下列关于锌铜原电池的说法正确的是( )

A. 负极发生的反应是:2H+ +2e—=H2↑
B. 溶液中SO42-向铜片的方向移动
C. 该装置实现了化学能转化为电能
D. 若生成0.2mol H2,则有6.5克锌被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)是一种重要的工业盐,易溶于水,微溶于乙醇。某化学兴趣小组对亚硝酸钠进行多角度探究:
Ⅰ.亚硝酸钠的制备。

(1)装置B的作用是___________________________________________。
(2)D中澄清石灰水变浑浊,则C中制备NaNO2的离子方程式为______________。
Ⅱ.探究亚硝酸钠与硫酸反应的气体产物成分。
已知:①NO+NO2+2OH-=2NO+H2O
②气体液化的温度:NO2为21 ℃,NO为-152 ℃
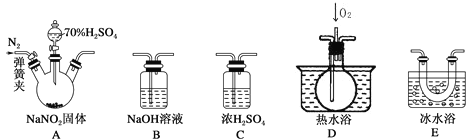
(3)反应前应打开弹簧夹,先通入一段时间氮气,目的是_______________________。
(4)仪器的连接顺序(按左→右连接):A→C→________。
(5)在关闭弹簧夹,打开分液漏斗活塞,滴入70%硫酸后,装置A中产生红棕色气体。
①确认装置A中产生的气体含有NO,依据的现象是_______________________。
②若D中通入过量O2,装置B中的化学方程式是_______________________。
Ⅲ.设计实验证明酸性条件下NaNO2具有氧化性。
(6)供选用的试剂:NaNO2溶液、KMnO4溶液、Fe2(SO4)3溶液、KI溶液、稀硫酸、淀粉溶液、KSCN溶液___________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物X是一种重要的有机化工原料,下图是以它为初始原料设计出的转化关系图(部分产物、合成路线、反应条件略去),Y是一种功能高分子材料。
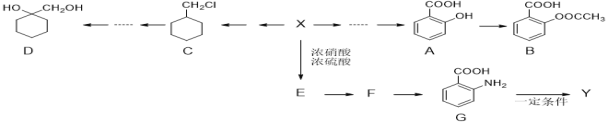
已知:
(1)X为芳香烃,其相对分子质量为92;
(2)烷基苯在高锰酸钾的作用下,侧链被氧化成羧基:![]() ;
;
(3)![]() (苯胺,易被氧化);
(苯胺,易被氧化);
回答下列问题:
(1)X的名称为________________,G的分子式为____________________。
(2)F的结构简式为___________________,B中官能团的名称为____________。
(3)X→E的反应类型为__________________________。
(4)A→B的化学方程式为__________________________。
(5)满足下列条件的B的同分异构体有________种。
①含有苯环;②只含一种官能团;③1 mol该有机物能与2 mol NaHCO3完全反应。
(6)请写出以C为原料制备![]() 的合成路线流程图(无机试剂任用)_________。
的合成路线流程图(无机试剂任用)_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com