
����Ŀ��X��Y��Z��W����ԭ������������������ֶ���������Ԫ�ء�����������������������Ԫ�����ڱ��У�Y��Z��W��λ����ͼ��ʾ����Y��Z��W����Ԫ�ص�ԭ������������֮��Ϊ17����X��Y��W�ֱ�λ�ڲ�ͬ���ڡ�����˵����ȷ����

A. ����Ԫ�ص�ԭ�Ӱ뾶��С˳��ΪW>Y>X>Z
B. Z��WԪ�ص�����⻯��ķе�ΪH2Z<H2W
C. X��Y��Z�����γ����ӻ���������γɹ��ۻ�����
D. X�ֱ���Y��Z֮���γɵĺ����������Ϊ10����ֻ��YX3��X2Z
���𰸡�C
������������������Ԫ�صĽṹ���������ڱ��е�λ�ÿ�֪��X��Y��Z��W�ֱ���H��N��O��S��
�����A��ͬ����Ԫ�ش����ң�ԭ�Ӱ뾶��С��ͬ����Ԫ�أ�ԭ�Ӱ뾶��������ԭ�Ӱ뾶˳����r��X����r��Z����r��Y����r��W����A����
B��Z��W�ֱ���O��S��ˮ�������γɵľ��嶼�Ƿ��Ӿ��壬��ˮ�����л�����������Էе�ˮ�ĸߣ���H2Z�ķе��H2W�ߣ�B����
C��X����������Ԫ��֮���γɵĺ����������Ϊ10������NH3��NH4����NH2����H2O��OH����H3O������6�֣�C����
D��X��Y��Z�γɵĻ�������������ǹ��ۻ��������������ӻ����D��ȷ��
��ѡD��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£����ܵ���ʵı�����Һ�д����ų����ܽ�ƽ�⣬��֪��
���� | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
Ksp(25 ��) | 8.0��10��16 | 2.2��10��20 | 4.0��10��38 |
25 ��ʱ�����ں�Fe2(SO4)3��FeSO4��CuSO4��0.5 mol��1 L�����Һ�������ϱ������жϣ�����˵������ȷ����(����)
A. ��pH��5����Һ�У�Fe3�����ܴ�������
B. �����Һ��c(SO![]() )��[c(Fe3��)��c(Fe2��)��c(Cu2��)]>5��4
)��[c(Fe3��)��c(Fe2��)��c(Cu2��)]>5��4
C. ������Һ����μ���0.1 mol��L��1NaOH��Һ�����ȿ������ɫ����
D. ������Һ�м���������ˮ��������pH��3��4���ˣ��ɻ�ϴ�����CuSO4��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ơ���װ��ʹ�÷�������ѧ��ѧʵ��Ļ�������ͼΪ����ʵ��װ�á�
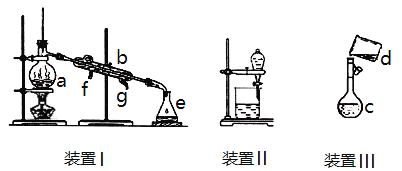
(1)д���������������ƣ�a.___________________b.____________________��
(2)������װ��I�������Ȼ�̼�;ƾ��Ļ�������ˮ��_____(��f��g)��ͨ�롣
(3)��װ��II��������ʱ��ΪʹҺ��˳�����£�Ӧ���еIJ�����_____________��
(4)ʵ������Na2CO3��10H2O��������0.05mol/L��Na2CO3��Һ970mL��
��Ӧ��������ƽ��ȡNa2CO3��10H2O��������_____________g��
��װ��III��ijͬѧת����Һ��ʾ��ͼ��ͼ�еĴ�����___________________��
(5)����ʱ�����ӿ̶��ߣ���������ҺŨ�ȵ�Ӱ�죺_____________(�ƫ��ƫС������Ӱ��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�ͬ���칹����Ŀ�������У���ȷ����
A. C2H6Oֻ��һ�ֽṹ
B. ����ʽ����C5H11Cl �Ļ�������6��
C. ��֪���ȱ���3��ͬ���칹�壬�����ȱ���ͬ���칹�����ĿΪ3��
D. �ƵĽṹ��ʽΪ![]() ���������ᷴӦ��������10��һ����ȡ����
���������ᷴӦ��������10��һ����ȡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̫���ܵ�ذ���ϳ��������⣬����ͭ�������ء����Ȼ�ѧ���ʡ�
��1����̬ͭԭ�ӵĵ����Ų�ʽΪ_____________����֪������CuO![]() Cu2O+O2����ͭԭ�Ӽ۲���ӽṹ(3d��4s�����Ӧ���ĵ�����)�仯�Ƕ�������������Cu2O��ԭ����___________________________��
Cu2O+O2����ͭԭ�Ӽ۲���ӽṹ(3d��4s�����Ӧ���ĵ�����)�仯�Ƕ�������������Cu2O��ԭ����___________________________��
��2���������������Ԫ���γ���̬�⻯��������γɵ�����⻯���У����ӹ��ͷֱ�Ϊ____________�� ����Si-H���й��õ��Ӷ�ƫ����Ԫ�أ�����������Ӧʱ�����������������������ĵ縺����Դ�СΪSe____Si ���>������<���������ǰѹ�����Ԫ���γɵ�һ�����й��顣�������ɡ��ṹ����Ӧ���������ƣ�����ķе�����Է��������Ĺ�ϵ��ͼ��ʾ���������ֱ仯��ԭ����_____________________________________________��

��3����������Ԫ�ش���ͬһ�������Ԫ�ؾ���ȱ������(�۵��������ڼ۲�����)���仯���������йµ��ӶԵķ��ӻ���������������BF3����NH3��Ӧ����BF3��NH3��BF3��NH3��Bԭ�ӵ��ӻ��������Ϊ______�� B��N֮���γ�___________����
��4�����ɰ(SiC)��Ӳ��Ϊ9.5���侧���ṹ����ͼ��ʾ������ɰ��������Ϊ_________________����SiC�У�ÿ��Cԭ����Χ�����Cԭ����ĿΪ___�����������ı߳�Ϊa pm������ɰ���ܶ�Ϊ____g/cm3 ����NA��ʾ����٤��������ֵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���Ԫ���� H2Y ��Һ�еμ� KOH ��Һ�����û����Һ�� pH ������Ũ�ȱ仯�Ĺ�ϵ����ͼ��ʾ�������й�˵����������

A. ���� M ��ʾ pH�� lg![]() �ı仯��ϵ
�ı仯��ϵ
B. a����Һ�У�c(H+) �D c(OH-)��2c(Y2��)��c(HY-) �D c(K+)
C. H2Y �ĵڶ������볣��Ka2(H2Y)��10��4.3
D. ����b����Һ�У�c(H2Y)��c(Y2-)��c(HY-)��c(H+)��c(OH-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ŀǰ����β���е�NO���������¼��ַ�����
��1���������������ϰ�װ��ת������NO��CO�����Ϊ����β���ijɷ֣������������ڴ�ת�����з�����Ӧ��2CO(g)��2NO(g)![]() N2(g)��2CO2(g) ��H ��
N2(g)��2CO2(g) ��H ��
����֪��N2(g)+O2(g)=2NO(g)��H1����180.5kJ��mol��1
C(s)+O2(g)=CO2(g) ��H2����393.5kJ��mol��1
2C(s)+O2(g)=2CO(g)��H3����221kJ��mol��1
���H=______��
��һ����ȤС���ij����������ʱ��β��������������CO��NO�ٷֺ�����ʱ��仯��ͼ1��ʾ��ǰ0��10s �Σ�CO��NO�ٷֺ���û���Ա仯��ԭ����_____________________��ͬʱ��С���ڹ̶��ݻ�Ϊ2L���ܱ�������ͨ��NO��CO��2mol���з�Ӧ��n(CO2)���¶ȣ�T����ѹǿ��P����ʱ�䣨t���ı仯������ͼ2��ʾ��ͼ�е����ߢ��Ӧ��Ӧ�ӿ�ʼ��ƽ��ʱ��CO2��ʾ��ƽ����Ӧ���ʷֱ�Ϊv(��)��v����v���������ߴ�С��ϵΪ______________��

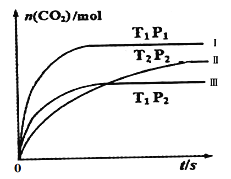
ͼ1 ͼ2
��2������̿Ҳ�����ڴ�������β���е�NO����1L�����ܱ������м���0.1000molNO��2.030mol�������̿������A��B�������壬�ڲ�ͬ�¶��²��ƽ����ϵ�и����ʵ����ʵ����Լ�������ѹǿ���±���
����̿/mol | NO/mol | A/mol | B/mol | P/MPa | |
200�� | 2.000 | 0.0400 | 0.0300 | 0.0300 | 3.93 |
X | 2.005 | 0.0500 | 0.0250 | 0.250 | 4.56 |
�����ϱ����ݣ�д�������з�����Ӧ�Ļ�ѧ����ʽ____�����ж�X_____200�棨�á���������������=����գ������㷴Ӧ��ϵ��200��ʱ��ƽ�ⳣ��Kp =_____����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ=��ѹ�������������
��3���ü�ӵ绯ѧ����ȥNO�Ĺ��̣���ͼ��ʾ����֪���ص�����������Һ��pH��4~7֮�䣬B��Ϊ_________(���������������)��д��A���ĵ缫��Ӧʽ��____________��
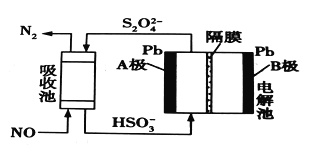
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���X��ij��ҩ�����Ҫ�ɷ֣���ҵ�Ϻϳɸû������һ��·������(���ַ�Ӧ���Ӧ������ȥ)��

��֪�����뺬�ǻ��Ļ�����ɷ���������������Ӧ��RCOO R�䣫R��OH![]() RCOOR�士R��OH(R��R�䡢R�����������)��
RCOOR�士R��OH(R��R�䡢R�����������)��
��1����Ӧ��������Լ���_______����Ӧ�ڵķ�Ӧ������_________��
��2��B�к��������ŵ�������________����Ӧ�ܵIJ������X���⣬��һ�ֲ����������________��
��3��D��һ���������ܷ������۷�Ӧ���ɸ߷��ӻ�����ø߷��ӻ�����Ľṹ��ʽΪ____________��
��4����Ӧ�۵Ļ�ѧ����ʽΪ_______________________��
��5��E��ͬ���칹���ж��֣�д�����������������л���ṹ��ʽ________��
��.������һ�ȴ���ֻ��һ��
��.���Ȼ�����Һ������ɫ��Ӧ
��.����̼��������Һ��Ӧ�ų�CO2
��6����֪����![]()
![]()
![]() ���ڵ�����������һ������CH3����Cl��ʱ���������ȡ����һ����������λ���λ��������������һ������NO2����COOH��ʱ���������ȡ����һ�������ļ�λ����д���Լױ����Ҵ�Ϊԭ���Ʊ�
���ڵ�����������һ������CH3����Cl��ʱ���������ȡ����һ����������λ���λ��������������һ������NO2����COOH��ʱ���������ȡ����һ�������ļ�λ����д���Լױ����Ҵ�Ϊԭ���Ʊ� �ĺϳ�·��ͼ(���Լ�����)____________��
�ĺϳ�·��ͼ(���Լ�����)____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ����Ũ�Ⱦ�Ϊ0.1mol��L-1��Na0H ��Һ������ֱ�ζ������Ϊ20mL��Ũ�Ⱦ�Ϊ0.1mol��L-1��HA��Һ��BOH��Һ���ζ���������Һ��pH��μ���Һ������仯��ϵ��ͼ��ʾ������˵������ȷ����

A. HAΪ���ᣬBOHΪǿ��
B. a��ʱ����Һ������Ũ�ȴ��ڹ�ϵ��c(B+)>c(Cl-)>c(OH-)>c(BOH)
C. b��ʱ����ЭҺ��ˮ�ĵ���̶���ͬ����V=20
D. c��d������Һ��Ϻ���֮����ڹ�ϵ��c(H+)= c(OH-)+c(BOH)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com