
【题目】现有五种元素,其中A、B、C为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
A元素的核外电子数和电子层数相等 |
B元素原子的核外p电子数比s电子数少1 |
C原子第一至第四电离能如下: I1=738 kJ·mol-1,I2=1451 kJ·mol-1,I3=7733 kJ·mol-1,I4=10540 kJ·mol-1 |
F是前四周期中电负性最小的元素 |
G在周期表的第八列 |
(1)已知BA5为离子化合物,写出其电子式:________。
(2)B元素基态原子中能量最高的电子,其电子云在空间有______个方向,原子轨道呈____形。
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为![]() ,该同学所画的电子排布图违背了___________________________________。
,该同学所画的电子排布图违背了___________________________________。
(4)G位于第____族____区,该元素的核外电子排布式为_____________________。该二价离子很容易被氧化成三价离子,从原子轨道理论解释原因________________________
(5)检验F元素的方法是___,请用原子结构的知识解释产生此现象的原因: ______。
【答案】![]() 3 哑铃(或纺锤) 泡利原理 Ⅷ d 1s22s22p63s23p63d64s2或[Ar] 3d64s2 Fe2+外围电子排布为3d6容易失一个电子变为3d5半充满状态 焰色反应 当基态原子的电子吸收能量后,电子会跃迁到较高能级,变成激发态原子。电子从较高能量的激发态跃迁到较低能量的激发态或基态时,将以光的形式释放能量
3 哑铃(或纺锤) 泡利原理 Ⅷ d 1s22s22p63s23p63d64s2或[Ar] 3d64s2 Fe2+外围电子排布为3d6容易失一个电子变为3d5半充满状态 焰色反应 当基态原子的电子吸收能量后,电子会跃迁到较高能级,变成激发态原子。电子从较高能量的激发态跃迁到较低能量的激发态或基态时,将以光的形式释放能量
【解析】
A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大,A元素的核外电子数和电子层数相等,A为H元素;B元素原子的核外p电子数比s电子数少1,B有2个电子层,为1s22s22p3,故B为N元素;由C原子的第一至第四电离能数据可以知道,第三电离能剧增,故C表现+2价,处于ⅡA族,原子序数大于N元素,故C为Mg元素;F是前四周期中电负性最小的元素,F为第四周期元素,故F为K元素;G在第四周期周期表的第8列,G为Fe元素,据此解答。
(1)NH5为离子化合物,是由NH4+与H-两种离子构成,电子式为![]() ,因此,本题正确答案是:
,因此,本题正确答案是:![]() ;
;
(2)B为N元素,核外电子排布式为1s22s22p3,基态原子中能量最高的电子,处于2p能级,有3个电子,其电子云在空间有3个方向,原子轨道呈纺锤形,因此,本题正确答案是:3;纺锤;
(3)某同学根据上述信息,推断C基态原子的核外电子排布为![]() ,该同学所画的电子排布图中3s能级,2个电子自旋方向相同,违背了泡利原理,因此,本题正确答案是:泡利原理;
,该同学所画的电子排布图中3s能级,2个电子自旋方向相同,违背了泡利原理,因此,本题正确答案是:泡利原理;
(4)G为Fe元素,是26号元素,位于第四周期第Ⅷ族,最后填充的为d电子,为d区元素,核外电子排布式为:1s22s22p63s23p63d64s2或[Ar] 3d64s2;Fe2+容易被氧化为Fe3+的原因是Fe2+外围电子排布为3d6容易失一个电子变为3d5半充满状态,因此,本题正确答案是:Ⅷ;d;1s22s22p63s23p63d64s2或[Ar] 3d64s2;Fe2+外围电子排布为3d6容易失一个电子变为3d5半充满状态;
(5)F为K元素,检验F元素的方法是焰色反应,产生此现象的原因是当基态原子的电子吸收能量后,电子会跃迁到较高能级,变成激发态原子。电子从较高能量的激发态跃迁到较低能量的激发态或基态时,将以光的形式释放能量,因此,本题正确答案是:焰色反应;当基态原子的电子吸收能量后,电子会跃迁到较高能级,变成激发态原子。电子从较高能量的激发态跃迁到较低能量的激发态或基态时,将以光的形式释放能量。


科目:高中化学 来源: 题型:
【题目】控制和治理CO2是解决温室效应及能源问题的有效途径。
已知:H2(g)和CH3OH(l)的标准燃烧热分別为△H=akJmol-1和△H=bkJmol-1
(1)研究表明,在Cu/ZnO催化剂存在下,CO2和H2 反应生成液态甲醇和液态水,该反应的热化学方程式为_________。
(2)已知:2CO2(g)+ 6H2(g)C2H4(g)+4H2O(g)△H,在两个固定容积均为1L的密闭容器中以不同的氢碳比[![]() ]充入H2和CO2,CO2的平衡转化率a(CO2)与温度的关系如图所示。
]充入H2和CO2,CO2的平衡转化率a(CO2)与温度的关系如图所示。
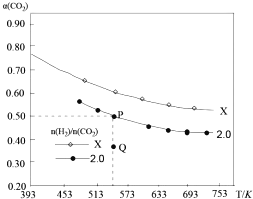
① X_______________(填“>”“<”或“=”) 2.0 ;
②若起始加入的CO2、H2的物质的量分別为1mol和2mol,计算P点时的化学平衡常数K=____________。
③比较P点和Q点的化学平衡常数:KP_________KQ(填“>”“<”或“=”),理由是__________________。
④一定温度下在体积为VL的容器中进行该反应,下列一定能说明反应达到平衡状态的是_______________(填字母序号)。
A.混合气体的平均相对分子质量不再变化
B.容器内气体总压强不再变化
C.2v正(CO2)=v逆(C2H4)
D.容器内混合气体的密度不再变化
(3)以CH3OH作燃料,以NaOH溶液作电解质溶液形成的燃料电池,电池工作时,溶液中的阴离子向电池的哪一极定向移动(填写电极名称)________;写出负极的电极反应式_________.
(4)常温下,若在![]() 硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的
硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的![]() 时,
时,![]() ____
____![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】伞形花内酯的一种制备方法如下: 下列说法不正确的是( )
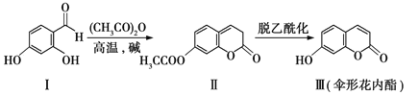
A. Ⅰ、Ⅱ、Ⅲ均能发生水解反应
B. Ⅰ、Ⅱ、Ⅲ均能与溴水反应
C. 检验化合物Ⅱ中是否混有化合物Ⅰ,可用FeCl3溶液
D. 与化合物Ⅰ官能团种类、数目均相同且含有苯环的同分异构体有5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列各组物质
①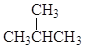 和
和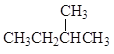 ②
②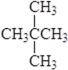 和
和![]() ③CH4和CH3CH2CH3 ④ 金刚石和石墨 ⑤ H、D、T ⑥ 16O、17O、18O ⑦乙醇(CH3CH2OH)和甲醚(CH3OCH3) ⑧臭氧(O3)和氧气(O2)。
③CH4和CH3CH2CH3 ④ 金刚石和石墨 ⑤ H、D、T ⑥ 16O、17O、18O ⑦乙醇(CH3CH2OH)和甲醚(CH3OCH3) ⑧臭氧(O3)和氧气(O2)。
属于同素异形体的是________________;互为同位素的是_________________;
互为同系物的是___________________;互为同分异构体的是_____________。(请将正确的序号填在横线上)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分。
碳 | 氮 | Y | |
X | 硫 | Z |
回答下列问题
(1)Z元素在周期表中的位置为__________。
(2)元素周期表中与Z元素同周期原子半径最大的是(写元素名称)__________,其最高价氧化物对应的水化物含有的化学键类型____________。
(3)下列事实能说明Y元素的非金属性比硫元素的非金属性强的是___;
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
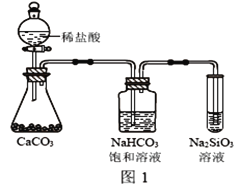
(4)根据下图实验,可以证明碳的非金属性比X强。饱和小苏打溶液的作用__________。发生的离子方程式是:__________________
(5)重水(D2O)是重要的核工业原料,下列说法错误的是________。
a.氘(D)原子核内有1个中子
b.1H与D互称同位素
c.H2O与D2O互称同素异形体
d.1H218O与D216O的相对分子质量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组设计实验探究元素周期律,如图所示。
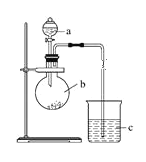
(1)仪器a的名称是____________,加入的药品为稀硝酸;仪器b的名称是____________,加入的药品为碳酸钠固体;b中反应现象为___________,验证氮的非金属性比碳的___(填“强”或“弱”)。
(2)c中装有硅酸钠溶液,c中反应现象为____,验证硅的非金属性比碳的___(填“强”或“弱”)。
(3)结论:同一周期从左到右元素非金属性逐渐____(填“增强”或“减弱”);同一主族从上到下元素非金属性逐渐_______(填“增强”或“减弱”)。
(4)某同学考虑到稀硝酸的挥发,则应在装置b和c之间增加一个盛有_______试剂的洗气瓶。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁及其化合物有重要且广泛的应用
(1)基态Fe2+的价层电子的轨道表示式为_____________
(2)检验Fe3+可以用KSCN溶液,写出SCN-的一种等电子体分子_______。
(3)部分电离能数据如下表:
元素 | Mn | Fe | |
电离能(kJ/mol) |
| 717 | 759 |
| 1 509 | 1 561 | |
| 3 248 | 2 957 | |
根据表中数据可知,气态Mn2+ 再失去一个电子比气态Fe2+ 再失去一个电子难,其原因是_______________________________________________________
(4)过渡金属原子可以与CO分子形成配合物,配合物价电子总数符合“18电子规则”。如Cr可以与CO形成Cr(CO)6 分子:价电子总数(18)= Cr的价电子数(6)+CO提供电子数(2×6).Fe原子也能与CO形成配合物,其化学式为________.
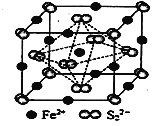
(5)FeS2晶体的晶胞如图所示。晶胞边长为a nm、FeS2相对式量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为___________g·cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
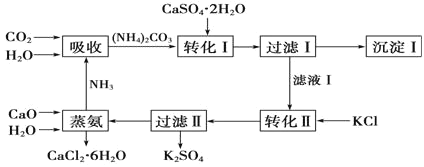
【题目】石膏转化为硫酸钾和CaCl2的工艺流程如图:
![]()
(1)CO2是一种很重要的副产品,工业上获得CO2的途径是___(用化学方程式表示)。
(2)过滤Ⅰ得到的滤液是___,检验滤液中含有CO32-的方法__。
(3)转化Ⅱ中发生反应的化学方程式为___,转化Ⅱ中可获得K2SO4的原因是__。
(4)氯化钙结晶水合物是目前常用的无机储热材料,选择的依据是___。
a.熔点较低(29℃熔化) b.能制冷
c.无毒 d.能导电
(5)废水中氨氮(主要以NH4+和NH3形式存在)的去除常见的有生物脱氮法和电解法。而电解法产生的强氧化物质HClO也可将氨氮转化为氮气而除去,实验室用石墨电极电解一定浓度的(NH4)2SO4与NaCl的酸性溶液来模拟。阳极的电极反应式___,处理1mol(NH4)2SO4,需要消耗HClO物质的量是___mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com