
����Ŀ�����������ڹ�ũҵ�������й㷺����;��
��1�����������Ʊ������ܶࡣ
���Ʊ�����һ��H2O2��Һ�������Ca(OH)2����Һ��Ӧ���Ʊ�CaO2��8H2O���仯ѧ����ʽΪ��_________��
���Ʊ������������÷�ӦCa(s)+O2 ![]() CaO2(s)���ڴ�����������ȡCaO2��ʵ����ģ��װ��ʾ��ͼ���£�
CaO2(s)���ڴ�����������ȡCaO2��ʵ����ģ��װ��ʾ��ͼ���£�
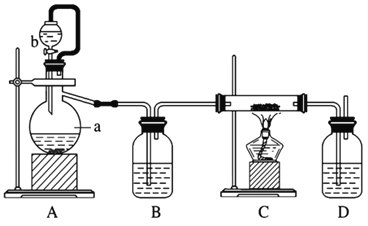
��ش��������⣺
װ��A�з�Ӧ�Ļ�ѧ����ʽΪ_________������a������Ϊ ________��װ��D��ʢ�е�Һ����Ũ���ᣬ������һ�ǹ۲����������٣��ж�����ͨ���Ƿ���켰������Ʒ�Ӧ���еij̶ȣ�����____________��
��2��ˮ��������(DO)�Ǻ���ˮ���������һ��ָ�꣬ͨ����ÿ��ˮ���ܽ������ӵ�������ʾ����λmg��L-1���ⶨԭ��Ϊ��
�ټ��������£�O2��Mn2+����ΪMnO(OH)2��2Mn2++O2+4OH-=2MnO(OH)2����
�����������£�MnO(OH)2��I-����ΪI2��MnO(OH)2+2I-+4H+=Mn2++I2+3H2O��
����Na2S2O2����Һ�ζ����ɵ�I2��2S2O32-+I2=S4O62-+2I-��
ˮ�������г���ˮ�м�һ����CaO2��8H2O����������ȡ��ˮ��100.0 mL�������������ⶨˮ��������������0.01000 mol/L Na2S2O2����Һ13.50 mL��
�ζ�������ʹ�õ�ָʾ����________����ˮ���е��ܽ�����(DO)Ϊ_________��
���𰸡� Ca(OH)2��H2O2��6 H2O ===CaO2��8H2O 2H2O2![]() 2H2O��O2��(��2Na2O2��2H2O===4NaOH��O2��) ������ƿ ��ֹ����CO2��ˮ��������װ��CӰ���Ʒ���� ������Һ 10.80 mg��L��1
2H2O��O2��(��2Na2O2��2H2O===4NaOH��O2��) ������ƿ ��ֹ����CO2��ˮ��������װ��CӰ���Ʒ���� ������Һ 10.80 mg��L��1
����������1����H2O2��Һ�������Ca(OH)2����Һ��Ӧ���Ʊ�CaO2��8H2O���仯ѧ����ʽΪCa(OH)2��H2O2��6 H2O ===CaO2��8H2O��
��������֪��AΪ��������װ�ã�������˫��ˮ�Ͷ���������ȡ������Ҳ�����ù���������ˮ��Ӧ��ȡ������BΪ����������װ����CΪ�Ʊ��������Ƶ�װ����D�DZ���װ������ֹ����CO2��ˮ��������װ��CӰ���Ʒ���ȡ����ԣ�װ��A�з�Ӧ�Ļ�ѧ����ʽΪ2H2O2![]() 2H2O��O2��(��2Na2O2��2H2O===4NaOH��O2��)������a������Ϊ������ƿ��װ��D��ʢ�е�Һ����Ũ���ᣬ������һ�ǹ۲����������٣��ж�����ͨ���Ƿ���켰������Ʒ�Ӧ���еij̶ȣ����Ƿ�ֹ����CO2��ˮ��������װ��CӰ���Ʒ���ȡ�
2H2O��O2��(��2Na2O2��2H2O===4NaOH��O2��)������a������Ϊ������ƿ��װ��D��ʢ�е�Һ����Ũ���ᣬ������һ�ǹ۲����������٣��ж�����ͨ���Ƿ���켰������Ʒ�Ӧ���еij̶ȣ����Ƿ�ֹ����CO2��ˮ��������װ��CӰ���Ʒ���ȡ�
��2��ˮ�������г���ˮ�м�һ����CaO2��8H2O����������ȡ��ˮ��100.0 mL���ⶨˮ��������������0.01000 mol/L Na2S2O2����Һ13.50 mL����Ϊ�������۱��������Եζ������п���ʹ�õ�����Һ��ָʾ�������ݷ�Ӧ���̷�����3����Ӧ�����Եõ���ϵʽO2~2MnO(OH)2~2 I2~4S2O32-������n(O2)= ![]() n(S2O32-)=
n(S2O32-)=![]() 13.50
13.50![]() 0.01000 mol/L=3..375
0.01000 mol/L=3..375![]() mol�����Ը�ˮ���е��ܽ�����(DO)Ϊ
mol�����Ը�ˮ���е��ܽ�����(DO)Ϊ![]() 10.80 mg��L��1��
10.80 mg��L��1��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����
A.��ұ��ʱ����������Ȼ�����ȡ������
B.���ʱ�����Ʋ�������Դ��������
C.���ε�س��ʱ��������ⷴӦ���ŵ�ʱ������ԭ��ط�Ӧ
D.����բ�������ֱ����Դ�ĸ����������ɷ�ֹ�䱻��ʴ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ܱ������У���Ӧ2X��g��+Y2��g��![]() 2XY��g������H��0���ﵽ��ƽ�⣮�ڽ��ı�ijһ�����ﵽ��ƽ�⣬���з�����ȷ����
2XY��g������H��0���ﵽ��ƽ�⣮�ڽ��ı�ijһ�����ﵽ��ƽ�⣬���з�����ȷ����

A. ͼI�У��ס��ҵ�ƽ�ⳣ���ֱ�ΪK1��K2����K1��K2
B. ͼ���У�ƽ��״̬��������ȣ�ƽ��״̬�ķ�Ӧ��ת���ʵ�
C. ͼ���У�tʱ����������ѹǿ
D. ͼ���Ƿ�Ӧ�ֱ��ڼס��������´ﵽƽ�⣬˵�����¶ȸ��ڼ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I���״���һ����Ҫ����ԭ�ϣ�����һ�ֿ�������Դ�����п�����Ӧ�õĹ���ǰ����
��1����֪��CH3OH(g)=HCHO(g)+H2(g) ��H=+84 kJ/mol 2H2(g)+O2(g)=2H2O(g) ��H=-484 kJ/mol����ҵ�ϳ��Լ״�Ϊԭ����ȡ��ȩ����д�� CH3OH (g)��O2 (g)��Ӧ����HCHO(g)��H2O(g)���Ȼ�ѧ����ʽ��_______________________��
��2���ɼ״���������NaOH��Һ���ɵ������ֻ���أ���ʹ�ֻ�����ʹ��һ���²ų�һ�ε硣�õ�ظ����ĵ缫��ӦʽΪ________________��
������2L�ܱ������У�800��ʱ��Ӧ2NO(g)+O2 (g)![]() 2NO2 (g)��ϵ�У�n(NO)��ʱ��ı仯�����
2NO2 (g)��ϵ�У�n(NO)��ʱ��ı仯�����
ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
��1����ͼ��ʾ����ʾNO2�仯���ߵ���_______����O2��ʾ��0��2 s�ڸ÷�Ӧ��ƽ������v=_______��
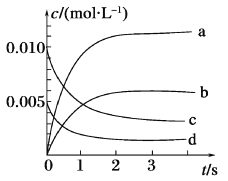
��2����˵���÷�Ӧ�Ѵﵽƽ��״̬����_______������ţ���
a��v(NO2) =2V(O2) b��������ѹǿ���ֲ���
c����ϵ��ɫ���ٸı� d���������ܶȱ��ֲ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��3NO2+H2O=2HNO3+NO�˷�Ӧ�������ͻ�ԭ������������
A. 2��1 B. 1��1 C. 1��2 D. ��ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2016���ҹ���ʵʩ�µġ����������������������д�ʩ�����ڸ��ƴ���������������������
�����о����˽�ҳ����ٳ����������� ���ƹ�ྻú���ü���
���Ż���Դ�ṹ�������Դ����Ч�ʣ� ����������¶�����
A.�ڢ�B.�ۢ�C.�٢�D.�٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��
A. Na��K��Cl��S��O B. Fe��Zn��Cu��B��Mn
C. N��H��O��P��C D. Ge��Ca��Cu��Mg��C
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС�������һ��ʵ����̽��Ԫ�������ɣ�
��ͬѧ����Ԫ�طǽ��������Ӧ��ۺ�����֮��Ĺ�ϵ���������ͼ1װ����һ�������N��C��Si���ַǽ���Ԫ�صķǽ�����ǿ���Ƚϵ�ʵ���о���
��ͬѧ�������ͼ2װ������֤±��Ԫ�����ʵĵݱ���ɣ�ͼ2�У�A��B��C�����ֱ���մ��NaBr��Һ������ʪ��ĵ���KI��ֽ��ʪ���ֽ����֪������Ũ�������������ܷ�Ӧ����������MnCl2�ȣ�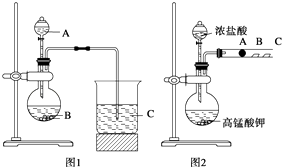
��1����ͬѧʵ����ѡ�õ����ʻ�ѧʽΪ��A �� B �� C��
��2��C����Ӧ�����ӷ���ʽΪ��
��3��д����ͬѧ��ʵ����Բ����ƿ�з�����Ӧ�Ļ�ѧ����ʽ��
��4��A����Ӧ�����ӷ���ʽΪ��
��5��B����ʵ������Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���ҳ���MnO2��Ũ���ᷴӦ���Ʊ�������MnO2+4HCl=MnCl2+2H2O+Cl2�����ڴ˷�Ӧ�У�
��1��������������
��2���������뻹ԭ�������ʵ���֮��Ϊ��
��3����˫���ŷ��������ת�Ƶķ������Ŀ����
��4����Ҫ����112mL��������ת�Ƶĵ�����Ŀ����
��5�����˷�Ӧ��д�����ӷ���ʽ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com