
对100mL 1mol·L-1的Na2CO3溶液,下列说法不正确的是
A.将溶液稀释,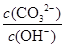 减少 减少 |
| B.滴人含0.l mol CH3COOH的溶液:c ( CH3 COO一)<c( HCO3一) |
| C.通人0.1 mo1CO2气体,溶液中存在:c ( Na+)=c( CO32一)十c( HCO3一)+c(H2CO3) |
| D.滴人酚酞,微热,溶液颜色加深 |
B
解析试题分析:A、碳酸钠溶液中CO32-水解,稀释促进水解,因此CO32-的物质的量减少和OH-的物质的量增加,所以将溶液稀释,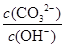 减少,A正确;B、滴人含0.l mol CH3COOH的溶液中二者反应恰好生成碳酸氢钠和醋酸钠,由于醋酸的酸性强于碳酸的,因此醋酸钠的水解程度小于碳酸氢钠的水解程度,所以溶液中c ( CH3 COO一)>c( HCO3一),B不正确;C、通人0.1 mo1CO2气体,二者恰好反应生成碳酸氢钠,根据物料守恒可知溶液中存在:c ( Na+)=c( CO32一)十c( HCO3一)+c(H2CO3),C正确;D、水解吸热,滴人酚酞,微热,促进水解,溶液碱性增强,因此溶液颜色加深,D正确,答案选B。
减少,A正确;B、滴人含0.l mol CH3COOH的溶液中二者反应恰好生成碳酸氢钠和醋酸钠,由于醋酸的酸性强于碳酸的,因此醋酸钠的水解程度小于碳酸氢钠的水解程度,所以溶液中c ( CH3 COO一)>c( HCO3一),B不正确;C、通人0.1 mo1CO2气体,二者恰好反应生成碳酸氢钠,根据物料守恒可知溶液中存在:c ( Na+)=c( CO32一)十c( HCO3一)+c(H2CO3),C正确;D、水解吸热,滴人酚酞,微热,促进水解,溶液碱性增强,因此溶液颜色加深,D正确,答案选B。
考点:考查盐类水解、溶液中离子浓度大小比较


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:单选题
常温下,向20 mL 0.2 mol/L H2A溶液中滴加0.2 mol/L NaOH溶液。有关微粒的物质的量变化如下图(其中I代表H2A,II代表HA-,III代表A2-)。根据下图图示判断,下列说法正确的是
| A.当V(NaOH)=20mL时,溶液中离子浓度大小关系:c(Na+)>c(HAˉ)>c(H+)>c(A2-)>c(OHˉ) |
| B.等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水的大 |
| C.欲使NaHA溶液呈中性,可以向其中加入酸或碱 |
| D.向NaHA溶液加入水的过程中,pH可能增大也可能减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是
| A.100℃时,KW =10-12,此温度下PH =6的溶液一定显酸性 |
| B.25℃时,0.1mol/L的NaHSO3溶液pH =4,说明HSO3-在水溶液中只存在电离 |
| C.NH4Cl、CH3COONa、NaHCO3、NaHSO4溶于水,对水的电离都有促进作用 |
| D.25℃时,10mL 0.1mol/L CH3COOH溶液与5mL 0.1mol/L NaOH溶液混合,所得溶液中有 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某温度下,已知醋酸的电离常数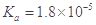 ,醋酸银的溶度积
,醋酸银的溶度积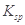 (CH3COOAg )=1.6×10
(CH3COOAg )=1.6×10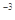 ,
,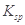 (Ag2CO3)="8.3"
(Ag2CO3)="8.3" 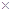 l0
l0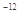 。在不考虑盐类水解的情况下,下列有关说法正确的是
。在不考虑盐类水解的情况下,下列有关说法正确的是
A.醋酸水溶液中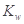 不变,故醋酸对水的电离无影响 不变,故醋酸对水的电离无影响 |
| B.该温度下饱和醋酸水溶液的pH =5-lgl.8 |
C.该温度下浓度均为0.01 mol 的CH3COONa溶液和AgNO3,溶液等体积混合(混合溶液体积具有加和性),有CH3COOAg沉淀生成 的CH3COONa溶液和AgNO3,溶液等体积混合(混合溶液体积具有加和性),有CH3COOAg沉淀生成 |
D.将0.02 mol 的Na2CO3,溶液与CH3COOAg沉淀上清液等体积混合,出现白色沉淀 的Na2CO3,溶液与CH3COOAg沉淀上清液等体积混合,出现白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实验数据如下表:
| 实验编号 | 起始浓度/(mol·L-1) | 反应后溶液的pH | |
| c(HA) | c(KOH) | ||
| ① | 0.1 | 0.1 | 9 |
| ② | x | 0.2 | 7 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关溶液中微粒的物质的量浓度关系正确的是
A.某弱酸的酸式盐NaHA溶液中一定有:c(OH-)+2c(A2-)=c(H+)+c(H2A)
B.0.1 mol·L-1CH3COONa 溶液与0.05 mol·L-1盐酸等体积混合后的酸性溶液中:c(CH3COO-)> c(CH3COOH) > c(Cl-) >c(H+)
C.物质的量浓度相等的HCN溶液和NaCN溶液等体积混合后的溶液中:c(CN-)+2c(OH-)=2c(H+)+c(HCN)
D.0.1 mol·L-1(NH4)2Fe(SO4)2溶液中:c(NH4+)+c(NH3·H2O)+c(Fe2+)=0.3 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
25℃时,0.1mol·L-1CH3COONa溶液pH=a,则
| A.该温度下,CH3COOH的Ka=1014-2a |
| B.该温度下,上述溶液中水的电离度α=(1.8×l0 a -14)% |
| C.升高温度,溶液中c(H+)增大,水解平衡常数K也增大 |
| D.加水稀释,CH3COONa水解程度增大,C(OH-)增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列各组关于强电解质、弱电解质、非电解质的归类,完全正确的是( )
| | A | B | C | D |
| 强电解质 | Fe | NaCl | CaCO3 | HNO3 |
| 弱电解质 | CH3COOH | NH3 | H3PO4 | Fe(OH)3 |
| 非电解质 | C12H22O11(蔗糖) | BaSO4 | C2H5OH | H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列应用与盐类的水解无关的是( )
| A.纯碱溶液可去除油污 |
| B.NaCl可用作防腐剂和调味剂 |
| C.TiCl4溶于大量水加热制备TiO2 |
| D.FeCl3饱和溶液滴入沸水中制Fe(OH)3胶体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com