
【题目】A、B、C、W均为中学常见的纯净物,它们之间有如下转化关系(其他产物及反应条件已略去,反应可以在水溶液中进行):![]() 。三种物质的焰色反应均为黄色;C常作面包和糕点的发泡剂,受热分解可生成B。
。三种物质的焰色反应均为黄色;C常作面包和糕点的发泡剂,受热分解可生成B。
(1)写出下列物质的化学式A______,B________,C________,W________。
(2)写出A溶液与C溶液反应的离子方程式为_______________________________。
(3)向两份30 mL同浓度的A溶液中通入不同体积的W气体,得到溶液M、N。向M、N溶液中逐滴加入浓度为0.25 mol·L-1盐酸,如图所示Ⅰ和Ⅱ分别为加入V(盐酸)与产生V(W)的关系。通过计算确定A溶液的物质的量浓度为 _______________。
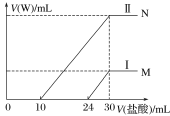
(4)M、N两溶液中相同溶质的物质的量之比为多少_______?(写出必要的文字说明和计算过程)
【答案】NaOH Na2CO3 NaHCO3 CO2 OH-+HCO3-===CO32-+H2O 0.25 mol·L-1 3:5
【解析】
(1).C常作面包和糕点的发泡剂,受热分解可生成B,则C是NaHCO3、B是Na2CO3。碳酸钠溶液与二氧化碳反应生成碳酸氢钠,所以W是二氧化碳气体;NaOH与二氧化碳反应生成碳酸钠,所以A是氢氧化钠。(2)氢氧化钠溶液与碳酸氢钠溶液反应生成碳酸钠和水;(3)加入30ml盐酸时二氧化碳的体积达最大,此时溶液为氯化钠溶液,根据氯离子、钠离子守恒,计算出氢氧化钠的物质的量,再根据物质的量浓度的定义计算;(4)碳酸钠溶液中逐滴滴入盐酸,依次发生反应:Na2CO3+HCl=NaHCO3+NaCl,NaHCO3+HCl=NaCl+CO2↑+H2O,结合图象分析各段发生反应,据此判断溶质的成分及物质的量。
(1)C常作面包和糕点的发泡剂,受热分解可生成B,则C是NaHCO3、B是Na2CO3。碳酸钠溶液与二氧化碳反应生成碳酸氢钠,所以W是二氧化碳气体;NaOH与二氧化碳反应生成碳酸钠,所以A是氢氧化钠。(1)根据以上分析,A是NaOH,B是Na2CO3,C是NaHCO3,W是CO2;
(2)氢氧化钠溶液与碳酸氢钠溶液反应生成碳酸钠和水,反应的离子方程式为OH-+HCO3-=CO32-+H2O;
(3)加入30mL盐酸时,气体恰好完全放出,溶液中的溶质只有氯化钠,根据氯离子、钠离子守恒,n(NaOH)=n(HCl),![]() ,
,![]() ;所以氢氧化钠溶液的物质的量浓度为0.25 mol·L-1;
;所以氢氧化钠溶液的物质的量浓度为0.25 mol·L-1;
(4)碳酸钠溶液中逐滴滴入盐酸,依次发生反应:Na2CO3+HCl=NaHCO3+NaCl,NaHCO3+HCl=NaCl+CO2↑+H2O。依据M可知,24-30段为碳酸氢钠与盐酸反应,则溶液中碳酸钠消耗的盐酸体积为30mL-24mL=6mL,说明溶质为碳酸钠与氢氧化钠混合物,依据方程式:Na2CO3+HCl=NaHCO3+NaCl,碳酸钠的物质的量为:0.006L×0.25molL-1=0.0015mol;依据N可知,10-30段为碳酸氢钠与盐酸反应,若溶质为碳酸钠则溶液中碳酸钠消耗的盐酸体积为30 mL -10 mL =20mL,而B中0-10mL<20mL,说明B中溶质为碳酸钠和碳酸氢钠,0-10mL盐酸为碳酸钠与盐酸反应生成碳酸氢钠,依据Na2CO3+HCl=NaHCO3+NaCl,碳酸钠的物质的量为:0.010L×0.25molL-1=0.0025mol;所以M、N两溶液中相同组分溶质的物质的量之比为:0.0015mol:0.0025mol=3:5。


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
Ⅰ.(1)将NaHSO4溶液滴入到Ba(OH)2溶液中至中性的离子方程式:_______
(2)将5-6滴饱和氯化铁溶液滴入到25mL沸水中,继续加热,得红褐色液体。写出反应的离子方程式:______________
(3)在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色。又变为棕黄色的原因是____________(用离子方程式表示)。
(4)向Na2S2O3 中加入稀硫酸反应的离子方程式______________。
Ⅱ.金属铬(Cr)的英文是Chromium,原意是颜色,因为它的化合物都有美丽的颜色。如表是几种常见铬的化合物或离子的水溶液的颜色:
离子或化合物 | Cr2O | Cr(OH)3 | Cr3+ | CrO2- | CrO |
颜色 | 橙色 | 灰蓝色 | 蓝紫色 | 绿色 | 黄色 |
含铬元素的化合物可以发生如图一系列变化:
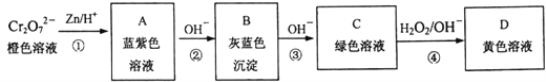
①写出反应④的离子方程式:___________________。
②结合上述转化图及所学知识,请分析向NaCrO2溶液中逐滴加入过量稀硫酸的现象为_______。
Ⅲ.二氧化硫是常见大气污染气体,二氧化硫尾气处理的方法之一是采用钠一钙联合处理法。
第一步:用NaOH溶液吸收SO2:2NaOH+SO2=Na2SO3+H2O
第二步:将所得的Na2SO3溶液与生石灰反应Na2SO3+CaO+H2O=CaSO3↓+2NaOH
若在第一步吸收SO2后得到的NaOH和Na2SO3混合溶液中,加入少许溴水,振荡后溶液变为无色,生成Na2SO4和NaBr。写出发生反应的离子方程式____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生物降解高分子材料F的合成路线如下,已知C是密度为1.16 g·L-1的烃。
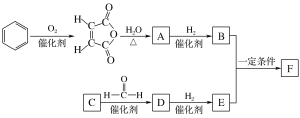
已知:
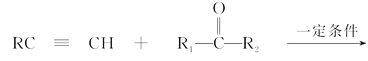
(1)下列说法正确的是________。
A.A能使酸性KMnO4溶液或溴的CCl4溶液褪色
B.等物质的量的B和乙烷,完全燃烧,消耗的氧气相同
C.E能和Na反应,也能和Na2CO3反应
D.B和E反应,可以生成高分子化合物,也可以形成环状物
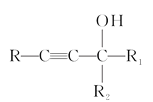
(2)C中含有的官能团名称是________。
(3)由B和E合成F的化学方程式是____________________________________。
(4)完成由CH2=CH2、HCHO合成H3COOCCH2CH2COOCH3合成路线_____________(用流程图表示,无机试剂任选)。
(5) 的同分异构体中,分子中含1个四元碳环,但不含—O—O—键。结构简式是________。
的同分异构体中,分子中含1个四元碳环,但不含—O—O—键。结构简式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应CO(g)+H2O(g) ![]() CO2(g)+H2(g) ΔH<0。在一定温度和压强下于密闭容器中,反应达到平衡。下列叙述正确的是( )
CO2(g)+H2(g) ΔH<0。在一定温度和压强下于密闭容器中,反应达到平衡。下列叙述正确的是( )
A.升高温度,K增大
B.减小压强,n(CO2)增加
C.更换高效催化剂,α(CO)增大
D.充入一定量的氮气,n(H2)不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置正确且能达到实验目的的是![]()
A.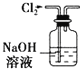 用如图所示装置除去Cl2中含有的少量HCl
用如图所示装置除去Cl2中含有的少量HCl
B.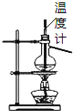 如图所示为石油分馏
如图所示为石油分馏
C.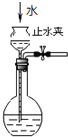 如图所示为检查装置气密性
如图所示为检查装置气密性
D.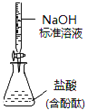 如图所示为测定未知盐酸的浓度
如图所示为测定未知盐酸的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列有关叙述正确的是 ( )
A.100 g 98%的浓硫酸中含有的氢原子数目为2NA
B.16g16O2和18O3的混合物中含有的质子数目为8NA
C.电解精炼铜的过程中,若阳极减重64g,则电路中一定通过2NA个电子
D.取50mL14.0mol/L浓硝酸与足量的铜片反应,生成气体分子的数目可能为0.25NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】咖啡鞣酸具有较广泛的抗菌作用,其结构简式如下图所示:

关于咖啡鞣酸的下列叙述正确的是( )
A.分子式为C16H13O9
B.1 mol咖啡鞣酸可与含8 mol NaOH的溶液反应
C.能使酸性KMnO4溶液褪色,说明分子结构中含有碳碳双键
D.与浓溴水能发生两种类型的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产生活有密切的联系。下列关于化学物质应用的说法错误的是![]()
A.84消毒液和洁厕灵不能混合使用
B.![]() 可作葡萄酒的防腐剂
可作葡萄酒的防腐剂
C.醋酸可用于除水垢是由于碳酸的酸性比醋酸强
D.![]() 过硫酸氢钾
过硫酸氢钾![]() 可用于游泳的杀菌消毒是由于它能使蛋白质变性
可用于游泳的杀菌消毒是由于它能使蛋白质变性![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下微粒含配位键的是( )
①N2H5+ ②CH4 ③OH- ④NH4+ ⑤Fe(CO)5 ⑥Fe(SCN)3 ⑦H3O+ ⑧[Ag(NH3)2]OH
A. ①②④⑦⑧B. ③④⑤⑥⑦
C. ①④⑤⑥⑦⑧D. 全部
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com