
【题目】有关如图所示化合物的说法不正确的是

A. 该有机物的分子式为C15H18O4
B. 1 mol该化合物最多可以与2 mol NaOH反应
C. 既可以催化加氢,又可以使酸性KMnO4溶液褪色
D. 既可与FeCl3溶液发生显色反应,又可与NaHCO3溶液反应放出CO2气体
 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:
【题目】下列各组物质间的反应既属于氧化还原反应,又属于离子反应的是( )
A. NaCl溶液与AgNO3溶液 B. Zn与稀H2SO4
C. H2与O2 D. Na2O与H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照① ⑥在表中的位置,用化学用语回答下列问题。

(1)元素①的原子结构示意图为_____
(2)元素②、③形成离子的半径_____>_____。
(3)元素⑤、⑥形成的气态氢化物稳定性__________>___________。
(4)元素④的最高价氧化物的水化物与元素③的最高价氧化物的水化物稀溶液反应的离子方程式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修3:物质结构与性质]
锌在工业中有重要作用,也是人体必需的微量元素。回答下列问题:
(1)Zn原子核外电子排布式为________________。
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能Ⅰ1(Zn)_______Ⅰ1(Cu)(填“大于”或“小于”)。原因是________________。
(3)ZnF2具有较高的熔点(872 ℃),其化学键类型是_________;ZnF2不溶于有机溶剂而ZnCl2、ZnBr2、ZnI2能够溶于乙醇、乙醚等有机溶剂,原因是________________。
(4)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为________________,C原子的杂化形式为________________。
(5)金属Zn晶体中的原子堆积方式如图所示,这种堆积方式称为_______________。六棱柱底边边长为a cm,高为c cm,阿伏加德罗常数的值为NA,Zn的密度为________________g·cm-3(列出计算式)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W均为短周期主族元素,X、Y、Z原子的最外层电子数之和为10。X与Z同族,Y最外层电子数等于X次外层电子数,且Y原子半径大于Z。W的最外层电子数等于X的核外电子总数,且W单质常温下为固体。请回答下列问题:
(1)Z在周期表中的位置为______________。
(2)Y元素形成的离子的结构示意图为____________。
(3)X、Y、Z三种元素对应的原子半径大小关系为____________(填元素符号)。
(4)X和Z形成的简单氢化物,热稳定性较好的是______________(填化学式)。
(5)Y与X的最高价氧化物在一定条件下反应的实验现象是___________________________。
(6)下列说法正确的是_______。
A.W的氧化物,均满足8e—稳定结构
B.最高价氧化物对应的水化物的酸性W>Z
C.由于Z的氧化物ZO2既可与酸反应,又能与碱反应,所以ZO2为两性氧化物
D.W的氧化物WO2,具有还原性,能使酸性KMnO4溶液褪色
(7)足量的单质Y与一定量的W的最高价氧化物对应的水化物的浓溶液,在一定条件下充分反应,所得气体的成分为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羟基扁桃酸是药物合成的重要中间体,它可由苯酚和乙醛酸反应制得:
![]() +
+![]() →
→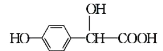
(乙醛酸) (羟基扁桃酸)
下列有关说法正确的是
A. 该反应是取代反应
B. ![]() 和羟基扁桃酸互为同系物
和羟基扁桃酸互为同系物
C. 1个羟基扁桃酸分子中最多有17个原子共平面
D. 1 mol羟基扁桃酸分子最多能分别和1 mol NaHCO3、2 mol NaOH、3 mol Na、4 mol H2发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2CO3和NaHCO3可作食用碱。下列方程式中正确的是( )
A.Na2O2与CO2反应生成Na2CO3:Na2O2 +CO2=Na2CO3+O2
B.Na2CO3溶液呈碱性:CO32-+H2O![]() H2CO3+2OH-
H2CO3+2OH-
C.NaHCO3可作发酵粉:2NaHCO3![]() Na2CO3+CO2↑ +H2O
Na2CO3+CO2↑ +H2O
D.Na2CO3溶液除去CH3COOC2H5中的CH3COOH:CO32-+2H+=CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计了由乙醇合成乙二醇的路线如下。下列说法正确的是
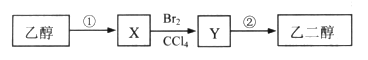
A. X可以发生加成反应
B. 步骤①的反应类型是水解反应
C. 步骤②需要在氢氧化钠醇溶液中反应
D. 等物质的量的乙醇、X完全燃烧,消耗氧气的量不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列8种化学符号:![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]()
①表示核素的符号共________种。
②质量数相等,但不能互称同位素的是________和________。
(2)为验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如图实验,请回答:
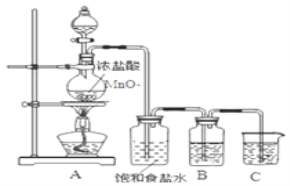
①装置B中盛放的试剂是____________(填选项),实验现象为____________。
A.Na2S溶液 B.Na2SO3溶液 C.Na2SO4溶液
②能证明氯元素比硫元素非金属性强的依据为____________。(填序号)
A.盐酸为强酸,氢硫酸为弱酸 B.次氯酸的氧化性比稀硫酸强
C.S2-比Cl-还原性强 D.HCl比H2S稳定
(3)在2L的密闭容器中放入4molN2O5,发生如下反应:2N2O5(g)![]() 4NO2(g)+O2(g)。反应至5min时,测得N2O5转化了20%,则v(NO2)为_________;5min时,N2O5在混合气体中的体积分数是____________。
4NO2(g)+O2(g)。反应至5min时,测得N2O5转化了20%,则v(NO2)为_________;5min时,N2O5在混合气体中的体积分数是____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com