
【题目】用NA表示阿伏加德罗常数的值,下列叙述中不正确的是( )
A.分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA
B.28 g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA
C.常温常压下,92g 的NO2和N2O4混合气体含有的原子数为6NA
D.常温常压下,22.4 L 氯气与足量的镁粉充分反应,转移的电子数为2NA
 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
【题目】在酸性介质中,往MnSO4溶液里滴加(NH4)2S2O8(过二硫酸铵)溶液会发生如下反应:Mn2++S2O82﹣+H2O→MnO4﹣+SO42﹣+H+ , 下列说法不正确的是( )
A.可以利用该反应检验Mn2+
B.氧气性比较:S2O82﹣>MnO4﹣
C.该反应中酸性介质可以为盐酸
D.若有0.1mol氧化产物生成,则转移电子0.5mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( ) ①NaHCO3溶液加水稀释,c(Na+)/c(HCO3﹣)的值保持增大
②浓度均为0.1molL﹣1的Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c(CO32﹣)+c(HCO3﹣)]
③在0.1molL﹣1氨水中滴加0.lmolL﹣1盐酸,恰好完全反应时溶液的pH=a,则由水电离产生的c(OH﹣)=l0﹣amolL﹣1
④向0.1molL﹣1(NH4)2SO3溶液中加入少量NaOH固体,c(Na+)、c(NH4+)、c(SO32﹣)均增大
⑤在Na2S稀溶液中,c(OH﹣)=c(H+)+2c(H2S)+c(HS﹣)
A.①④
B.②④
C.①③
D.②⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯化铁是中学化学实验室中常用的化学试剂.同学们利用废铁屑(含少量铜杂质)来探究制备FeCl36H2O的方法,同学甲设计的实验装置如图所示,其实验步骤如下:A中放有废铁屑,烧杯中盛有足量的稀硝酸,实验时先打开a并关闭b,用分液漏斗向A中加入过量的盐酸充分反应,此时溶液呈浅绿色;再打开b进行过滤,过滤结束后,取烧杯内溶液倒入蒸发皿加热,蒸发掉部分水并使剩余HNO3分解,再降温结晶得FeCl36H2O晶体. 填写下列空白:
(1)滴加盐酸时,发现反应速率较之盐酸与纯铁粉反应要快,其原因是 .
(2)烧杯内放过量稀HNO3的原因是(用离子方程式表示).
(3)整个实验过程中,弹簧夹a都必须打开,除为排出产生的气体外,另一个目的是 .
(4)乙同学对该实验进行了改进,他是用空烧杯盛接滤液,加入适当的试剂,然后在HC1的气流中、一定温度下蒸发、浓缩、降温结晶而得到纯净的FeCl36H2O,你认为加入的试剂可以是 . (填序号) ①适量氯气 ②适量过氧化氢和稀盐酸
③酸性高锰酸钾溶液 ④氢氧化钠溶液.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回收铅蓄电池的电极填充物(铅膏,主要含PbO、PbO2、PbSO4),可制备热稳定剂三盐基硫酸铅(组成可表示为3PbOPbSO4H2O),其实验流程如下: 
(1)物质X可以循环利用,该物质是 . 最后一次过滤之后需要洗涤,检验三盐基硫酸铅是否洗净的方法是 .
(2)从滤液A可提取出一种含结晶水的钠盐副产品.若检验该晶体中结晶水的含量,所需的硅酸盐材质仪器有、、、玻璃棒、石棉网、干燥器等.
(3)流程中不直接利用H2SO4溶液与PbO、PbCO3反应制取PbSO4 , 原因可能是 .
(4)生成三盐基硫酸铅的离子反应方程式为 .
(5)向铅膏浆液中加入Na2SO4溶液的目的是将其中的PbO2还原为PbO.若实验中所取铅膏的质量为47.8g,其中PbO2的质量分数为15.0%,则要将PbO2全部还原,至少需加mL 1.0molL﹣lNa2SO3溶液.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】晶体硅是信息科学和能源科学中的一种重要材料,可用于制芯片和太阳能电池等.以下是工业上制取纯硅的一种方法. 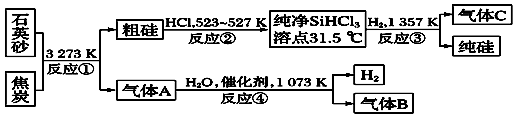
请回答下列问题(各元素用相应的元素符号表示):
(1)在上述生产过程中,属于置换反应的有(填反应代号).
(2)写出反应③的化学方程式 .
(3)化合物W的用途很广,通常可用作建筑工业和造纸工业的黏合剂,可作肥皂的填充剂,是天然水的软化剂.将石英砂和纯碱按一定比例混合加热至1 373~1 623K反应,生成化合物W,其化学方程式是
(4)A、B、C三种气体在“节能减排”中作为减排目标的一种气体是(填化学式);分别通入W溶液中能得到白色沉淀的气体是(填化学式).
(5)工业上合成氨的原料H2的制法是先把焦炭与水蒸气反应生成水煤气,再提纯水煤气得到纯净的H2 , 提纯水煤气得到纯净的H2的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝镁合金是制造飞机的重要材料。为测定己除去表面氧化膜的某铝镁合金(假设不含共他元素)镁的质量分数,学习小组同学设计了如下两种实验方案。
(1)[方案1]准确称最ag铝镁合金样品与足量NaOH溶液反应,经过滤、洗涤、干燥后,称量剩余固体的质量。该样品与NaOH溶液反应的化学方程式是。若剩余固体质量为bg,则铝镁合金中镁的质量分数是(列出计算式即可)。若未洗涤过滤后的滤渣,则最终测量结果是。( 填“偏低、偏高、不影响” )。
[方案2]将铝镁合金与足量稀硫酸溶液反应,测定生成气体的体积。
(2)同学们选用甲装置进行实验:实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开其活塞,一会儿后稀硫酸就不能顺利滴入锥形瓶。请你帮助分析原因是。
(3)同学们经讨论认为甲装置有两个方面会引起较大误差,分别是和。
(4)于是他们设计了实验装置乙。乙中导管a的作用是。若实验前后滴定管中液面读数分别为V1mL、V2mL。则产生氢气的体积为mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列四种溶液:①pH=0的盐酸,②0.1molL﹣1的盐酸,③0.01molL﹣1的NaOH溶液,④pH=11的NaOH溶液中,由水电离生成的H+的物质的量浓度之比为( )
A.1:10:100:1000
B.0:1:12:11
C.14:13:12:11
D.14:13:2:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com