
 O2+HbCO,实验表明,c(HbCO)即使只有c(HbO2)的
O2+HbCO,实验表明,c(HbCO)即使只有c(HbO2)的 ,也可造成人的智力损伤。已知t ℃时上述反应的平衡常数K=200,吸入肺部O2的浓度约为1.0×10-2 mol·L-1,若使c(HbCO)小于c(HbO2)的
,也可造成人的智力损伤。已知t ℃时上述反应的平衡常数K=200,吸入肺部O2的浓度约为1.0×10-2 mol·L-1,若使c(HbCO)小于c(HbO2)的 ,则吸入肺部CO的浓度不能超过______mol·L-1。
,则吸入肺部CO的浓度不能超过______mol·L-1。 FeO(s)+CO(g) ΔH=Q1,平衡常数K1
FeO(s)+CO(g) ΔH=Q1,平衡常数K1 FeO(s)+H2(g) ΔH=Q2,平衡常数为K2
FeO(s)+H2(g) ΔH=Q2,平衡常数为K2 CO(g)+H2O(g) ΔH=Q3,平衡常数为K3
CO(g)+H2O(g) ΔH=Q3,平衡常数为K3| T/℃ | K1 | K2 | K3 |
| 700 | 1.47 | 2.38 | 0.62 |
| 900 | 2.15 | 1.67 | |
 CO(g)+H2O(g)为________(填“放”或“吸”)热反应,Q3________0(填“>”、“<”或“=”)。③改变条件使可逆反应H2(g)+CO2(g)
CO(g)+H2O(g)为________(填“放”或“吸”)热反应,Q3________0(填“>”、“<”或“=”)。③改变条件使可逆反应H2(g)+CO2(g) CO(g)+H2O(g)已经建立的平衡逆向移动,可采取的措施有________。
CO(g)+H2O(g)已经建立的平衡逆向移动,可采取的措施有________。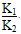 1.29 吸 > ③BD (3)7或9
1.29 吸 > ③BD (3)7或9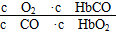 =
=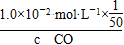 =200,所以c(CO)=1.0×10-2 moL·L-1×
=200,所以c(CO)=1.0×10-2 moL·L-1× ×
×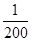 =1.0×10-6 mol·L-1。(2)①第一个热化学方程式减去第二个热化学方程式等于第三个热化学方程式,故Q3=Q1-Q2;②
=1.0×10-6 mol·L-1。(2)①第一个热化学方程式减去第二个热化学方程式等于第三个热化学方程式,故Q3=Q1-Q2;②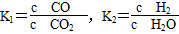 ,K3=
,K3= ,故K3=
,故K3=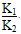 ,当T=900 ℃时,K3=
,当T=900 ℃时,K3=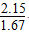 ≈1.29;温度越高,平衡常数越大,说明升高温度导致平衡正向移动,故该反应为吸热反应,即Q3>0。③该反应为反应前后气体分子数不变的反应,故改变容器体积不会使平衡移动,A项错误;因为该反应为吸热反应,降低温度可以使平衡逆向移动,B项正确、E项错误;使用催化剂不能使平衡移动,C项错误;增加生成物的浓度,可以使平衡逆向移动,D项正确。(3)CO2与过氧化钠反应的化学方程式为2CO2+2Na2O2=2Na2CO3+O2,由化学方程式可知当有88 g CO2参加反应时,固体增重为88 g-32 g=56 g,由实际增重7 g可知m(CO2)=7 g×88 g÷56 g=11 g,n(CO2)=
≈1.29;温度越高,平衡常数越大,说明升高温度导致平衡正向移动,故该反应为吸热反应,即Q3>0。③该反应为反应前后气体分子数不变的反应,故改变容器体积不会使平衡移动,A项错误;因为该反应为吸热反应,降低温度可以使平衡逆向移动,B项正确、E项错误;使用催化剂不能使平衡移动,C项错误;增加生成物的浓度,可以使平衡逆向移动,D项正确。(3)CO2与过氧化钠反应的化学方程式为2CO2+2Na2O2=2Na2CO3+O2,由化学方程式可知当有88 g CO2参加反应时,固体增重为88 g-32 g=56 g,由实际增重7 g可知m(CO2)=7 g×88 g÷56 g=11 g,n(CO2)=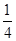 mol。若CO与氧气反应,CO不足,则n(CO)=n(CO2)=
mol。若CO与氧气反应,CO不足,则n(CO)=n(CO2)=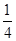 mol,m(CO)=
mol,m(CO)=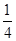 mol×28 g·mol-1=7 g。若CO与氧气反应,CO过量,则n(O2)=
mol×28 g·mol-1=7 g。若CO与氧气反应,CO过量,则n(O2)=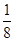 mol,故m(CO)=13 g-
mol,故m(CO)=13 g-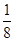 mol×32 g·mol-1=9 g。
mol×32 g·mol-1=9 g。

科目:高中化学 来源:不详 题型:填空题
 HOI(aq) △H2
HOI(aq) △H2 I2(aq) + H2O(l) △H3
I2(aq) + H2O(l) △H3 I3-(aq),其平衡常数表达式为_______.
I3-(aq),其平衡常数表达式为_______.


| A.c(H+)减小 | B.c(I-)减小 | C.I2(g)不断生成 | D.c(Fe3+)增加 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 它所对应的化学反应为:__ ___
它所对应的化学反应为:__ ___| 容器 | 容积/L | 温度/℃ | 起始量/mol | 平衡量/mol[ | 达到平衡所需时间/min | |
| C(s) | H2O(g) | H2(g) | ||||
| 甲 | 2 | T1 | 2 | 4 | 3.2 | 8 |
| 乙 | 1 | T2 | 1 | 2 | 1,2 | 3 |
 CH3OCH3(g)+ 3H2O(g)
CH3OCH3(g)+ 3H2O(g)| 投料比[n(H2)/ n(CO2)] | 500 K | 600 K | 700 K | 800 K |
| 1.5 | 45% | 33% | 20% | 12% |
| 2.0 | 60% | 43% | 28% | 15% |
| 3.0 | 83% | 62% | 37% | 22% |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CO(g)+H2(g);②C(s)、CO(g)和H2(g)完全燃烧的热化学方程式分别为:
CO(g)+H2(g);②C(s)、CO(g)和H2(g)完全燃烧的热化学方程式分别为:
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 、
、 , NO2中氮氧键的键能为466 kJ·mol-1,N2O4中N-N键键能为167 kJ·mol-1,氮氧键的键能为438.5 kJ·mol-1,写出N2O4转化为NO2的热化学方程式 ;
, NO2中氮氧键的键能为466 kJ·mol-1,N2O4中N-N键键能为167 kJ·mol-1,氮氧键的键能为438.5 kJ·mol-1,写出N2O4转化为NO2的热化学方程式 ;  NiO(OH)+MH
NiO(OH)+MH查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 Fe3+(aq)+3OH-(aq) ; ΔH=" a" kJ?mol-1
Fe3+(aq)+3OH-(aq) ; ΔH=" a" kJ?mol-1 H+(aq)+OH-(aq) ;ΔH=" b" kJ?mol-1
H+(aq)+OH-(aq) ;ΔH=" b" kJ?mol-1查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。
2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。


 N2(g)+CO2(g)+2H2O(g) ΔH1="-867" kJ/mol
N2(g)+CO2(g)+2H2O(g) ΔH1="-867" kJ/mol N2O4(g) ΔH2="-56.9" kJ/mol
N2O4(g) ΔH2="-56.9" kJ/mol
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

| 实验编号 | T(℃) | n(N2)/n(H2) | p(MPa) |
| ⅰ | 450 | 1/3 | 1 |
| ⅱ | | | 10 |
| ⅲ | 480 | | 10 |
 2NH3(g)的特点,在给出的坐标图2中,画出其在1 MPa和10 MPa条件下H2的转化率随温度变化的趋势曲线示意图,并标明各条曲线的压强。
2NH3(g)的特点,在给出的坐标图2中,画出其在1 MPa和10 MPa条件下H2的转化率随温度变化的趋势曲线示意图,并标明各条曲线的压强。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com