
【题目】图I 是NO2(g) +CO(g)![]() CO2(g)+NO(g)反应过程中能量变化的示意图。一定条件下,在固定容积的密闭容器中该反应达到平衡状态。当改变其中一个条件X, Y随X的变化关系曲线如图II所示。
CO2(g)+NO(g)反应过程中能量变化的示意图。一定条件下,在固定容积的密闭容器中该反应达到平衡状态。当改变其中一个条件X, Y随X的变化关系曲线如图II所示。

下列有关说法正确的是( )
A.一定条件下,向密闭容器中加入1molNO2(g)与1molCO(g)反应放出234kJ热量
B.若X表示CO的起始浓度,则Y表示的可能是NO2的转化率
C.若X表示反应时间,则Y表示的可能是混合气体的密度
D.若X表示温度,则Y表示的可能是CO2的物质的量浓度
【答案】D
【解析】
试题分析:A.由于反应物的能量高于生成物,所以该反应是放热反应,该反应的焓变△H=-234kJ/mol,但反应是可逆反应,.一定条件下,向密闭容器中加入1molNO2(g)与1molCO(g)反应放出的热量小于234kJ,A错误;B.若X表示CO的起始浓度,则在其它条件不变时,CO的起始浓度越高, NO2的转化率就越高,不符合图像,B错误;C.若X表示反应时间,由于该反应的物质都是气体,容器的容积不变,所以气体的密度不变,C错误;D.根据图示可知该反应是放热反应,若X表示温度,升高温度,平衡向吸热的逆反应方向移动,所以随着温度的升高,c(CO2)逐渐减小,故Y表示的可能是CO2的物质的量浓度,D正确。答案选D。


科目:高中化学 来源: 题型:
【题目】CuSO4溶液与K2C2O4溶液棍合反应,产物之一是某种只含一种阴离子的蓝色钾盐水合物。通过下述实验确定该晶体的组成。
步骤a:称取0.6720 g样品,放入锥形瓶,加入适量2 mol·L-1稀硫酸,微热使样品溶解。再加入30 ml水加热,用0.2000 mol·L-1 KMnO4溶液滴定至终点,消耗8.00 mlKMnO4溶液。
步骤b:接着将溶液充分加热,使淡紫红色消失,溶液最终呈现蓝色。冷却后,调节pH并加入过量的KI固体,溶液变为棕色并产生白色沉淀CuI。用0.2500 mol·L-1 Na2S2O3标准溶液滴定至终点,消耗8.00 ml Na2S2O3溶液。已知涉及的部分反应的离子方程式为:
I2+2S2O32-=2I+S4O62-
(1)已知室温下CuI的Ksp=1.27×10-12,欲使溶液中c(Cu )≤1.0×10-6 mol·L-1,应保持溶液中c(I-)≥ mol·L-1。
(2)MnO4-在酸性条件下,加热能分解为O2,同时生成Mn2+。写出该反应的离子方程式为 若无此加热操作,则测定的Cu2+的含量将会 (填“偏高”、“偏低”或“不变”)。
(3)步骤b中第一步反应的方程式为 ,若用淀粉溶液做指示剂,则滴定终点观察到的现象为 。
(4)通过计算确定样品晶体的组成。(请写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学在生活中有着广泛的应用,下列对应关系错误的是( )
化学性质 | 实际应用 | |
A. | Al2(SO4)3和小苏打反应 | 泡沫灭火器灭火 |
B. | 铁比铜金属性强 | FeCl3腐蚀Cu刻制印刷电路板 |
C. | 次氯酸盐具有氧化性 | 漂白粉漂白织物 |
D. | HF与SiO2反应 | 氢氟酸在玻璃器皿上刻蚀标记 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在100℃时,将0.40mol二氧化氮气体充入2L密闭容器中,每隔一段时间对该容器内的得到数据如下
时间(s) | 0 | 20 | 40 | 60 | 80 |
n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
下列说法中正确的是
A.反应开始20s内以二氧化氮表示的平均反应速率为0.00125mol·L-1·s-
B.80s时混合气体的颜色与60s时相同,比40s时的颜色深
C.80s时向容器中加入0.32mol氦气,同时将容器扩大为4L,则平衡将不移动
D.若起始投料为0.20molN2O4,相同条件下达平衡,则各组分含量与原平衡体系对应相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年12月,中共中央、国务院印发了《关于全面推行河长制的意见》,进一步加强水污染治理工作。下列做法不应该提倡的是( )
A.用碱性废水中和处理酸性废水
B.将工业废液排入海洋以减少河道污染
C.生活污水无害化处理后用于绿化灌溉
D.推广使用高效、低毒农药,减轻水体污染
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物G是一种“β-兴奋剂”,其合成路线如下:
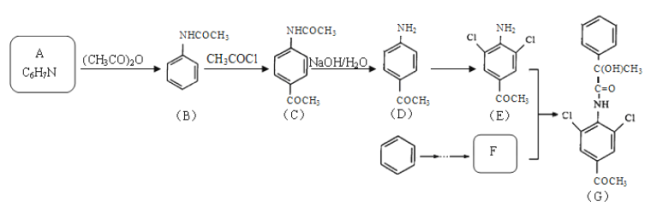
已知:
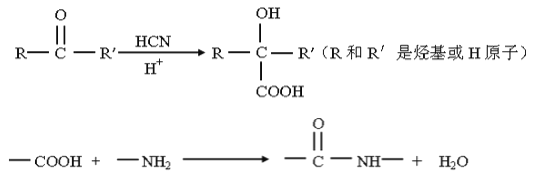
(1)写出化合物E同时符合下列条件的所有同分异构体有 种。
①红外光谱显示含有三种官能团,其中无氧官能团与E相同,不含甲基
②1H-NMR谱显示分子中含有苯环,且苯环上只有一种不同化学环境的氢原子。
③苯环上只有4个取代基,能发生银镜反应
(2)下列说法不正确的是
A.化合物B生成C的反应为取代反应
B.1mol化合物D最多与4molH2发生加成反应
C.化合物D生成E的条件为浓氯水/铁屑
D.化合物G的分子式为C17H14Cl2NO3
(3)写出E+F→G的化学方程式 。
(4)根据题中信息,设计以苯和CH3COCl为原料制备F的合成路线(用流程图表示,其他无机试剂任选)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活、科技、环境等密切相关,下列说法正确的是( )
A.用加酶洗衣粉洗衣服时水的温度越高越好
B.用CO2合成聚碳酸酯可降解塑料能实现“碳”的循环
C.用纳米铁粉的吸附性去除污水中的Cu2+、Hg2+等重金属离子
D.用高锰酸钾溶液、酒精、双氧水的强氧化性进行杀菌消毒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)常温下0.1moL/L 盐酸和0.06mol/L氢氧化钡溶液以等体积混合后pH=______
(2)常温下pH=9的Ba(OH)2溶液与pH=12的KOH溶液,按4:1的体积比混合,则混合溶液的pH=_______(己知lg2=0.3,lg5=0.7)
(3)如图所示,向A中充入 1mol X和1mol Y,向B中充入 2mol X和2mol Y, 起始时VA=VB=a L。在相同温度和有催化剂存在的条件下,两容器各自发生下列反应:X+Y![]() 2Z+ W;正反应为放热反应,(四物质均为气体)。达到平衡时。VA=1.2aL,试回答:
2Z+ W;正反应为放热反应,(四物质均为气体)。达到平衡时。VA=1.2aL,试回答:
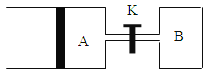
①A中的X的转化率 αA=__________;
②A、B中X的转化率αA ______αB (填“>、=、<”)
③打开K,一段时间后又达到平衡时,A 的体积为_______ L(连通管中的气体体积不计)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知水在25℃和95℃时,其电离平衡曲线如图所示:

(1)则95℃时,水的电离平衡曲线应为B,请说明理由______________________.
25℃时,将pH=9的NaOH溶液与pH=4的硫酸溶液混合,所得混合溶液的pH=7,则NaOH溶液与硫酸溶液的体积比为______________。
(2)95℃时,若100体积pH=a的某强酸溶液与1体积pH=b的某强碱溶液混合后溶液呈中性,则a与b之间应满足的关系是______________.
(3)曲线A所对应的温度下,pH=2的HCl溶液和pH=11的某BOH溶液中,若水的电离程度分别用α1、α2表示,则α1______________α2(填“大于”、“小于”、“等于”或“无法确定”)。
(4)曲线B对应温度下,将0.02mol/LBa(OH)2溶液与等物质的量浓度的NaHSO4溶液等体积混合后,混合溶液的pH=________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com