
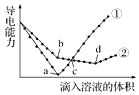
 在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示.下列分析不正确的是( )
在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示.下列分析不正确的是( )| A. | c点,两溶液中含有相同量的OH- | |
| B. | b点,溶液中大量存在的离子是Na+、OH- | |
| C. | ①代表滴加H2SO4溶液的变化曲线 | |
| D. | a、d两点对应的溶液均显中性 |
分析 A.c点,①中稀硫酸过量,溶质为硫酸,②中硫酸氢钠过量,则溶质为NaOH、Na2SO4;
B.根据图知,a点为Ba(OH)2溶液和H2SO4恰好反应,H2SO4、NaHSO4溶液的物质的量浓度相等,则b点溶液溶质为NaOH;
C.Ba(OH)2溶液和H2SO4、NaHSO4溶液反应方程式分别为H2SO4+Ba(OH)2=BaSO4↓+2H2O、NaHSO4+Ba(OH)2=BaSO4↓+NaOH+H2O,2NaHSO4+Ba(OH)2=BaSO4↓+Na2SO4+2H2O,溶液导电能力与离子浓度成正比,根据图知,曲线①在a点溶液导电能力接近0,说明该点溶液离子浓度最小,应该为Ba(OH)2溶液和H2SO4的反应,则曲线②为Ba(OH)2溶液和NaHSO4溶液的反应;
D.a点①中硫酸和氢氧化钡恰好完全反应,溶液中只含水;d点②中溶质为Na2SO4;
解答 解:A.c点,①中稀硫酸过量,溶质为硫酸,②中硫酸氢钠过量,则溶质为NaOH、Na2SO4,因为硫酸根离子浓度相同,②中钠离子浓度大于①中氢离子浓度,所以溶液中氢氧根离子浓度不同,故A错误;
B.根据图知,a点为Ba(OH)2溶液和H2SO4恰好反应,H2SO4、NaHSO4溶液的物质的量浓度相等,则b点溶液溶质为NaOH,则大量存在的离子是Na+、OH-,故B正确;
C.Ba(OH)2溶液和H2SO4、NaHSO4溶液反应方程式分别为H2SO4+Ba(OH)2=BaSO4↓+2H2O、NaHSO4+Ba(OH)2=BaSO4↓+NaOH+H2O,2NaHSO4+Ba(OH)2=BaSO4↓+Na2SO4+2H2O,溶液导电能力与离子浓度成正比,根据图知,曲线①在a点溶液导电能力接近0,说明该点溶液离子浓度最小,应该为Ba(OH)2溶液和H2SO4的反应,则曲线②为Ba(OH)2溶液和NaHSO4溶液的反应,即①代表滴加H2SO4溶液的变化曲线,故C正确;
D.a点①中硫酸和氢氧化钡恰好完全反应,溶液中只含水;d点②中溶质为Na2SO4,水和硫酸钠溶液都呈中性,故D正确;
故选A.
点评 本题考查酸碱混合溶液定性判断,为高频考点,侧重考查学生分析判断及识图能力,明确发生的反应及各点溶液中溶质成分是解本题关键,注意:溶液导电能力与离子浓度成正比,易错选项是A.


科目:高中化学 来源: 题型:选择题
| A. | 钠与水反应:2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | 钠与硫酸铜溶液的反应:2Na+Cu2+═2Na++Cu | |
| C. | 铁与稀盐酸的反应:2Fe+6H+═2 Fe 3++3H2↑ | |
| D. | 铝粉和氢氧化钠溶液的反应:2Al+2 OH-═2AlO2-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C4H9Cl | B. | C3H7Cl | C. | C6H13Cl | D. | C5H11Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2=CH-CH=CH2;l,3 一二丁烯 | |
| B. | CH3CH(C2H5)CH2CH2CH3,2 一乙基戊烷 | |
| C. |  2 一甲基一3一戊烯 2 一甲基一3一戊烯 | |
| D. |  异戊烷 异戊烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 碱性氧化物 氧化铁 Fe2O3 | B. | 酸性氧化物 干冰 CO2 | ||
| C. | 酸 硫酸 H2S | D. | 碱 纯碱 Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④⑦ | B. | ⑦ | C. | ①②⑤⑦ | D. | ①③④⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 操作 | 测定结果评价 |
| A | 酸式滴定管在装液前未用标准盐酸润洗2~3次 | 偏高 |
| B | 开始实验时酸式滴定管尖嘴部分有气泡,在滴定过程中气泡消失 | 偏高 |
| C | 锥形瓶未干燥 | 无影响 |
| D | 盛NaOH溶液的锥形瓶滴定前用NaOH溶液润洗2~3次 | 偏低 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

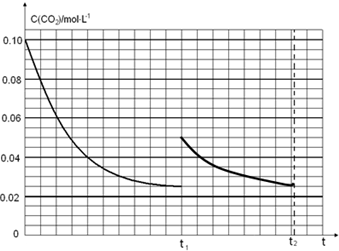 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com