
【题目】实验室要配制1mol/L的稀硫酸250mL,回答下列问题:
(1)需要98%密度为1.84g/cm3的浓硫酸_______mL。
(2)配制时,必须使用的仪器有_______(填编号)。
①烧杯 ②100mL量筒 ③20mL量筒 ④1000mL容量瓶 ⑤ 胶头滴管 ⑥托盘天平(带砝码) ⑦玻璃棒,还缺少的仪器是___________。
(3)配制过程中出现以下情况,对所配溶液浓度有何影响(填“偏高”“偏低”“不影响”):
①溶液未冷却到室温就转移到容量瓶,________。
②如果加水超过了刻度线,用胶头滴管吸出多余部分,使液面恰好到刻度线,_________。
【答案】 13.6 ①③⑤⑦ 250mL容量瓶 偏高 偏低
【解析】(1)①密度ρ=1.84gmL-1,质量分数为98%的浓硫酸的浓度为:c=![]() =18.4mol/L,配制250mL 1molL-1的稀硫酸,需要该浓硫酸的体积为:
=18.4mol/L,配制250mL 1molL-1的稀硫酸,需要该浓硫酸的体积为: ![]() ≈0.0136L=13.6mL,故答案为:13.6;
≈0.0136L=13.6mL,故答案为:13.6;
(2)配制250mL1mol/L的稀硫酸的步骤为:计算→量取→稀释、冷却→移液→定容→摇匀→装瓶→贴签,需要使用的仪器有:①烧杯③20mL量筒⑤胶头滴管⑦玻璃棒;定容时必须使用250mL容量瓶,所以还缺少的仪器为250mL容量瓶,故答案为:①③⑤⑦;250mL容量瓶;
(3)①溶液未冷却到室温就转移到容量瓶,导致配制的溶液的体积偏小,配制的溶液浓度偏高,故答案为:偏高;
②如果加水超过了刻度线,用胶头滴管吸出多余部分,使液面恰好到刻度线,导致溶质的物质的量偏少,配制的溶液浓度偏低,故答案为:偏低。


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
【题目】将Na2O2投入FeCl3溶液中,可观察到的现象是 ( )
①生成白色沉淀 ②生成红褐色沉淀 ③有气泡产生
④因为Na2O2具有漂白性,所以FeCl3溶液褪色
A. ①④ B. ②③ C. ①③ D. 仅②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中只含有Na+, Al3+,Cl-,SO42-四种离子,已知前三种离子的个数比为3∶2∶1,则溶液中Al3+和 SO42-的离子个数比为
A. 1:2 B. 1:4 C. 3:4 D. 3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是实验室中制备气体或验证气体性质的装置图

(1)发生装置A中制取氯气的化学方程式 .
(2)利用上图装置制备纯净的氯气,并证明氧化性:C12>Fe3+
则装置B中的溶液的作用是 ;装置D中加的最佳试剂是(填序号) :供选试剂:a.浓H2SO4b.FeCl2溶液 c.无水氯化钙 d.KSCN与FeCl2的混合溶液
(3)在图所示圆底烧瓶内加入碳,a中加入浓硫酸,开始实验,加热产生的气体缓慢通过后续装置同时完成如下实验:
实验1:证明SO2具有氧化性和漂白性
实验2:证明碳元素的非金属性比硅元素的强
证明SO2具氧化性和漂白性:B中为少量Na2S溶液、C中加品红溶液,D中应加入足量的 (填溶液名称),E中加入 溶液(填化学式).
(4)证明碳元素的非金属性比硅元素的强的现象为 ;实验2不严谨之处应如何改进 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某矿渣主要含硫酸钡、氧化铜、氧化铝等(杂质不参加反应),利用矿渣提取金属的工艺流程如图所示(乙、丙、丁、戊均为单质):

回答下列问题:
(1)沉淀①为_____________(填“强”、“弱”或“非”)电解质。
(2)灼烧沉淀②所需要的非玻璃仪器有坩埚、__________、___________、__________。
(3)滤液①的主要成分为___________________________。
(4)滤液①中加入适量盐酸发生的离子方程式为_______________、__________________。
(5)反应①的反应条件是________________________。
(6)电解滤液③时阴极的电极反应式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①Na3N+3H2O=3NaOH+NH3↑,②NaH+H2O=NaOH+H2↑。下列叙述正确的是
A. 离子半径:Na+>N3->H+
B. 反应①和②都是氧化还原反应
C. 反应②每生成1 mol H2,转移的电子数为NA
D. Na3N和NaH与盐酸反应都只生成一种盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知氯气与NaOH溶液反应可生成NaCl、NaClO、NaClO3,NaClO在加热条件下分解生成NaCl和NaClO3,现向氢氧化钠溶液中通入一定量的氯气,加热少许时间后溶液中形成混合体系。下列判断不正确的是( )
A. 若反应过程中消耗1 mol氯气,则1 mol<转移电子数<![]() mol
mol
B. 反应停止后n(NaClO)∶n(NaCl)∶n(NaClO3)(物质的量之比)可能为1∶11∶2
C. 反应过程中消耗氯气与NaOH的物质的量之比为1∶2
D. 氧化产物为NaClO和NaClO3,反应过程中n(NaClO)∶n(NaClO3)为1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaOH标准溶液的配制和标定时,需经过NaOH溶液的配制、基准物质H2C2O4·2H2O的称量以及用NaOH溶液滴定等操作。下列操作正确的是( )
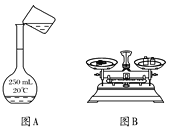
A. 用图A所示的方法转移NaOH溶液到容量瓶中
B. 用图B所示的装置准确称得0.15 g H2C2O4·2H2O
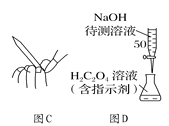
C. 用图C所示的操作排除碱式滴定管中的气泡
D. 用图D所示的装置,用NaOH待测液滴定H2C2O4溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com