
【题目】如图装置闭合电键K时,电流计A的指针将发生偏转。试回答:

(1) 丙池是____________(填“原电池”或“电解池”),甲中a极电极名称是________________,丙中c极电极名称是_____________________;
(2)乙中Cu极的电极反应式是__________,若电路中有0.02mol电子通过,则甲中a电极溶解的质量为__________g;
(3)闭合电键K一段时间后,丙池中生成两种气体和一种碱,则丙池中发生的总的化学方程式是_________________;
(4)丙池中反应进行较长时间后,收集到标准状况下氢气2.24L,此时测得丙池溶液质量实际减少4.23 g,含有碱0.100mol(不考虑气体在水中的溶解),则实际放出气体的物质的量是______________mol;
(5)如果要给丙中铁片上镀上一层Cu,则丙池应作何改进_________________________。
【答案】电解池 负极 阳极 Cu2++2e- = Cu 0.65 2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑ 0.165 “C”换成“Cu”、将“NaCl溶液”换成“CuSO4溶液”
2NaOH+H2↑+Cl2↑ 0.165 “C”换成“Cu”、将“NaCl溶液”换成“CuSO4溶液”
【解析】
(1)甲和乙形成原电池,所以丙有外加电源,属于电解池;甲中a失电子为负极;丙中c电极连接原电池的正极属于阳极,故答案为:电解池;负极;阳极;
(2)乙中Cu极上铜离子得电子生成铜单质,其电极反应为:Cu2++2e-=Cu;Zn从0价升高到+2价失去2个电子,已知电路中有0.02mol电子通过,所以消耗的Zn为0.01mol,m(Zn)=nM=65g/mol×0.01mol=0.65g,故答案为:0.65g;
(3)丙池中是电解NaCl溶液生产氢气,氯气和氢氧化钠,其电解方程式:2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑,故答案为:2NaCl+2H2O
2NaOH+H2↑+Cl2↑,故答案为:2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑;
2NaOH+H2↑+Cl2↑;
(4)已知碱0.100mol,n(H2)=![]() =0.1mol,由电解方程式可知,生成碱0.100mol,时,n(H2)=0.05mol,所以m(H2)=nM=0.1mol×2g/mol=0.2g,m( Cl2)=nM=0.05mol×71g/mol=3.55g,丙池溶液质量实际减少4.23g,是氢气、氯气和氧气的质量和,所以m(O2)=4.23g-3.55g-0.2g=0.48g,n(O2)=0.48g÷32g/mol=0.015mol,因此实际放出气体的物质的量是:0.1mol+0.05mol+0.015mol=0.165mol,故答案为:0.165;
=0.1mol,由电解方程式可知,生成碱0.100mol,时,n(H2)=0.05mol,所以m(H2)=nM=0.1mol×2g/mol=0.2g,m( Cl2)=nM=0.05mol×71g/mol=3.55g,丙池溶液质量实际减少4.23g,是氢气、氯气和氧气的质量和,所以m(O2)=4.23g-3.55g-0.2g=0.48g,n(O2)=0.48g÷32g/mol=0.015mol,因此实际放出气体的物质的量是:0.1mol+0.05mol+0.015mol=0.165mol,故答案为:0.165;
(5)要给丙中铁片上镀上一层Cu,则阳极应该为Cu电极,电解质溶液为硫酸铜溶液,故答案为:把C电极换成Cu电极,把NaCl溶液换为硫酸铜溶液。


科目:高中化学 来源: 题型:
【题目】已知H2(g)、C2H4(g)和C2H5OH(1)的燃烧热分别是-285.8kJ·mol-1、-1411.0kJ·mol-1和-1366.8kJ·mol-1,则由C2H4(g)和H2O(l)反应生成C2H5OH(l)的△H为( )
A. -44.2kJ·mol-1 B. +44.2kJ·mlo-1
C. -330kJ·mol-1 D. +330kJ·mlo-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.Al、SiO2、Ca(OH)2、NaHCO3等既能与盐酸反应,又能与氢氧化钠溶液反应
B.若a、b、c分別为Si、SiO2、H2SiO3,则可以通过一步反应实现如图所示的转化关系![]()
C.Fe2O3![]() Fe2(SO4)3(aq)
Fe2(SO4)3(aq)![]() 无水Fe2(SO4)3
无水Fe2(SO4)3
D.Na![]() Na2O2
Na2O2![]() NaI
NaI
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质互为同分异构体的是
A.![]() 和
和![]()
B.CH3— CH2—CH3 和CH3—CH2—CH2—CH3
C.CH3—CH=CH—CH3和 CH2=CH—CH2—CH3
D.CH≡CH 和CH≡C—CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重铬酸钾(K2Cr2O7)溶液是实验和科研中一种常用氧化剂。酸性条件下,Cr2O72—通常被还原为Cr3+。
(1)某同学欲用K2Cr2O7固体配制500 mL 0.04000 mol·L-1的K2Cr2O7溶液。
①需用的玻璃仪器有烧杯、玻璃棒、量筒、 ____。
②应该称取K2Cr2O7固体的质量为______。
(2)交警常用装有重铬酸钾酒精测试仪检测司机是否酒后驾车,其化学反应原理如下:2K2Cr2O7+3C2H5OH+8H2SO4===2Cr2(SO4)3+3CH3COOH+2K2SO4+11H2O。每有1 mol C2H5OH发生反应,转移电子的物质的量是__。
(3)由两种阳离子和一种阴离子组成的化合物X(不带结晶水)。将两份质量相等的化合物X,分别配成溶液,分别进行如下实验:
步骤1:向其中一份溶液中加入足量Ba(OH)2溶液并加热,有气体逸出,该气体能使湿润的红色石蕊试纸变蓝,同时生成白色沉淀,随即沉淀变为灰绿色,最后带有红褐色,用足量稀盐酸处理上述沉淀物,经洗涤和干燥,得到白色固体2.33 g。
步骤2:将另一份溶液与0.04000 mol·L-1的酸性K2Cr2O7溶液反应,消耗K2Cr2O7溶液20.84 mL。
试通过计算确定化合物X的化学式______。(写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验现象预测正确的是( )
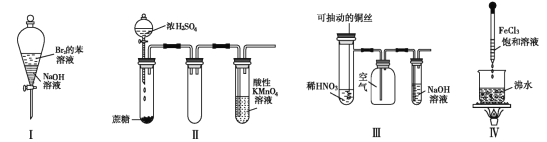
A. 实验Ⅰ:振荡后静置,上层溶液颜色保持不变
B. 实验Ⅱ :酸性 KMnO4 溶液中出现气泡,且颜色逐渐褪去
C. 实验Ⅲ:微热稀 HNO3 片刻,溶液中有气泡产生,广口瓶内始终保持无色
D. 实验Ⅳ:滴入 FeCl3 后,可形成带电的胶体,该分散系导电能力增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在探究新制氯水成分及性质的实验中,依据下列方法和现象,不能得出相应结论的是
方法 | 现象 | 结论 | |
A | 观察氯水颜色 | 氯水呈黄绿色 | 氯水中含Cl2 |
B | 向饱和NaHCO3溶液中加入足量氯水 | 有无色气体产生 | 氯水中含HClO |
C | 向红色纸条上滴加氯水 | 红色纸条褪色 | 氯水具有漂白性 |
D | 向FeCl2溶液中滴加氯水 | 溶液变成棕黄色 | 氯水具有氧化性 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,关于1mol·L-1的H2C2O4溶液的理解正确的是( )
A.加水稀释过程中,溶液的pH减小
B.c(H2C2O4)+c(HC2O4-)+c(C2O42-)=1mol·L-1
C.溶液中,1mol·L-1<c(H+)<2mol·L-1
D.溶液中,H2C2O4电离出的c(H+):c(C2O42-)=2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于碳酸钠和碳酸氢钠的比较中,错误的是
A. 二者在一定的条件下可以相互转化
B. 可以用澄清石灰水对二者进行鉴别,能产生白色沉淀的为碳酸钠
C. 等质量的碳酸钠与碳酸氢钠与足量盐酸反应,后者更剧烈,前者产生二氧化碳少
D. 将二氧化碳通入到饱和碳酸钠溶液中,有浑浊产生,原因之一是碳酸钠溶解度更大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com