
【题目】将一定量Fe、FeO和Fe2O3的混合物加入240 mL 2 mol·L-1稀硝酸中,恰好完全反应,放出1.344 L(标准状况下)NO气体,往所得溶液中加入酸性KMnO4溶液,无明显现象。若用足量的H2在加热条件下与相同质量的上述混合物充分反应,能得到铁的质量为
A.6.72gB.7.84gC.8.96gD.11.76g
科目:高中化学 来源: 题型:
【题目】工业上常利用反应Cr2O7n-+CH3OH+H+→Cr3++CO2↑+H2O(未配平)来测定工业甲醇中甲醇的含量,下列说法中正确的是( )
A. 溶液的颜色从灰绿色变为橙色
B. Cr2O7n-发生氧化反应
C. 若配平后Cr3+和CO2的化学计量数比为2:1,则Cr2O7n-中的n=2
D. 若有3.2 g CH3OH参加反应,则转移的电子数为6.02×1022
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语表达不正确的是( )
①丙烷的球棍模型 ②丙烯的结构简式为CH3CHCH2
②丙烯的结构简式为CH3CHCH2
③某有机物的名称是2,3-二甲基戊烷 ④![]() 与C8H6互为同分异构体
与C8H6互为同分异构体
A. ①②B. ②③C. ②④D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KNO3和Cu(NO3)2的混合溶液200mL,其中c(NO3-)=2mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到2.24L气体(标准状况),假设电解后溶液体积不变,下列说法正确的是( )
A.原混合溶液中c(K+)=0.5mol·L-1
B.电解得到的Cu的物质的量为0.2mol
C.上述电解过程中共转移0.4mol电子
D.电解后溶液中c(H+)=2mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解原理在化学工业中有广泛的应用。如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
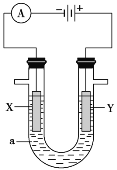
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中X极上的电极反应式为__________________,在X极附近观察到的现象是__________________。
②Y电极上的电极反应式为_____________,检验该电极反应产物的方法是______________________。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:①Y电极的材料是_______________,主要的电极反应式为_____________________。
②溶液中的c(Cu2+)与电解前相比________(填“变大”、“变小”或“不变”)。
(3)如利用该装置实现铁上镀锌,电极X上发生的反应为_______________________,电解池盛放的电镀液可以是__________________________(只要求填一种电解质溶液)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿魏酸在食品、医药等方面有着广泛用途。一种合成阿魏酸的反应可表示为( )
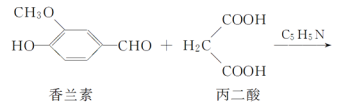

下列说法不正确的是( )
A. 不可用酸性KMnO4溶液检测上述反应是否有阿魏酸生成
B. 与香兰素互为同分异构体,分子中有5种不同化学环境的氢,且能发生银镜反应的酚类化合物共有3种
C. 通常条件下,香兰素、阿魏酸都能发生取代、加成、氧化反应
D. 香兰素、阿魏酸均可与Na2CO3、NaOH溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,某恒容密闭容器中含有![]() 、
、![]() 两种气体,反应开始至达到平衡状态过程中,两种物质的浓度随时间的变化如下所示。
两种气体,反应开始至达到平衡状态过程中,两种物质的浓度随时间的变化如下所示。

(1)表示 NO2浓度变化的曲线是________________,写出相应的化学方程式:________________________
(2)从反应开始至达到平衡的过程中,用![]() 表示的反应速率
表示的反应速率![]() =__________________________,a、b两点对应状态中,曲线X代表的物质的反应速率相对大小为v(a)_____v(b)。
=__________________________,a、b两点对应状态中,曲线X代表的物质的反应速率相对大小为v(a)_____v(b)。
(3)下列叙述说明该反应达到化学平衡的是_______________________
A、单位时间生成n mol NO2同时生成n mol N2O4
B、容器内气体颜色不变
C、混合气体的密度不变
D、混合气体的平均相对分子质量不变
E、混合气体的物质的量不变
F、容器内气体压强不变
G、混合气体中NO2的体积分数不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下超氧化钾晶体呈立方体结构,晶体中氧的化合价部分为0价,部分为﹣2价.如图所示为超氧化钾晶体的一个晶胞(晶体中最小的重复单元),则下列说法中正确的是

A. 晶体中每个K+周围有8个O2﹣,每个O2﹣周围有8个K+
B. 晶体中与每个K+距离最近的K+有8个
C. 超氧化钾的化学式为KO2,每个晶胞含有4个K+和4个O2﹣
D. 晶体中,0价氧与﹣2价氧的数目比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在密闭容器里进行如下可逆反应:![]() 橙黄色液体
橙黄色液体![]() 气
气![]() 鲜红色液体
鲜红色液体![]() 。下列说法正确的是
。下列说法正确的是![]()
![]()
A. 达到平衡时,单位时间里消耗nmol![]() 的同时也生成n
的同时也生成n![]()
B. 增大压强,平衡常数将增大
C. 达到平衡时,若升高温度,氯气的百分含量减小
D. 加入氯气,平衡向正反应方向移动,氯气的转化率一定升高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com