
【题目】电解原理在化学工业中有广泛的应用。如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
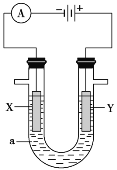
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中X极上的电极反应式为__________________,在X极附近观察到的现象是__________________。
②Y电极上的电极反应式为_____________,检验该电极反应产物的方法是______________________。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:①Y电极的材料是_______________,主要的电极反应式为_____________________。
②溶液中的c(Cu2+)与电解前相比________(填“变大”、“变小”或“不变”)。
(3)如利用该装置实现铁上镀锌,电极X上发生的反应为_______________________,电解池盛放的电镀液可以是__________________________(只要求填一种电解质溶液)。
【答案】2H++2e-=H2↑ 有气体放出,溶液变红 2Cl--2e-=Cl2↑ 把湿润的淀粉碘化钾试纸放在Y电极附近,试纸变蓝色,说明生成了Cl2 纯铜 Cu2++2e-=Cu 变小 Zn2++2e-=Zn ZnCl2(或ZnSO4溶液)
【解析】
(1)①若X、Y都是惰性电极,a是饱和NaCl溶液,和电源的负极相连的电极X极是阴极,该电极上氢离子发生得电子的还原反应,即2H++2e=H2↑,所以该电极附近氢氧根浓度增大,碱性增强,滴入几滴酚酞试液会变红,
故答案为:2H++2e=H2↑;溶液变红,有气泡产生;
②和电源的正极相连的电极,Y极是阳极,该电极上氯离子发生失电子的氧化反应,即2Cl2e=Cl2↑,氯气可用淀粉碘化钾试纸检验,可使试纸变蓝色,
故答案为:2Cl2e=Cl2↑;把湿润的淀粉碘化钾试纸放在Y电极附近,试纸变蓝色,说明生成了Cl2;
(2)①电解方法精炼粗铜,电解池的X电极是阴极,材料是纯铜,电极反应为:Cu2++2e=Cu,
故答案为:纯铜;Cu2++2e=Cu;
②电解方法精炼粗铜,阴极是Cu2++2e=Cu,阳极上先是金属锌、铁、镍等金属失电子,然后是铜失电子生成铜离子的过程,所以电解后,铜离子浓度是减小的,
故答案为:变小;
(3)如利用该装置实现铁上镀锌,镀件铁是阴极,镀层金属锌是阳极,电极X极即阴极上发生的反应为:Zn2++2e=Zn,电镀液是含有镀层金属阳离子的盐溶液,可以是ZnCl2溶液或是ZnSO4溶液。
故答案为:Zn2++2e=Zn;ZnCl2溶液(或ZnSO4溶液)。


 华东师大版一课一练系列答案
华东师大版一课一练系列答案科目:高中化学 来源: 题型:
【题目】铅丹(Pb3O4)可作防锈用涂料,已知铅丹中Pb元素的化合价只有+2、+4,且+2价稳定,+4价的Pb具有强氧化性,能氧化浓盐酸生成Cl2。则下列说法不正确的是 ( )
A. Pb3O4可表示为2PbO·PbO2
B. 可用PbO在空气中加热制备铅丹,其n(氧化剂):n(还原剂)=1:6
C. 0.1mol Pb3O4与足量的浓盐酸反应,生成Cl20.1 mol
D. a mol Pb3O4加强热分解生成PbO,则加热过程中转移电子数为2a NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以高硫铝土矿(主要成分为Al2O3、Fe2O3、SiO2,少量FeS2和金属硫酸盐)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如下:
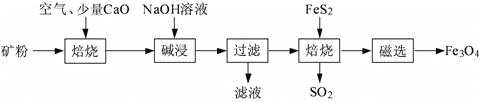
(1)焙烧过程均会产生SO2,用NaOH溶液吸收过量SO2的离子方程式为:___________________。
(2)“过滤”得到的滤渣中含有大量的Fe2O3。
①不添加CaO的矿粉焙烧时,其中FeS2转化为Fe2O3时发生的化学方程式:____________。
②添加质量分数为1%CaO后,硫元素最终转化为______________。(填化学式)
(3)向“过滤”得到的滤液中通入过量CO2,含铝元素的物质发生转化的离子方程式为_____________。
(4)“过滤”得到的滤渣中含大量的Fe2O3。Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,理论上完全反应消耗的n(Fe2O3)∶n(FeS2)=_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液可能含有Cl-、SO![]() 、CO
、CO![]() 、NH
、NH![]() 、Fe3+、Al3+和K+。取该溶液100 mL,加入过量NaOH溶液,加热,得到0.02 mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6 g固体;向上述滤液中加足量BaCl2溶液,得到4.66 g不溶于盐酸的沉淀。由此可知原溶液中
、Fe3+、Al3+和K+。取该溶液100 mL,加入过量NaOH溶液,加热,得到0.02 mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6 g固体;向上述滤液中加足量BaCl2溶液,得到4.66 g不溶于盐酸的沉淀。由此可知原溶液中
A.至少存在5种离子B.Cl-一定存在,且c(Cl-)≥0.4 mol·L-1
C.SO![]() 、NH
、NH![]() 一定存在,Cl-可能不存在D.CO
一定存在,Cl-可能不存在D.CO![]() 、Al3+一定不存在,K+可能存在
、Al3+一定不存在,K+可能存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaClO是漂白液的有效成分,某研究小组探究NaClO溶液的性质,设计了下列实验:
装置图 | 试剂X | 实验现象 | |
| ① | 0.2molL-1盐酸 | 产生黄绿色气体 |
② | 0.2molL-1KI-淀粉溶液 | 溶液变蓝 | |
③ | 0.2molL-1FeSO4(H+)和KSCN混合溶液 | 溶液变红 | |
④ | 0.2molL-1AlCl3溶液 | 产生白色沉淀 | |
下列判断不正确的是
A.实验①中发生的反应:ClO-+Cl-+2H+=Cl2↑+H2O
B.实验②中发生的反应:ClO-+2I-+2H+=Cl-+I2+H2O
C.实验③中该条件下氧化性强弱:ClO->Fe3+
D.实验④中ClO-与Al3+相互促进水解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量Fe、FeO和Fe2O3的混合物加入240 mL 2 mol·L-1稀硝酸中,恰好完全反应,放出1.344 L(标准状况下)NO气体,往所得溶液中加入酸性KMnO4溶液,无明显现象。若用足量的H2在加热条件下与相同质量的上述混合物充分反应,能得到铁的质量为
A.6.72gB.7.84gC.8.96gD.11.76g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置中有机物样品在电炉中充分燃烧,通过测定生成的CO2和H2O的质量,来确定有机物分子式。
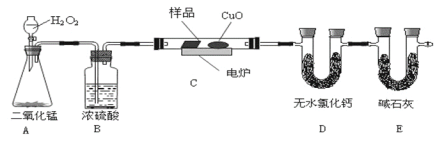
(1)A装置是提供实验所需的O2, C中CuO的作用是____________。
(2)若实验中所取样品只含C、H、O三种元素中的两种或三种,准确称取0.44 g样品,经充分反应后,D管质量增加0.36g,E管质量增加0.88 g,已知该物质的相对分子质量为44,则该样品的化学式为_________。
(3)若该有机物的核磁共振氢谱如下图所示,峰面积之比为1:3则其结构简式为__________________;该化合物具有的性质是:_________。(填序号)
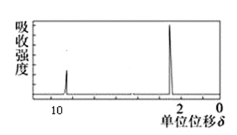
A、能与水、乙醇、氯仿等互溶 B、无色、无味液体
C、能使酸性KMnO4溶液和溴水褪色 D、任何条件下不能与H2反应
(4)若符合下列条件,则该有机物的结构简式为_____________________ 。
①环状化合物②只有一种类型的氢原子
(5)某同学认E和空气相通,会影响测定结果准确性,应在E后再增加一个装置E,其主要目的是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镓(Ga)与铝同主族,曾被称为“类铝”,其氧化物和氢氧化物均为两性化合物。工业制备镓的流程如图所示:
![]()
下列判断不合理的是( )
A. Al、Ga均处于ⅢA族B. Ga2O3可与盐酸反应生成GaCl3
C. 酸性:Al(OH)3>Ga(OH)3D. Ga(OH)3可与NaOH反应生成NaGaO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表所示为元素周期表的一部分,参照元素①~⑩在表中的位置,请回答下列问题:

(1)写出①和④两种元素原子按1:1组成的常见化合物的电子式______。
(2)用电子式表示⑥和⑨形成化合物的过程:______。
(3)③、⑧、⑩的最高价氧化物对应水化物的酸性由强到弱的顺序为 ______(用化学式表示)。
(4)已知周期表中存在对角相似规则,如②与⑦在周期表中处于对角线位置则化学性质相似,②的氧化物、氢氧化物也有两性,写出②的氢氧化物与⑥的氢氧化物反应的化学方程式 ______。
(5)⑤、⑥、⑩的离子半径由大到小的顺序为 ______(用离子符号表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com