
【题目】绿矾(FeSO4·7H2O)外观为半透明蓝绿色单斜结晶或颗粒,无气味。受热能分解,且在空气中易被氧化。
I.医学上绿矾可用于补血剂甘氨酸亚铁[(NH2CH2COO)2Fe]颗粒的制备,有关物质性质如下:
甘氨酸(NH2CH2COOH) | 柠檬酸 | 甘氨酸亚铁 |
易溶于水,微溶于乙醇,两性化合物 | 易溶于水和乙醇,有强酸性和还原性 | 易溶于水,难溶于乙醇 |
(1)向绿矾溶液中,缓慢加入NH4HCO3溶液,边加边搅拌,反应结束后生成沉淀FeCO3。该反应的离子方程式为_______。
(2)制备(NH2CH2COO)2Fe:往FeCO3中加入甘氨酸(NH2CH2COOH)的水溶液,滴入柠檬酸溶液并加热。反应结束后过滤,滤液经蒸发结晶、过滤、洗涤、干燥得到产品。
①加入柠檬酸溶液一方面可调节溶液的pH促进FeCO3溶解,另一个作用是__。
②洗涤操作,选用的最佳洗涤试剂是_______(填序号)。
A.热水 B.乙醇 C.柠檬酸
II.绿矾晶体受热分解的反应为2FeSO4·7H2O![]() Fe2O3+SO2↑+SO3↑+14H2O,实验室用图I所示装置验证其分解产物。请回答下列问题:
Fe2O3+SO2↑+SO3↑+14H2O,实验室用图I所示装置验证其分解产物。请回答下列问题:
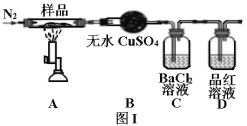
(1)加热前通入氮气的目的是_______。
(2)实验中观察到装置B现象为_______。
(3)C装置和D装置能否调换_______(填“能”或“否”)。
(4)样品完全分解后,残留物全部为红棕色固体,检验装置A中的残留物含有Fe2O3的方法是_______。
(5)该装置有个明显缺陷是_______。
III.测定绿矾样品中铁元素的含量。
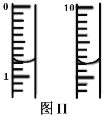
称取m g绿矾样品于锥形瓶中溶解后加稀H2SO4酸化,用 c mol·L1 KMnO4 溶液滴定至终点。耗KMnO4溶液体积如图II所示,(滴定时发生反应的离子方程式为:5Fe2++MnO4+8H+=5Fe3++Mn2++4H2O),该晶体中铁元素的质量分数为_______(用含m、c的式子表示)。
【答案】Fe2++2HCO3=FeCO3↓+CO2↑+ H2O 防止二价铁被氧化 B 将装置内空气排尽(或隔绝空气或防止Fe2+被氧化) 白色粉末变蓝 否 取少许固体粉末于试管中,加稀硫酸溶解,滴入1~2滴KSCN溶液,溶液变红色,证明含有Fe2O3 没有尾气处理装置 ![]()
【解析】
Ⅰ(1)FeCl2溶液中,加入NH4HCO3,可以认为Fe2+结合HCO3-电离出来的CO32-,H+与HCO3-结合生成CO2和水;
(2)柠檬酸除了酸性还有还原性,可以起到防氧化的作用;
(3)产物易溶于水,难溶于乙醇,洗涤时,为了防止溶解损失,应该用乙醇洗涤;
Ⅱ绿矾分解,其产物中有SO2、SO3和水,
用无水硫酸铜验证水,用BaCl2溶液验证SO3,品红溶液验证SO2。
Ⅰ(1) FeCl2溶液中,加入NH4HCO3,可以认为Fe2+结合HCO3-电离出来的CO32-,H+与HCO3-结合生成CO2和水,离子方程式为Fe2++2HCO3=FeCO3↓+CO2↑+ H2O;
(2)根据表中信息,柠檬酸除了酸性还有还原性,可以起到防氧化的作用,因此另一个作用是防止二价铁被氧化;
(3)甘氨酸亚铁易溶于水,难溶于乙醇,为了防止溶解损失,可以用乙醇洗涤,答案选B;
II(1)加热前通氮气,排除装置中的空气,防止样品,加热是被氧化;
(2)产物中有水,无水硫酸铜,遇到水蒸气,变蓝色;
(3)SO3会溶于水,生成H2SO4,如果C、D装置调换位置,SO3会溶于品红溶液,不能进入C中,被检验到;
(4)检验Fe2O3,可以检验Fe3+,用KSCN溶液,方法为取少许固体粉末于试管中,加稀硫酸溶解,滴入1~2滴KSCN溶液,溶液变红色,证明含有Fe2O3;
(5)品红溶液只能用于检验SO2,不能吸收SO2,SO2为有毒气体,需要进行尾气出来,该装置的缺陷是没有气体处理装置;
III根据化学方程式,可知关系式5Fe2+~MnO4,消耗KMnO4溶液的体积为10.80mL-0.80mL=10.00mL,则n(KMnO4)=10.00mL×10-3×cmol·L-1=0.01cmol;n(Fe2+)=5n(KMnO4)=0.01cmol×5=0.05cmol;则铁元素的质量为0.05cmol×56g·mol-1=2.8cg,则晶体中铁元素的质量分数为![]() 。
。


 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源: 题型:
【题目】某同学设计了如图实验装置探究硝酸的性质,根据图示判断下列结论不正确的是

A. 试管内壁上的“黄霜”的成分是硫
B. 该实验既说明了浓硝酸具有氧化性,又说明了浓硝酸具有挥发性
C. 烧杯内氢氧化钠溶液的作用是除去尾气,防止尾气污染环境
D. 试管中浓硝酸可以用浓盐酸代替
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据相关知识回答下列问题
(1)①已知H2与O2反应生成lmolH2O(g)时放出241.8kJ的热量,请完成该反应的热化学方程式:2H2(g)+O2(g)-2H2O(g)△H=_____________kJ/mol;
②已知:C(石墨,s)=C(金刚石,s)△H>0 则稳定性:石墨_________金刚石(填“>”、“<“或“=”)。
(2)①25℃时,0.10mol/L的NaHCO3溶液呈碱性,原因是_________水解引起的(填“Na+”或“HCO3-”);该溶液中c(Na+)+c(HCO3-)_________0.2mol/L(填“>”、“<“或 “=”)
②常温下,0.0100mol/L盐酸的pH=________________;
③用0.0100mol/L盐酸滴定未知浓度的NaOH溶液,酚酞作指示剂,滴定终点时,溶液的颜色由浅红色变为__________(填“蓝色“或“无色”),且半分钟内保持不变。
(3)在某密闭容器中进行可逆反应:FeO(s)+CO(g)![]() Fe(s)+CO2(g)△H>0, 平衡常数表达式为K=
Fe(s)+CO2(g)△H>0, 平衡常数表达式为K=![]()
①反应达到平衡后,向容器中通入CO,化学平衡向__________方向移动(填“正反应”或“逆反应”);
②若升高温度,平衡常数K____________(填“增大”、“减少”“不变”);
③查阅资料得知1100℃时K=0.263。某时刻测得容器中c(CO2)=0.025mol/L,c(CO)=0.10mol/L,此时刻反应_____________平衡状态(填“达到”或“未达到”);其理由为:__________(写出必要的计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分枝酸可用于生化研究。其结构简式如下图。下列关于分枝酸的叙述正确的是( )
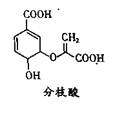
A.分子中含有3种官能团
B.1mol分枝酸最多可与3mol NaOH发生中和反应
C.可与乙醇、乙酸反应,且反应类型相同
D.可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是一种以液态肼(N2H4)为燃料,某固体氧化物为电解质的新型燃料电池。该电池的工作温度可高达700~900℃,生成物均为无毒无害的物质。下列说法错误的是
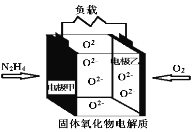
A.电池总反应为:N2H4+2O2=2NO+2H2O
B.电池内的O2由电极乙移向电极甲
C.当甲电极上消耗lmol N2H4时,乙电极理论上有 22.4L(标准状况下)O2参与反应
D.电池正极反应式为:O2+4e=2O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列方程式书写正确的是( )
A. HCO3-在水溶液中的电离方程式:HCO3-+H2O![]() H3O++CO32-
H3O++CO32-
B. H2SO3的电离方程式H2SO3![]() 2H++SO32-
2H++SO32-
C. CO32-的水解方程式:CO32-+2H2O![]() H2CO3+2OH-
H2CO3+2OH-
D. CaCO3的电离方程式:CaCO3 ![]() Ca2++CO32-
Ca2++CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是( )
A.煤中含有苯、甲苯、二甲苯等芳香烃,可通过干馏得到
B.C6H3Cl2Br的同分异构体有7种(不含立体异构)
C.乙醇和乙酸均能与酸性KMnO4溶液发生氧化反应
D.X是苯的同系物,苯环上有两个位于对位的取代基,其结构可表示为![]() ,则X的结构共有(不考虑立体异构)10种
,则X的结构共有(不考虑立体异构)10种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学实验可以验证化学假说,获得化学事实,下列实验仪器常用于物质分离的是
①普通漏斗 ②量筒 ③蒸馏烧瓶 ④滴定管 ⑤分液漏斗 ⑥容量瓶
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化硅(Si3N4)是一种新型陶瓷材料,它由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2(s)+6C(s)+2N2(g)![]() Si3N4(s)+6CO(g)。
Si3N4(s)+6CO(g)。
(1)该反应的平衡常数表达式为K=_________;
(2)若知上述反应为放热反应,则其反应热△H___0(填“>”、“<”或“=”);升高温度,其平衡常数值___(填“增大”、“减小”或“不变”);若已知CO生成速率为v(CO)=18molL﹣1min﹣1,则N2消耗速率为v(N2)=_____;
(3)达到平衡后,改变某一外界条件(不改变N2、CO的量),反应速率v与时间t的关系如图.图中t4时引起平衡移动的条件可能是___;图中表示平衡混合物中CO的含量最高的一段时间是_____。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com