
【题目】下列有关化学用语正确的是 ( )
A.乙烯的最简式 C2H4B.乙炔的结构简式 CHCH
C.四氯化碳的电子式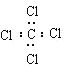 D.甲烷的比例模型
D.甲烷的比例模型![]()
【答案】D
【解析】
A.最简式是元素原子个数的最简比;
B.乙炔的结构简式中没有标出碳碳三键
C.四氯化碳的电子式中,氯原子的最外层达到8电子稳定结构,漏掉了氯原子的最外层3对未成键电子;
D.甲烷分子中含有4个碳氢键,为正四面体结构,碳原子的相对体积较大。
A.乙烯的结构简式为:CH2=CH2,乙烯的分子式为C2H4,最简式为CH2,故A错误;
B.乙炔分子中含有碳碳三键,其结构简式中必须标出官能团碳碳三键,正确的结构简式为CH≡CH,故B错误;
C.四氯化碳分子中含有4个碳氯键,碳原子和氯原子最外层达到8电子稳定结构,四氯化碳正确的电子式为: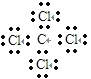 ,故C错误;
,故C错误;
D.甲烷为正四面体结构,其比例模型为![]() ,故D正确;
,故D正确;
故选:D。


 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案 全优冲刺100分系列答案
全优冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】某密闭容器中发生如下反应:X(g)+3Y(g)2Z(g);△H<0.上图表示该反应的速率(v)随时间
(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中不正确的是( )

A. ![]() 时加入了催化剂B.
时加入了催化剂B. ![]() 时降低了温度
时降低了温度
C. ![]() 时增大了压强D.
时增大了压强D. ![]() 时间内转化率最高
时间内转化率最高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硫酰氯(SOC12)又名氯化亚砜,其熔点一105℃,沸点79℃,140℃以上时易分解。是一种无色或淡黄色发烟液体,遇水剧烈与水反应生成SO2和另一酸性气体,常用作脱水剂,广泛应用于医药、农药、来料工业及有机合成工业。
(1)氯化亚砜储存于阴凉、干燥、通风良好的库房,但久置后微显黄色,其原因是___;用硫黄、液氯和三氧化硫为原料在一定条件可合成氯化亚砜,如果想达到原子利用率最大化,则三者的物质的量之比为___。
(2)实验室合成SOCl2的原理之一为SO2+Cl2+SCl2![]() 2SOCl2,部分装置如图所示。
2SOCl2,部分装置如图所示。
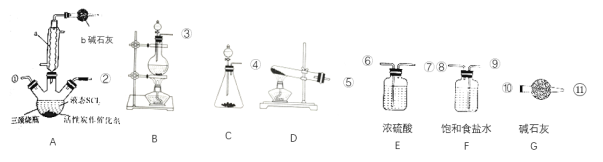
①装置b的作用是___。
②实验室制取SOCl2所选仪器的链接顺序:③→___。
(3)甲同学设计如图装置用ZnCl2·xH2O晶体制取无水ZnCl2,回收剩余的SOCl2并验证生成物中含有SO2(夹持及加热装置略)。选用装置如图: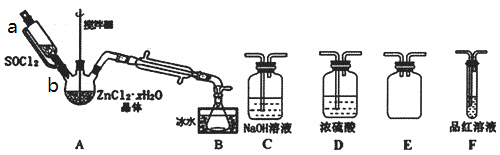
①向仪器A中缓慢滴加SOCl2,需打开活塞___(填“a”、“b”或“a和b”)。
②为了更加充分的回收SOCl2,写出可对装置B采取的有效措施___。
(4)乙同学认为利用(3)中装置,由FeCl3·6H2O制取无水FeCl3也可用SOCl2作脱水剂,但丙同学认为会发生氧化还原反应而难以制无水FeCl3。丙同学设计了如下实验方案验证自己的观点:
取少量FeCl3·6H2O于试管中,加入过量SOCl2,振荡使两种物质充分反应;再往试管中加水溶解,加入___,证明该过程发生了氧化还原反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在常温下,有下列五种溶液:
①0.1mol/LNH4Cl②0.1mol/LCH3COONH4③0.1mol/LNH4HSO4
④0.1mol/LNH4HCO3 ⑤0.1mol/LNaHCO3
请根据要求填写下列空白:
(1)溶液①呈 ______ 性(填“酸”、“碱”或“中”),其原因是: ______ (用离子方程式表示)
(2)溶液⑤呈 ______ 性(填“酸”、“碱”或“中”),其原因是: ______ (用离子方程式表示)
(3)比较溶液①、③中c(NH4+)的大小关系是① ______ ③(填“>”、“<”或“=”)
(4)常温下,测得溶液②的pH=7,则CH3COO-的水解程度 ______ NH4+的水解程度(填“>”、“<”或“=”),CH3COO-与NH4+浓度的大小关系是:c(CH3COO-)_____c(NH4+)(填“>”、“<”或“=”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中,错误的是 ( )
A.配制 5%食盐溶液时,称量 5g 食盐放入烧杯中加入 95g 水搅拌溶解
B.胆矾晶体结晶水含量测定时,需用小火缓慢加热,防止晶体飞溅
C.测定未知 NaOH 溶液浓度时,红色手柄滴定管需用标准酸液润洗 2﹣3 次
D.配制 0.1 mol/L 的 H2SO4 溶液时,将量取的浓 H2SO4 放入容量瓶中加水稀释
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 K2FeO4 溶于水后,会水解生成多种微粒。下图是0.10 mol·L1 K2FeO4 溶液中各含铁微粒随溶液 pH 的变化图,纵坐标表示其个数百分含量,则下列说法不正确的是
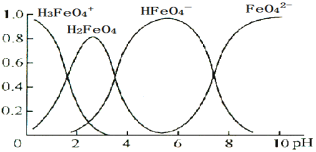
A.K2FeO4 溶于水呈碱性B.![]() 水解强于电离
水解强于电离
C.H2FeO4 既能和强碱反应又能和强酸反应D.0.10 mol·L1 的 K2FeO4 的 pH 近似等于 10
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.由三种常见元素组成的化合物A,按如下流程进行实验。气体B、C、D均无色、无臭,B、D是纯净物;浓硫酸增重3.60g,碱石灰增重17.60g;溶液F焰色反应呈黄色。
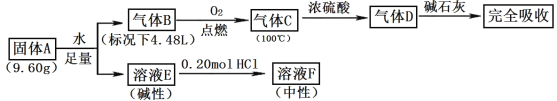
请回答:
(1)组成A的非金属元素是_____,气体B的结构简式_____。
(2)固体A与足量水反应的化学方程式是_____。
(3)一定条件下,气体D可能和FeO发生氧化还原反应,试写出一个可能的化学方程式_____。
Ⅱ.某兴趣小组为验证卤素单质的氧化性强弱,向NaBr溶液中通入一定量Cl2,将少量分液漏斗中溶液滴入试管中,取试管振荡,静止后观察现象。实验装置如图:
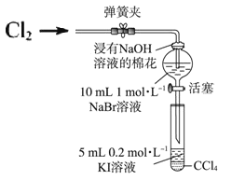
(4)说明氧化性 Br2>I2 的实验现象是_____。
(5)为了排除Cl2对溴置换碘实验的干扰,需确认分液漏斗中通入Cl2 未过量。试设计简单实验方案检____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)有相同温度和压强下的两种气体12C18O和14N2,若两种气体的质量相同,则两种气体所含的质子数之比为__________,若两种气体的原子数相等,则两种气体所含中子数之比_________,若两种气体的体积相同,则两种气体的密度之比为_________。
(2)10.8 g R2O5中氧原子的数目为3.01×1023,则元素R的相对原子质量为 ________。
(3)将10 mL1.00 mol/L Na2CO3溶液与10 mL1.00 mol/L CaCl2溶液相混和,则混和溶液中Na+的物质的量浓度为___________(忽略混合前后溶液体积的变化)。
(4)在标准状况下,由CO和CO2组成的混合气体为6.72 L,质量为12 g,此混合物中CO和CO2物质的量之比是_________。
(5)在空气中煅烧CoC2O4生成钴的氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为1.344L(标准状况),则钴氧化物的化学式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式的书写正确的是( )
A. H2SO4溶液与Ba(OH)2溶液反应:Ba2++OH﹣+H++![]() →BaSO4↓+H2O
→BaSO4↓+H2O
B. 将Na投入到CuSO4溶液中:2Na+Cu2+===2Na++Cu↓
C. 大理石溶于醋酸中:CaCO3+2CH3COOH===Ca2++2CH3COO﹣+CO2↑+H2O
D. 将Cl2通入水中:Cl2+H2O===2H++Cl﹣+ClO﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com