
【题目】用质量分数为98%,密度为1.84 g·cm-3的浓硫酸配制1 mol/L稀硫酸100 mL,其操作有以下各步:
①用量筒量取一定体积的浓硫酸
②洗涤烧杯和玻璃棒2~3次,将洗涤液转入容量瓶中
③将稀释、冷却后的硫酸转入容量瓶中
④将浓硫酸倒入盛有水的烧杯中稀释、冷却
⑤加水至液面接近刻度线1~2 cm处,定容,摇匀
完成下列填空:
(1)第①步操作中应用量筒量取__________mL浓硫酸;应选择_________mL量筒(填5、10 或 50)。
(2)本实验用到的仪器己有烧杯、量筒、玻璃棒,还缺少的仪器是___________。
(3)正确的操作顺序是_________________(用序号填写)。
(4)下列操作会对所配溶液浓度产生什么影响(填“偏高”、“偏低”或“无影响”)
①转移浓硫酸后,小烧杯未洗涤:_______________;
②量取浓硫酸的量筒用蒸馏水洗涤两次,并将洗涤液转入容量瓶中:________________;
③定容时俯视容量瓶刻度线:________________;
④使用前容量瓶未干燥:_________________。
【答案】 5.4 10 100 mL容量瓶、胶头滴管 ①④③②⑤ 偏低 偏高 偏高 无影响
【解析】(1)根据![]() 可知浓硫酸的浓度是
可知浓硫酸的浓度是![]() mol/L=18.4mol/L,因此第①步操作中应用量筒量取浓硫酸的体积为
mol/L=18.4mol/L,因此第①步操作中应用量筒量取浓硫酸的体积为![]() ,所以应选择10mL量筒。(2)本实验用到的仪器己有烧杯、量筒、玻璃棒,还缺少的仪器是100 mL容量瓶、胶头滴管。(3)配制一定物质的量浓度溶液的一般步骤是计算、量取、稀释、冷却、转移、洗涤、摇匀、定容等,所以正确的操作顺序是①④③②⑤。(4)①转移浓硫酸后,小烧杯未洗涤,溶质的物质的量减少,浓度偏低;②量取浓硫酸的量筒用蒸馏水洗涤两次,并将洗涤液转入容量瓶中,溶质的物质的量增加,浓度偏高;③定容时俯视容量瓶刻度线,液面在刻度线下方,体积减少,浓度偏高;④使用前容量瓶未干燥不影响。
,所以应选择10mL量筒。(2)本实验用到的仪器己有烧杯、量筒、玻璃棒,还缺少的仪器是100 mL容量瓶、胶头滴管。(3)配制一定物质的量浓度溶液的一般步骤是计算、量取、稀释、冷却、转移、洗涤、摇匀、定容等,所以正确的操作顺序是①④③②⑤。(4)①转移浓硫酸后,小烧杯未洗涤,溶质的物质的量减少,浓度偏低;②量取浓硫酸的量筒用蒸馏水洗涤两次,并将洗涤液转入容量瓶中,溶质的物质的量增加,浓度偏高;③定容时俯视容量瓶刻度线,液面在刻度线下方,体积减少,浓度偏高;④使用前容量瓶未干燥不影响。


科目:高中化学 来源: 题型:
【题目】为了测定某铁碳合金中铁的质量分数,某化学兴趣小组设计了图示实验装置。

(1)写出碳与浓硫酸反应的化学方程式_____________。
(2)C中品红溶液的作用_____________。
(3)该小组同学设计的实验装置存在缺陷,下列因素可能导致铁的质量分数测量值偏高的是_____________。
A. A中反应不完全
B. E 中碱石灰吸收空气中的CO2和H2O
C.反应生成的SO2部分被E 中碱石灰吸收
D.反应完全后,还有CO2气体滞留在装置体系中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种物质都含有一种共同的元素,A是常见的金属,C的水溶液呈现黄色,A、B、C、D之间有如图所示转化关系。

(1)A是________________(填写相关物质的化学式);
(2)C溶液与NaOH溶液混合后产生的现象____________________;
(3)①的反应类型:______(选填“化合”、“分解”、“置换”、“复分解”) ;
(4)某待测液中既有B中阳离子,又有C中阳离子。
检验待测液中有C中阳离子的方法:___________________________;
检验待测液中有B中阳离子的方法:__________________________;
(5)写出D![]() E的反应方程式:______________________。
E的反应方程式:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学帮助水质检测站配制490 mL 0.5 mol L-1NaOH溶液以备使用。
(1)该同学应选择_____mL的容量瓶。
(2)应用托盘天平准确称量_______g NaOH固体。
(3)配制过程如图乙所示,则图甲操作应在图乙中的______ (填字母)之间。
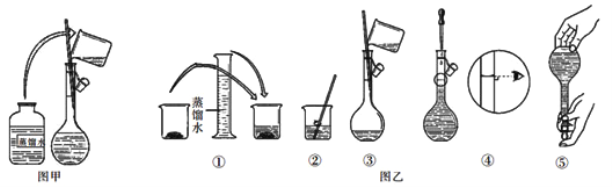
A.①与② B.②与③ C.③与④
(4)若在配制过程中出现下列情况,会使所配制NaOH溶液的浓度偏低的是______(填字母)。
A.转移溶液后,未洗涤烧杯和玻璃棒就直接定容
B.定容时俯视
C.配制溶液所用的容量瓶洗净后没有烘干
D.NaOH固体在烧杯中溶解后,立即将溶液转移到容量瓶内,并接着进行后续操作
E.定容摇匀后,发现液面低于刻度线,再加入蒸馏水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应既属于离子反应又属于氧化还原反应且反应过程中会放出热量的是( )
A. 甲烷在氧气中的燃烧反应 B. Ba(OH)2·8H2O晶体与NH4Cl晶体的反应
C. 灼热的碳与二氧化碳的反应 D. 钠与水的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】①热分解法、②热还原法、③电解法是工业上制取金属的三种常用方法。下列金属与冶炼方法相对应的是( )
A. Al、Na—③ B. Ca、Cu—② C. Fe、Mg—③ D. Al、Hg—①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】填空:
(1)碱金属元素原子最外层的电子都是________个,在化学反应中它们容易失去________个电子。
(2)碱金属元素中还原性最强的是________,原子半径最小的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于钠的说法正确的是:
A. 4.6g钠溶于水所得溶液中.要使100个水分子溶有1个钠离子,需要水的质量是360g
B. 根据金属间置换的原理,把一小粒金属钠放入硫酸铜溶液中,可以生成金属铜
C. 当钠、钾等金属不慎着火时,可以用沙子扑灭、水浇灭等方法
D. 少量的金属钠长期暴露在空气中,它的最终产物是Na2CO3而不是NaHCO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com