
 ,过氧化钠中含离子键和O-O非极性共价键,
,过氧化钠中含离子键和O-O非极性共价键, ;AC;
;AC;| 2.7g |
| 18g/mol |
| 2.24L |
| 22.4L/mol |
| 0.8g |
| 16g/mol |
| 2.3g |
| 46g/mol |
| 68.35kJ |
| 0.05mol |


 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源: 题型:
| A、0.9mol/L |
| B、0.45m01/L |
| C、0.25mol/L |
| D、0.225mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 充电 |
| 放电 |
| A、放电时的负极反应为Li-e-=Li+ |
| B、若用该电池电解水,阴极生成3.52gO2,则该电池负极质量减少0.77g |
| C、锂离子电池充电时的阴极反应为Si+4.4e-+4.4Li+=Li4.4Si |
| D、放电时电解质LiPF6水溶液中的Li+移向正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
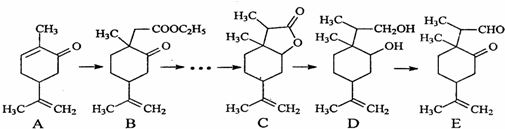
| CH3I |
| 催化剂 |
| LiBH4 |
| THF |
| LiBH4 |
| THF |
| HBr |
| NaOH溶液 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| D | ||
| A | B | C |
| E |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.4g | B、0.8g |
| C、0.01g | D、0.02g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com