
【题目】把下列4种溶液,分别加入到4支装有形状大小相同的锌粒的试管中充分反应,其中产生H2的速率最大的是 ( )
A. 40 mL,5 mol·L-1的盐酸
B. 60 mL,6 mol·L-1的硝酸
C. 15 mL,4 mol·L-1的硫酸
D. 40mL,18 mol·L-1的硫酸
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】向平底烧瓶中放入氢氧化钡晶体[Ba(OH)2·8H2O]和氯化铵晶体,塞紧瓶塞。在瓶底和木板间滴少量水(如图所示)。一段时间后,发现瓶内固态物质变稀,有液体生成,瓶壁变冷,小木板黏结在烧瓶底部。这时打开瓶塞,烧瓶中散发出刺鼻的气味。

(1)下列有关该实验的结论正确的是 (填字母)。
A.自发反应一定是放热反应
B.自发反应一定是吸热反应
C.有的吸热反应也能自发进行
D.吸热反应不能自发进行
(2)发生反应的化学方程式为 。
(3)从化学反应进行方向的角度解释上述现象: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一个简易测量物质反应是吸热还是放热的实验装置。将镁片加入小试管内,然后注入足量的盐酸。

请根据要求回答下列问题:
(1)有关反应的离子方程式是__________________________________。
(2)试管中观察到的现象是__________________________________。
(3)U形管中左端液面 (填“上升”或“下降”),原因是________________________________,说明此反应是______(填“放热”或“吸热”)反应。
(4)由实验推知,MgCl2和H2的总能量____________(填“大于”、“小于”或“等于”)镁片和盐酸的总能量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把500 mL含有BaCl2和KCl的混合溶液分成5等份,取一份加入含a mol硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含bmol硝酸银的溶液,恰好使氯离子完全沉淀。则该混合溶液中钾离子浓度为 ( )
A. 0.1(b-2a)mol·L-1 B. 10(2a-b) mol·L-1
C. 10(b-2a) mol·L-1 D. 10(b-a) mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知还原性Cl-<Fe2+<H2O2<I-<SO2,下列反应不能发生的是
A. 2Fe3++SO2+2H2O===SO42-+4H++2Fe2+
B. I2+SO2+2H2O===H2SO4+2HI
C. H2O2+2H++SO42-===SO2↑+O2↑+2H2O
D. Cl2+2Fe2+===2Fe3++2Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1997年,第一只“克隆羊”在英国诞生,“克隆羊”的关键技术之一是找到一些特殊的酶,它们能激活普通体细胞,使之像生殖细胞一样发育成个体。下列有关酶的叙述错误的是
A.酶是具有催化功能的蛋白质
B.酶的催化作用具有选择性和专一性
C.酶通常在强酸或强碱条件下发挥作用
D.高温或紫外线照射会降低酶的活性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄糖是人体所需能量的重要来源之一。葡萄糖燃烧的热化学方程式为:
C6H12O6(s)+6O2(g) ![]() 6CO2(g)+6H2O(l) ΔH=2800 kJ mol1
6CO2(g)+6H2O(l) ΔH=2800 kJ mol1
葡萄糖在人体组织中氧化的热化学方程式与它燃烧的热化学方程式相同。计算:
(1)100 g葡萄糖在人体内完全氧化时所产生的热量为_______________。
(2)人的体温一般要保持在36.5°C,低于此温度则要“打寒战”,并靠消耗葡萄糖释放出的能量来维持体温,与此同时有一部分能量转化为ATP。若形成 1 mol ATP需消耗10.75 g葡萄糖,则“打寒战”时会有________ %的能量转化成热量。(已知形成1 mol ATP需消耗75.24 kJ的能量)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种粒子之间有如图所示关系,根据图示转化关系推测下列说法不正确的是

A. 可用KI淀粉试纸和食醋检验加碘盐中是否含有碘
B. 足量Cl2能使湿润的KI淀粉试纸变白的原因可能是5Cl2+I2+6H2O==2HIO3+10HCl
C. 由图可知氧化性的强弱顺序为Cl2>I2>IO3-
D. 途径Ⅱ中若生成1 mol I2,反应中转移的电子数为10NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组构想将汽车尾气(NO、NO2)转化为重要的化工原料HNO3,其原理如图所示,其中A、B为多孔材料。下列说法正确的是( )
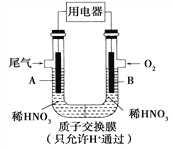
A. 电解质溶液中电流的方向由B到A,电子的流向与之相反
B. 电极A表面反应之一为NO-3e-+2H2O===NO![]() +4H+
+4H+
C. 电极B附近的c(NO![]() )增大
)增大
D. 该电池工作时,每转移4 mol电子,生成22.4 L O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com