
【题目】下表是![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 五种短周期元素的某些性质:
五种短周期元素的某些性质:
元素 | A | B | C | D | E |
最低负化合价 |
|
|
|
|
|
电负性 | 2.55 | 2.58 | 3.16 | 3.44 | 3.98 |
下列判断正确的是( )
A.![]() 、
、![]() 、
、![]() 的简单氢化物的稳定性:
的简单氢化物的稳定性:![]()
![]() 元素原子的最外层原子轨道中无自旋状态相同的电子
元素原子的最外层原子轨道中无自旋状态相同的电子
C.![]() 元素与
元素与![]() 元素不可能形成化合物
元素不可能形成化合物
D.与![]() 元素同周期的第一电离能最小的元素的单质能与
元素同周期的第一电离能最小的元素的单质能与![]() 发生置换反应
发生置换反应
【答案】D
【解析】
A、B、C、D、E五种短周期元素,根据元素化合价知,A属于第ⅣA族,B、D属于第ⅥA族,C、E属于第VⅡA族,B的电负性小于D,所以D是O元素,B是S元素;C的电负性小于E,所以C是Cl元素,E是F元素,硅的电负性小于S,A的电负性接近S元素,所以A是C元素,结合物质的结构、性质解答。
由以上分析可知A为C元素,B为S元素,C为Cl元素,D为O元素,E为F元素。
A. 非金属性F>O>Cl,元素的非金属性越强,对应的氢化物越稳定,故A错误;
B. A为C元素,价层电子为2s22p2,p轨道有2个电子,自旋状态相同,故B错误;
C. 元素B、C之间可形成化合物S2Cl2等,故C错误;
D. 与元素B同周期且第一电离能最小的元素的单质Na为活泼金属,能与H2O发生置换反应生成氢气,故D正确;
答案选D。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】恒温恒容下,向2L密闭容器中加入MgSO4(s)和CO(g),发生反应:MgSO4(s)+CO(g)MgO(s)+CO2(g)+SO2(g)反应过程中测定的部分数据见下表:
反应时间/min | n(MgSO4)/mol | n(CO)/mol | n(CO2)/mol |
0 | 2.00 | 2.00 | 0 |
2 | 0.80 | ||
4 | 1.20 |
下列说法正确的是( )
A.反应在0~2min内的平均速率为v(SO2)=0.6molL-1min-1
B.反应在2~4min内容器内气体的密度没有变化
C.若升高温度,反应的平衡常数变为1.00,则正反应为放热反应
D.保持其他条件不变,起始时向容器中充入1.00molMgSO4和1.00molCO,到达平衡时n(CO2)<0.60mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)NiO(氧化镍)晶体的结构与NaCl相同,Ni2+与最邻近O2-的核间距离为a×10-8cm,计算NiO晶体的密度____________________。(已知NiO的摩尔质量为74.7gmol-1)
(2)天然的和绝大部分人工制备的晶体都存在各种缺陷。例如:在某种NiO晶体中就存在如下图所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代,其结果晶体仍呈电中性,但化合物中Ni和O的比值却发生了变化。某氧化镍样品组成为Ni0.97O,试计算该晶体中Ni3+与Ni2+的离子数之比____________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次增大,X、Y和Z组成的一种化合物可有效灭杀新型冠状病毒,它的结构式为: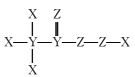 。向W的一种钠盐水溶液中通入YZ2气体,产生沉淀的质量m与通入YZ2气体的体积V的关系如图所示。下列说法正确的是
。向W的一种钠盐水溶液中通入YZ2气体,产生沉淀的质量m与通入YZ2气体的体积V的关系如图所示。下列说法正确的是
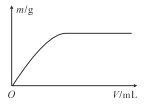
A.氢化物的熔点一定是:Y<Z
B.最高价氧化物对应水化物的酸性:Y>W
C.X、Y、Z三种元素只能组成一种化合物
D.工业上常用热还原法冶炼单质W
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜及其化合物在生产、生活中有广泛应用。回答下列问题:
(1)铜和锌相邻,铜和锌的几种状态:①铜:[Ar]3d10;②铜:[Ar]3d104s1③铜:[Ar]3d104p1④锌:[Ar]3d104s1⑤锌:[Ar]3d104s2。它们都失去1个电子时需要的能量由大到小排序为 ___(填字母)。
a.①⑤④②③ b.①④⑤②③ c.②①③⑤④ d.⑤①④③②
画出基态铜原子的价电子排布图____。
(2)Cu2+与NH3·H2O等形成配离子。[Cu(NH3)4]2+中2个NH3被2个H2O取代得到两种结构的配离子,则[Cu(NH3)4]2+的空间构型是____(填“正四面体”或“正四边形”)。
(3)CuF2晶体的熔点为836℃。其能量循环图示如下(a、b、c 等均大于0):

F-F键能为 ___kJmol-1,CuF2(s)的晶格能为 ___kJmol-1。
(4)铜常作醇氧化反应的催化剂。M中C原子的杂化类型有 ___种,M的熔沸点比N的高,原因是 ___。
![]()
![]()
![]()
(5)磷青铜晶胞结构如图所示。NA代表阿伏加德罗常数的值,铜、磷原子最近距离为![]()
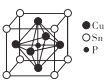
①铜与铜原子最近距离为____nm。
②磷青铜晶体密度为___ gcm-3(用代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A.28g晶体硅中含有NA个Si-Si键
B.叠氮化铵(NH4N3)发生爆炸反应:NH4N3=2N2![]() +2H2
+2H2![]() ,当产生标准状况下22.4L气体时,转移电子的数目为NA
,当产生标准状况下22.4L气体时,转移电子的数目为NA
C.pH=1的H3PO4溶液中所含H+的数目为0.1NA
D.200mL1mol/LAl2(SO4)3溶液中A13+和SO42-的数目总和是NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用草酸“沉钴”,再过滤草酸钴得到的母液A经分析主要含有下列成分:
H2C2O4 | Co2+ | Cl- | |
质量浓度 | 20.0g/L | 1.18g/L | 2.13g/L |
为了有效除去母液A中残留的大量草酸,一般用氯气氧化处理草酸,装置如下:
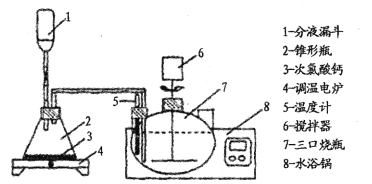
回答下列问题:
(1)母液A中c(CoO2)为____mol·L-1。 ,
(2)分液漏斗中装入盐酸,写出制取氯气的离子方程式 ____________。反应后期使用调温电炉加热,当锥形瓶中____(填现象)时停止加热。
(3)三颈烧瓶反应温度为50℃,水浴锅的温度应控制为 ____(填序号)。
A.50℃ B.5l-52℃ C.45 - 55℃ D.60℃
(4)氯气氧化草酸的化学方程式为________ 。
(5)搅拌器能加快草酸的去除速率,若搅拌速率过快则草酸去除率反而降低,主要原因是__________。
(6)若用草酸铵代替草酸“沉钴”,其优点是____ ,其主要缺点为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量纯净的 X 置于某 10 L 容积恒定的真空容器中(假设固体试样体积忽略不计),在恒定温度下使其达到分解平衡:X(s) ![]() 2Y(g)+Z(g),实验测得不同温度下的分解平衡常数列于下表,下列说法中不正确的是( )
2Y(g)+Z(g),实验测得不同温度下的分解平衡常数列于下表,下列说法中不正确的是( )
温度( oC) | 15.0 | 25.0 | 30.0 | 35.0 |
K/(×10-8 mol3·L-3) | 0.205 | 1.64 | 4.68 | 10.8 |
A.该反应在高温下可能自发
B.若Z的体积分数不再随时间变化时表示反应达平衡状态
C.若在恒温下,压缩容器体积,再次达平衡后,n(X)比原平衡大
D.35℃时,达平衡时,X分解了0.03 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】脱氢醋酸钠是FAO和WHO认可的一种安全型食品防霉、防腐保鲜剂,它是脱氢醋酸的钠盐。脱氢醋酸的一种制备方法如图:
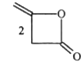 (a双乙烯酮)
(a双乙烯酮)![]()
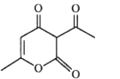 (b脱氢醋酸)
(b脱氢醋酸)
下列说法错误的是
A.a分子中所有原子处于同一平面B.a.b均能使酸性KMnO4溶液褪色
C.a、b均能与NaOH溶液发生反应D.b与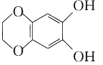 互为同分异构体
互为同分异构体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com