
【题目】可逆反应3H2+N2![]() 2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示,下列各关系中能说明反应已达到平衡状态的是( )
2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示,下列各关系中能说明反应已达到平衡状态的是( )
A.υ正(N2)=υ正(H2)B.υ正(N2)=υ逆(NH3)C.3υ正(H2)=2υ逆(NH3)D.3υ正(N2)=υ逆(H2)
【答案】D
【解析】
当υ正=υ逆时,反应达到平衡状态,据此判断。
A. 只有正反应速率,没有逆反应速率,不能确定υ正=υ逆,不能说明反应达到平衡状态;
B. 当υ正(N2)=υ逆(NH3)时,反应没有达到平衡状态;
C. 当3υ正(H2)=2υ逆(NH3)时,反应没有达到平衡状态;
D. 当3υ正(N2)=υ逆(H2)时,正反应速率等于逆反应速率,反应达到平衡状态;
答案选D。
化学反应 | mA(g)+nB(g) | 是否平衡 |
正、逆反 应速率之 间的关系 | ①单位时间内消耗了m mol A,同时也生成了m mol A | 平衡 |
②单位时间内消耗了n mol B,同时也消耗了p mol C | 平衡 | |
③v(A)∶v(B)∶v(C)∶v(D)=m∶n∶p∶q | 不一定平衡 | |
④单位时间内生成了n mol B,同时也消耗了q mol D | 不一定平衡 |


 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:
【题目】以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的工艺流程如下:
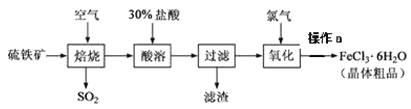
回答下列问题:
(1)在一定条件下,SO2转化为SO3的反应为2SO2+O2![]() 2SO3,该反应的平衡常数表达式为K=____;过量的SO2与NaOH溶液反应的化学方程式为_________________。
2SO3,该反应的平衡常数表达式为K=____;过量的SO2与NaOH溶液反应的化学方程式为_________________。
(2)用36.5%(密度为1.2g·㎝-3)的盐酸的配制500mL的30%(密度为1.095g·㎝-3的盐酸,所需玻璃仪器是 (___)
A.玻璃棒 B.烧杯 C.托盘天平 D.500mL量筒 E、500mL容量瓶 F、胶头滴管
(3)酸溶及后续过程中均需保持盐酸过量,其目的是________________________、
________________________________________________________。
(4)通氯气氧化时,发生的主要反应的离子方程式为_________________________;该过程产生的尾气可用碱溶液吸收,尾气中污染空气的气体为________________(写化学式)。
(5)操作a为_________________________、过滤、洗涤、干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)出的能量。已知白磷(P4)和P4O6的分子结构如图所示,
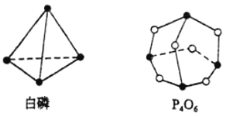
已知:
化学键 | P—P | P—O | O=O |
键能(kJ·mol1) | 198 | 360 | 498 |
则反应P4(g)+3O2(g)= P4O6(g)的△H=_________。
(2)已知①2C(s)+O2(g)=2CO(g) △H=-221.0kJ/mol
②2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ/mol
则制备水煤气的反应C(s)+H2O(g)=CO(g)+ H2(g)的△H=_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥中Cr(III)的处理工艺如下:

其中硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
(1)酸浸时,为了提高浸取率可采取的措施有___________、__________。
(2)H2O2的作用是将滤液Ⅰ中的Cr3+转化为Cr2O72-,写出此反应的离子方程式:___________。
(3)常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
阳离子 | Fe3+ | Mg2+ | Al3+ | Cr3+ |
开始沉淀时的pH | 2.7 | —— | —— | —— |
沉淀完全时的pH | 3.7 | 11.1 | 8 | 9(>9溶解) |
加入NaOH溶液使溶液呈碱性,Cr2O72-转化为CrO42-。滤液Ⅱ中阳离子主要有___________;但溶液的pH不能超过8,其理由是_____________________。
(4)钠离子交换树脂的反应原理为:Mn++nNaR→MRn+nNa+,利用钠离子交换树脂除去滤液Ⅱ中的金属阳离子是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气和燃煤尾气是造成空气污染的重要原因之一,治理汽车尾气和燃煤尾气是环境保护的重要课题。回答下列问题:
(1)在汽车排气系统中安装三元催化转化器,可发生反应:2NO(g)+2CO(g)![]() 2CO2(g)+N2(g)。在某密闭刚性容器中通入等量的CO和NO,发生上述反应时,c(CO)随温度(T)和时间(t)的变化曲线如图所示。
2CO2(g)+N2(g)。在某密闭刚性容器中通入等量的CO和NO,发生上述反应时,c(CO)随温度(T)和时间(t)的变化曲线如图所示。
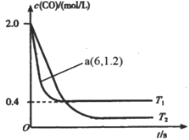
①据此判断该反应的正反应为________(填“放热”或“吸热”)反应。
②温度T1时,该反应的平衡常数K=_____;反应速率v=v正- v逆=k正c2(NO)c2(CO)-k逆c2(CO2)c(N2),k正、k逆分别为正、逆反应速率常数,计算a处![]() =________。
=________。
(2)SNCR-SCR脱硝技术是一种新型的除去烟气中氮氧化物的脱硝技术,一般采用氨气或尿素作还原剂,其基本流程如图:
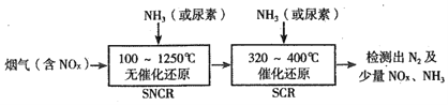
①SNCR-SCR脱硝技术中用NH3作还原剂还原NO的主要反应为4NH3(g)+4NO(g)+O2(g)=4N2(g)+6H2O(g),△H<0,则用尿素[CO(NH2)2]作还原剂还原NO2的化学方程式为______________。
②体系温度直接影响SNCR技术的脱硝效率,如图所示:

SNCR与SCR技术相比,SCR技术的反应温度不能太高,其原因是__________;当体系温度约为925℃时,SNCR脱硝效率最高,其可能的原因是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种物质的焰色反应都呈黄色,A、B分别与水反应都有气体放出,同时都生成C溶液,A与水反应放出的气体具有还原性,B与水反应放出的气体具有氧化性,C与适量的F气体反应生成D,D溶液与F气体反应生成E,E加热能够生成D和F气体。根据以上叙述回答下列问题:
(1)写出下列物质的化学式:B____,D____,E______。
(2)按要求完成方程式:
①加热E生成D和F的化学方程式____;
②C溶液和CO2反应生成D的离子方程式____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于放热反应:H2+Cl2![]() 2HCl,下列说法中正确的是( )
2HCl,下列说法中正确的是( )
A.断开1molH—H键和1molC1—C1键所吸收的总能量大于形成2molH—C1键所放出能量
B.产物所具有的总能量高于反应物所具有的总能量
C.反应物所具有的总能量高于产物所具有的总能量
D.该反应中,化学能只转变为热能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是 ![]()
A.某二元酸![]() 在水中的电离方程式是:
在水中的电离方程式是:![]() ,
,![]() ;则NaHA溶液中:
;则NaHA溶液中:![]()
B.相同温度下将足量氯化银固体分别放入相同体积的①蒸馏水、②![]() 盐酸、③
盐酸、③![]() 氯化镁溶液、④
氯化镁溶液、④![]() 硝酸银溶液中,
硝酸银溶液中,![]() 为①>④=②>③
为①>④=②>③
C.常温下,某溶液的![]() ,则该物质一定是酸或强酸弱碱盐
,则该物质一定是酸或强酸弱碱盐
D.若![]() 、
、![]() 、
、![]() 分别表示常温下
分别表示常温下![]() 的电离平衡常数、
的电离平衡常数、![]() 的水解平衡常数和水的离子积常数,则三者之间的关系为
的水解平衡常数和水的离子积常数,则三者之间的关系为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,实验测得1.0mol/L NH4HCO3 溶液pH=8.0。平衡时碳的分布系数(各含碳微粒的浓度占含碳各种微粒浓度之和的分数)与pH的关系如图所示。下列说法正确的是( )
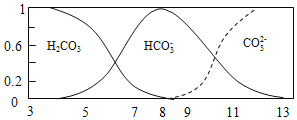
A. 常温下,Kb(NH3H2O)>Ka1(H2CO3)>Ka2(H2CO3)
B. pH=13时,溶液中不存在HCO3-的水解平衡
C. pH由8~11 时,随着pH值的增大,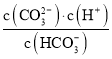 增大
增大
D. pH=3时,有c(NH4+)+c(NH3H2O)=c(HCO3-)+c(H2CO3)+c(CO32-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com