
【题目】欲制取较纯净的CH2ClCH2Cl(即1,2-二氯乙烷),可采取的方法是
A.乙烯与Cl2加成
B.乙烯与HCl加成
C.乙烷与Cl2按1∶2的体积比在光照条件下反应
D.乙烯先与HCl加成,再与等物质的量的Cl2在光照下反应
科目:高中化学 来源: 题型:
【题目】Ⅰ.现有各组物质:①O2和O3 ②![]() 和
和![]() ③
③![]() 和
和![]() ④
④![]() 和
和![]() ⑤
⑤  ⑥
⑥ ![]() 和质量数为238、中子数为146的原子 ⑦
和质量数为238、中子数为146的原子 ⑦![]()
请按要求用序号填空:
(1)属于同系物的是___________(2)属于同分异构体是_________(3)属于同位素的是_________(4)属于同素异形体的是________(5)属于同种物质的是___________
II.命名或写出结构简式:
(1) 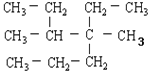 ________________________________
________________________________
(2)2-乙基-1-戊烯 _______________________________
(3)支链上只有一个乙基,且式量最小的烷烃 _________________
【答案】 ④ ⑦ ⑥ ① ⑤ 3,4﹣二甲基﹣4﹣乙基庚烷 CH2=C(CH2CH3)CH2CH2CH3 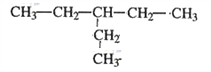
【解析】Ⅰ、同系物是指结构相似,组成上相差1个或者若干个CH2原子团的化合物。具有相同分子式而结构不同的化合物互为同分异构体;质子数相同质量数(或中子数)不同的原子互称同位素;同种元素形成的不同单质互为同素异形体;
①O2和O3是由氧元素组成的不同单质,互为同素异形体;②CH2=CH-CH3和CH2=CH-CH=CH2的结构不同,分子式也不同;③![]() 和
和![]() 分子式不同,结构也不同;④
分子式不同,结构也不同;④![]() 和
和![]() 的结构相似,组成上相差2个CH2,属于同系物;⑤
的结构相似,组成上相差2个CH2,属于同系物;⑤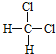 和
和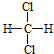 组成和结构都相同,为同一物质;⑥质量数为238,中子数为146的原子其质子数为238-146=92,与
组成和结构都相同,为同一物质;⑥质量数为238,中子数为146的原子其质子数为238-146=92,与![]() 的质子数相同,质量数(或中子数)不同,互称同位素;⑦C2H5C=C=CH2和CH3CH=CHCH=CH2具有相同分子式而结构不同,属于同分异构体。
的质子数相同,质量数(或中子数)不同,互称同位素;⑦C2H5C=C=CH2和CH3CH=CHCH=CH2具有相同分子式而结构不同,属于同分异构体。
故答案为:(1)④;(2)⑦;(3)⑥;(4)①;(5)⑤。
II、(1)烷烃命名时,选最长碳链为主链,从支链最近的一端进行编号;该物质最长碳链含有七个碳,2个-CH3分别在3、4号位,1个乙基在4号位,故命名为:3,4﹣二甲基﹣4﹣乙基庚烷;
(2)2-乙基-1-戊烯,含碳碳双键在内最长碳链有5个碳原子,离双键最近的一端编号,碳碳双键在1号碳,2号碳有一个乙基,据此写出结构简式:CH2=C(CH2CH3)CH2CH2CH3;
(3)支链的长度不能超过其所在位置两侧的主链的长度,烷烃中含有乙基,则乙基至少在3号位,所以只有一个乙基且式量最小的烷烃的结构简式为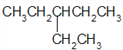 。
。
【题型】综合题
【结束】
24
【题目】(1)在25℃条件下将pH=11的氨水稀释100倍后溶液的pH为(填序号)____________。
A.9 B.13 C.11~13之间 D.9~11之间
(2)25℃时,向0.1mol/L的氨水中加入少量氯化铵固体,当固体溶解后,测得溶液pH减小,主要原因是(填序号)_____________________。
A.氨水与氯化铵发生化学反应
B.氯化铵溶液水解显酸性,增加了c(H+)
C.氯化铵溶于水,电离出大量铵离子,抑制了氨水的电离,使c(OH―)减小
(3)已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
A.c(Cl-)>c(NH4+)>c(H+)>c(OH-) B.c(Cl-)>c(NH4+)>c(OH-)>c(H+)
C.c(Cl-)>c(H+)>c(NH4+)>c(OH-) D.c(NH4+)>c(Cl-)>c(OH-)>c(H+)
①若溶液中只溶解了一种溶质,该溶质的名称是__________,上述离子浓度大小顺序关系中正确的是(选填序号)_________________________。
②若上述关系中C是正确的,则溶液中溶质的化学式是___________________________。
③若该溶液中由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)(填“>”、“<”、或“=”,下同)_____________c(NH3·H2O),混合后溶液中c(NH4+)与c(Cl-)的关系c(NH4+)____________c(Cl-)。
(4)室温下,如果将0.1mol NH4Cl和0.05mol NaOH全部溶于水,形成混合溶液(假设无损失),
①_______________和______________两种粒子的物质的量之和等于0.1mol。
②_______________和______________两种粒子的物质的量之和比OH―多0.05mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】部分弱酸的电离平衡常数如下表:
弱酸 | HCOOH | HCN | H2CO3 |
电离平衡常数(25℃) | Ka=1.77×10-4 | Ka=4.9×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
下列选项正确的是( )
A. 2CN-+H2O+CO2=2HCN+CO32-
B. 中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者大于后者
C. 物质的量浓度相等的HCOONa和KCN溶液中,c(Na+)-c(HCOO-)>c(K+)-c(CN-)
D. 浓度均为0.1 mol·L-1的①(NH4)2CO3、②(NH4)2SO4、③(NH4)2Fe(SO4)2溶液中,c(NH4+)的大小顺序为③>②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“纳米材料”是粒子直径为1~100nm(纳米)的材料,纳米碳就是其中的一种.若将纳米碳均匀地分散到蒸馏水中,所形成的物质 ①是溶液 ②是胶体 ③是浊液 ④不能透过滤纸 ⑤能透过滤纸 ⑥能产生丁达尔效应 ⑦静置后,会析出黑色沉淀( )
A.②⑤⑥
B.②⑥⑦
C.①⑤
D.③④⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把a、b、c、d四种金属片浸入稀硫酸中,用导线两两相连,可以形成原电池。若a、b相连时,a为负极;c、d相连时,c溶解;a、c相连时,c极上产生大量气泡;b、d相连时,b极上有大量气泡。则四种金属的活动性顺序是
A.a>c>d>bB.c>a>b>dC.a>c>b>dD.c>a>d>b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钠(Na2FeO4)是一种新型绿色水处理剂。工业上可用电解浓NaOH溶液制备Na2FeO4,其工作原理如右图所示,两端隔室中离子不能进入中间隔室。下列说法错误的是

A. 电解时,铜电极连接电源负极 B. 甲溶液可回用于该电解池
C. 离子交换膜a是阴离子交换膜 D. 阳极电极反应式:Fe-6e-+8OH-=FeO42-+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示。
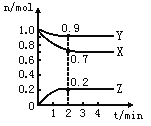
(1)由图中所给数据进行分析,该反应的化学方程式为__________。
(2)反应从开始至2分钟,用Z的浓度变化表示的平均反应速率为V(Z)= __________。
(3)2min反应达平衡,容器内混合气体的平均相对分子质量比起始时______(填增大、减小或不变);混合气体密度比起始时_______(填增大、减小或不变).
(4)将amolx与bmolY的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n(X)=n(Y)=n(Z),则原混合气体中a:b=__________。
(5)下列措施能加快反应速率的是_________。
A.恒压时充入He;B.恒容时充入He;C.恒容时充入X;D.及时分离出Z;E.升高温度; F.选择高效的催化剂
(6)下列说法正确的是__________。
A.升高温度改变化学反应的限度
B.已知正反应是吸热反应,升高温度平衡向右移动,正反应速率加快,逆反应速率减慢
C.化学反应的限度与时间长短无关
D.化学反应的限度是不可能改变的
E.增大Y的浓度,正反应速率加快,逆反应速率加快,正反应速率大于逆反应速率
F.加入高效催化剂可加快正、逆反应速率,化学平衡正向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去NaCl溶液中混有的Ca2+、Mg2+、SO42﹣、HCO3﹣等杂质,通常采用以下四种试剂:①Na2CO3 ②BaCl2 ③NaOH ④盐酸,加入试剂顺序合理的是( )
A.④②①③
B.①③②④
C.③②①④
D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】晶体硅是制备太阳能电池板的主要原料,电池板中还含有硼、氮、钛、钻、钙等多种化学物质。
请回答下列问题:
(1)第二周期元素的电负性按由小到大的顺序排列,B元素排在第__________位。
(2)硅酸根有多种结构形式,一种无限长链状结构如图1所示,其化学式为____________,Si原子的杂化类型为__________________。
(3)N元素位于元素周期表_____________区;基态N原子中,核外电子占据最高能级的电子云有____个伸展方向。
(4)[Co(NH3)6]3+的几何构型为正八面体形,Co在中心。
①[Co(NH3)6]3+中,1个Co提供_______________个空轨道。
②若将[Co(NH3)6]3+中的两个NH3分子换成两个Cl-,可以形成_________种不同的结构形式。
(5)—种由Ca、Ti、O三种元素形成的晶体的立方晶胞结构如图2所示。
①与Ti紧邻的Ca有___________________个。
②若Ca与O之间的最短距离为α pm,阿伏加德罗常数的值为NA,则晶体的密度ρ=__________________g· cm-3(用含α、NA的代数式表示)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com