
明矾石经处理后得到明矾[KAl(SO4)2·12H2O]。从明矾制备Al、K2SO4和H2SO4的工艺过程如下所示:
 焙烧明矾的化学方程式为:4KAl(SO4)2·12H2O+3S=2K2SO4+2Al2O3+9SO2↑+48H2O
焙烧明矾的化学方程式为:4KAl(SO4)2·12H2O+3S=2K2SO4+2Al2O3+9SO2↑+48H2O
请回答下列问题:
(1)在焙烧明矾的反应中,还原剂是________。
(2)从水浸后的滤液中得到K2SO4晶体的方法是________。

(3)Al2O3在一定条件下可制得AlN,其晶体结构如右图所示,该晶体中Al的配位数是________。
(4)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池反应的化学方程式是________。
(5)焙烧产生的SO2可用于制硫酸。已知25℃、101 kPa时:
2SO2(g)+O2(g) 2SO3(g) ΔH1=-197 kJ/mol;
2SO3(g) ΔH1=-197 kJ/mol;
H2O(g)=H2O(l) ΔH2=-44 kJ/mol;
2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l) ΔH3=-545 kJ/mol。
则SO3(g)与H2O(l)反应的热化学方程式是________。焙烧948 t明矾(M=474 g/mol),若SO2的利用率为96%,可生产质量分数为98%的硫酸________t。
(1)S(硫) (2)蒸发结晶 (3)4
(4)Al+3NiO(OH)+NaOH+H2O=NaAlO2+3Ni(OH)2
(5)SO3(g)+H2O(l)=H2SO4(l) ΔH=-130 kJ/mol 432
【解析】 结合流程图,根据物质的溶解性去分析解决问题。(1)根据焙烧明矾的化学方程式中各元素的化合价可知,明矾中部分硫元素的化合价降低,而硫单质在反应中元素的化合价升高,故还原剂为单质硫。(2)从滤液中得到晶体的方法为蒸发结晶。(3)由图中的晶体结构可以看出每个Al原子的周围距离相等且最近的N原子有4个,故其配位数为4。(4)放电时Al作负极,失电子被氧化,NiO(OH)在正极得电子,反应的方程式为Al+3NiO(OH)+NaOH+H2O=NaAlO2+3Ni(OH)2。(5)给题中的三个热化学方程式分别编号为①、②、③,根据盖斯定律由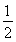 (③-①)-②可得到目标热化学方程式;设可生成硫酸的质量为x吨,据题意列式得到
(③-①)-②可得到目标热化学方程式;设可生成硫酸的质量为x吨,据题意列式得到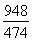 ×
×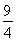 ×96%=
×96%=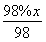 ,故x=432。
,故x=432。
点拨:知识:氧化还原反应、实验基本操作、原子配位数、原电池电池反应方程式、热化学方程式。能力:考查考生框图推断能力、读图识图分析图像能力、知识应用能力。试题难度:较大。


科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 物质结构与性质练习卷(解析版) 题型:选择题
我国科学家研制出一种催化剂,能在室温下高效催化空气中甲醛的氧化,其反应如下:HCHO+O2 CO2+H2O。下列有关说法正确的是( )
CO2+H2O。下列有关说法正确的是( )
A.该反应为吸热反应
B.CO2分子中的化学键为非极性键
C.HCHO分子中既含σ键又含π键
D.每生成1.8 g H2O消耗2.24 L O2
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 有机化学基础练习卷(解析版) 题型:填空题
华法林是一种治疗心脑血管疾病的药物,可由化合物E和M在一定条件下合成得到(部分反应条件略)。

(1)A的名称为________,A→B的反应类型为________。
(2)D→E的反应中,加入的化合物X与新制Cu(OH)2反应产生红色沉淀的化学方程式为________。
(3)G→J为取代反应,其另一产物分子中的官能团是________。
(4)L的同分异构体Q是芳香酸,Q R(C8H7O2Cl)
R(C8H7O2Cl)  S
S  T,T的核磁共振氢谱只有两组峰,Q的结构简式为________,R→S的化学方程式为________。
T,T的核磁共振氢谱只有两组峰,Q的结构简式为________,R→S的化学方程式为________。
(5)题图中,能缩合成体型高分子化合物的酚类单体是________。
(6)已知:L→M的原理为:
①
②
则M的结构简式为_________________
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 常见无机物及其应用练习卷(解析版) 题型:实验题
某化学兴趣小组以木炭和浓硝酸为起始原料,探究一氧化氮与过氧化钠反应制备亚硝酸钠。设计装置如下(忽略装置中空气的影响),请回答下列问题:

(1)组装好仪器后,必须进行的一项操作是_________________。
(2)装置A的试管中发生反应的化学方程式是_______________。
(3)推测B中可以观察到的主要现象是________;C装置的作用是________。
(4)装置D中除生成NaNO2外,还有另一种固态物质Y,Y的化学式是________;可以通过适当改进,不产生Y物质,请你提出改进方法:______________________。
(5)已知:亚硝酸是弱酸,不稳定,室温下存在反应3HNO2=HNO3+2NO↑+H2O;在酸性溶液中,NO2-可将MnO4-还原为Mn2+且无气体生成。
①写出检验D中产物是亚硝酸钠的方法:_________________;
②E装置中试剂X可以是________。
A.稀硫酸 B.酸性高锰酸钾溶液
C.稀硝酸 D.水
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 常见无机物及其应用练习卷(解析版) 题型:选择题
下列说法正确的是( )
A.Na2O2可用为潜艇工作人员的供氧剂
B.常温下铝箔放在浓HNO3中,生成H2
C.水蒸气通过炽热的铁,生成Fe(OH)3和H2
D.用新制Cu(OH)2检查尿糖,Cu(OH)2是还原剂
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 化工生产流程、无机物的判断练习卷(解析版) 题型:选择题
物质X、Y、Z均含有同一种元素,其转化关系如图所示。下列物质X和试剂M的组合不可能是( )

ABCD
X的化学式Na2OAlMgSO2
试剂M水NaOH溶液稀硫酸NaOH溶液
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 化学能与热能练习卷(解析版) 题型:选择题
已知下列热化学方程式:
Na+(g)+Cl-(g)=NaCl(s) ΔH
Na(s)+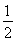 Cl2(g)=NaCl(s) ΔH1
Cl2(g)=NaCl(s) ΔH1
Na(s)=Na(g) ΔH2,Na(g)-e-=Na+(g) ΔH3
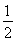 Cl2(g)=Cl(g) ΔH4,Cl(g)+e-=Cl-(g) ΔH5
Cl2(g)=Cl(g) ΔH4,Cl(g)+e-=Cl-(g) ΔH5
则ΔH与ΔH1、ΔH2、ΔH3、ΔH4、ΔH5的关系正确的是( )
A.ΔH=ΔH1+ΔH2+ΔH3+ΔH4+ΔH5
B.ΔH=ΔH1-ΔH2-ΔH3-ΔH4-ΔH5
C.ΔH=ΔH1-ΔH2+ΔH3-ΔH4+ΔH5
D.ΔH=ΔH2+ΔH3+ΔH4+ΔH5-ΔH1
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 化学实验基础练习卷(解析版) 题型:选择题
用下列实验装置进行的实验中,能达到相应实验目的的是( )

A.装置甲:为防止铁钉生锈
B.装置乙:除去一氧化碳中混有的乙烯
C.装置丙:验证HCl气体在水中的溶解性
D.装置丁:实验室制取乙酸乙酯
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 化学基本概念练习卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.使甲基橙变红色的溶液:Mg2+、K+、SO42—、NO3—
B.使酚酞变红色的溶液:Na+、Cu2+、HCO3—、NO3—
C.0.1 mol·L-1 AgNO3溶液:H+、K+、SO42—、I-
D.0.1 mol·L-1 NaAlO2溶液:H+、Na+、Cl-、SO42—
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com