
【题目】中国科学院大连化物所的研究团队创新性提出锌碘单液流电池的概念, 实现锌碘单液流中电解液的利用率近 100%, 其原理如图所示。
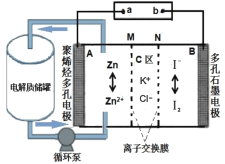
下列说法正确的是
A.放电时A电极反应式为:Zn+2e-=Zn2+B.放电时电解质储罐中离子总浓度减小
C.M为阴离子交换膜,N为阳离子交换膜D.充电时A极增重65g,C区增加离子数为2NA
【答案】C
【解析】
A. 放电时,B电极为正极,I2得到电子生成I,电极反应式为I2+2e=2I,A电极是负极,电极反应式为Zn2e═Zn2+,故A错误;
B. 放电时,左侧即负极,电极反应式为Zn2e═Zn2+,右侧是正极,电极反应式为I2+2e=2I,所以储罐中的离子总浓度增大,故B错误;
C. 离子交换膜是防止正负极I2、Zn接触发生自发电,负极区生成Zn2+,正电荷增加,正极区生成I,负电荷增加,所以Cl通过M膜进入负极,K+通过N膜进入正极,所以M为阴离子交换膜,N为阳离子交换膜,故C正确;
D. 充电时,A极反应式Zn2e═Zn2+,A极增重65g转移2mol电子,所以C区增加2molK+、2molCl,离子总数为4NA,故D错误;
故选:C。


 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:
【题目】下列有关化学用语表示正确的是( )
A.CH3CH(OH)CH(CH3)CH3的系统命名为2—羟基—3—甲基丁烷
B.用电子式表示二氧化碳的形成过程:![]()
C.聚氯乙烯的链节:—CH2—CHCl—
D.甲醇和氧气设计成燃料电池,两极均以石墨为电极,K2CO3溶液为电解质,则负极电极反应式为:CH3OH+8OH--6e-=CO![]() +6H2O
+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近我国科学家研制出一种高分子大规模储能二次电池,其示意图如下所示。这种电池具有寿命长、安全可靠等优点,下列说法错误的是
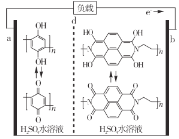
A.硫酸水溶液主要作用是增强导电性
B.充电时,电极b接正极
C.d膜是质子交换膜
D.充放电时,a极有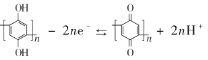
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黑磷是磷的一种稳定的同素异形体,黑磷具有正交晶系的晶体结构(图A),晶胞参数a=3.310A,b=4.380A,c=10.500A。黑磷烯是二维的单层黑磷(图B),黑磷烯与石墨烯结构相似,P的配位数为3。与石墨烯相比,黑磷烯具有半导体性质,更适合于制作电子器件。已知黑磷结构中只有一种等效的三配位P,所有P原子的成键环境一样,图A中编号为①的P原子的晶胞内坐标为(0.50,0.090,0.598)。请回答下列问题:
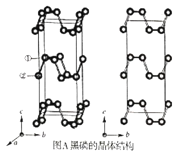
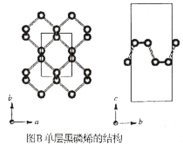
(1)写出P原子的价电子排布:___。
(2)P和F的电负性大小顺序是X(P)___X(F)。(填“<”“=”或“>”)P和F形成的分子PF3和PF5,它们的几何构型分别为__、__。
(3)①黑磷中P原子杂化类型是__。黑磷中不存在__(选填字母序号)。
A.共价键 B.σ键 C.π键 D.范德华力
②红磷、白磷与黑磷熔点从高到低的顺序为__,原因是__。
(4)图A中编号为②的P原子的晶胞内坐标为__,黑磷的晶胞中含有__个P原子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组利用某酸性腐蚀废液(含Fe3+、Cu2+、NH4-、SO42-),制取铵明矾[NH4Al(SO4)2·12H2O]的流程如下:
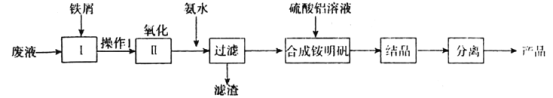
回答下列问题:
(1)加入铁屑的目的是______________________。
(2)第II步中用双氧水作为氧化剂。请写出步骤II氧化反应离子方程式__________________。
(3)检验溶液中含有NH4+的方法是______________________。
(4)工业上将流程中产生的滤渣用NaClO碱性溶液氧化可生成一种高效净水剂(Na2FeO4),写出对应的离子方程式:_________________________________。
(5)固体铵明矾加热过程中,固体质量随温度的变化如图所示。
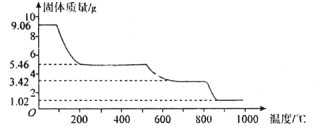
若将铵明矾加热灼烧,400℃时剩余固体成分的化学式为___________。在温度从800℃到950℃的过程中得到的两种氧化物,一种为固体,一种为氧化性气体,该气体的名称是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三明清流“天芳悦潭”温泉富含珍稀“锗”元素。其中锗石含有人体所需的硒、锌、镍、钴、锰、镁、钙等30多种对人体有益的微量元素。
回答下列问题:
(1)基态Ge原子价电子排布图为_______,Ge原子的电子发生跃迁时会吸收或发出不同的光,可用光谱分析仪获得______光谱(填“连续”或 “线状”),鉴定Ge元素的存在。
(2)锗与碳同族,性质和结构有一定的相似性,锗元素能形成无机化合物(如锗酸钠:Na2GeO3;二锗酸钠:Na2Ge2O5等),也能形成类似于烷烃的锗烷(GenH2n+2)。
①Na2GeO3中锗原子的杂化方式是______。
②推测 1molGenH2n+2中含有的σ键的数目是_____(用NA表示阿伏加德罗常数值)。
(3)利用离子液体[EMIM] [AlCl4]可电沉积还原金属Ge,其熔点只有7℃其中 EMIM+结构如图所示。
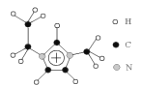
①该物质的晶体类型是_________。
②EMIM+ 离子中组成元素的电负性由小到大的顺序是________。
(4)独立的NH3分子中H-N-H 的键角为 107.3 ,[Zn(NH3)6]2+离子中H-N-H的键角________107.3° ( 填“大于”、“小于”或“等于” )。
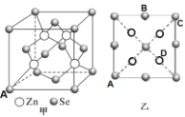
(5)硒化锌( ZnSe)是一种重要的半导体材料,其晶胞结构如图甲所示,该晶胞中硒原子的配位数是_____;已知晶胞边长为a pm,乙图为甲图的俯视图,A点坐标为( 0,0,0),B点坐标为(![]() ,a,
,a,![]() ) ,则 D点坐标为_______;若该晶胞密度为ρ g·cm-3,则阿伏加德罗常数NA为_______(列出计算式)。
) ,则 D点坐标为_______;若该晶胞密度为ρ g·cm-3,则阿伏加德罗常数NA为_______(列出计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图象表示的意义与相关的化学反应完全正确的是
A.向FeCl3溶液中不断加入铁粉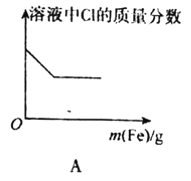
B.Fe(OH)2固体露置在空气中质量的变化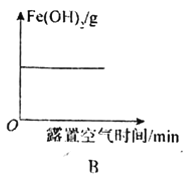
C.25℃时,向Cl2水溶液中通入二氧化硫(生成两种常见的酸) 
D.向AlCl3溶液中不断滴入烧碱溶液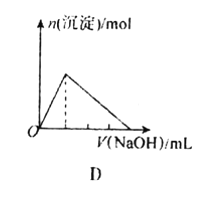
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚维酮碘的水溶液是一种常用的碘伏类缓释消毒剂,聚维酮通过氢键与HI3形成聚维酮碘,其结构表示如图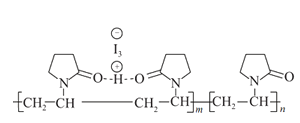 ,下列说法不正确的是( )
,下列说法不正确的是( )
A.聚维酮的单体是![]() B.聚维酮分子由(m+n)个单体聚合而成
B.聚维酮分子由(m+n)个单体聚合而成
C.聚维酮碘是一种水溶性物质D.聚维酮在一定条件下能发生水解反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com