
【题目】下列有关化学用语表示正确的是( )
A.CH3CH(OH)CH(CH3)CH3的系统命名为2—羟基—3—甲基丁烷
B.用电子式表示二氧化碳的形成过程:![]()
C.聚氯乙烯的链节:—CH2—CHCl—
D.甲醇和氧气设计成燃料电池,两极均以石墨为电极,K2CO3溶液为电解质,则负极电极反应式为:CH3OH+8OH--6e-=CO![]() +6H2O
+6H2O
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:高中化学 来源: 题型:
【题目】用压强传感器探究生铁在pH=2和pH=4醋酸溶液中发生腐蚀的装置及得到的图像如下:

分析图像,以下结论错误的是( )
A. 析氢腐蚀和吸氧腐蚀的速率一样快
B. 在酸性溶液中生铁可能发生吸氧腐蚀
C. 溶液pH≤2时,生铁发生析氢腐蚀
D. 两溶液中负极反应均为Fe – 2e- = Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备溴苯可用如图所示装置。
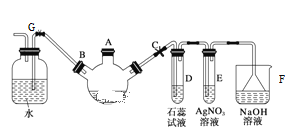
填空:
(1)关闭G夹,打开C夹,向装有少量苯的三颈烧瓶的A口加适量溴,再加入少量铁屑,塞住A口,三颈烧瓶中发生反应的有机反应方程式为___。
(2)E试管内出现的现象为___。
(3)F装置的作用是___。
(4)待三颈烧瓶中的反应进行到仍有气泡冒出时松开G夹,关闭C夹,可以看到的现象是___。
(5)反应结束后,拆开装置,从A口加入适量的NaOH溶液,然后将液体倒入__中(填仪器名称),振荡静置,从该仪器__口将纯净溴苯放出(填“上”或“下”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】辛烯醛是重要化工原料,某小组拟用正丁醛制备辛烯醛并探究其结构。
[制备实验]
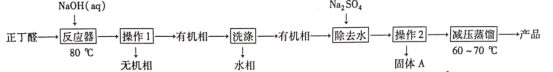
已知:①正丁醛的沸点为75.7℃。辛烯醛沸点为177℃,密度为0.848 g·cm-3,不溶于水。
②CH3CH2CH2CHO![]()
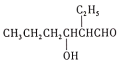
![]()
![]()
(1)在如图1三颈瓶中加入12.6 mL 2% NaOH溶液,在充分搅拌下,从恒压滴液漏斗慢慢滴入10 mL正丁醛。最适宜的加热方式是___________;使用冷凝管的目的是____________。
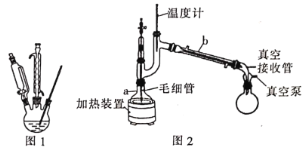
(2)操作1中使用的主要仪器名称是___________,有机相从___________(填“上”或“下”)口取出。
(3)判断有机相已洗涤至中性的操作方法:___________。
(4)操作2的名称是_____________;固体A的摩尔质量为322 g·mol-1,固体A的化学式为___________。
(5)利用图2装置进行“减压蒸馏”。下列有关说法错误的是___________。(填选项)
A 温度计示数为177℃,指示馏分温度
B 随着温度计液泡高度的提升,所得液体的沸点升高
C 毛细管的作用和沸石相似,防止液体暴沸
D 实验结束后,应先关闭冷凝水,再关闭真空泵
[性质实验]
资料显示:醛类(RCHO)在常温下能与溴水、酸性高锰酸钾溶液反应;在加热条件下能与银氨溶液、新制氢氧化铜浊液反应。
(6)为了证明辛烯醛含有碳碳双键,设计如下方案,能达到实验目的的是________。(填选项)
a 取少量溴水,滴加辛烯醛,振荡,溶液褪色
b 取少量酸性高锰酸钾溶液,滴加辛烯醛,振荡,溶液褪色
c 取少量辛烯醛,加入足量的银氨溶液,水浴加热充分反应后,冷却,在上层清液中先滴加稀盐酸酸化,再滴加溴水,振荡
d 取少量辛烯醛,加入足量的新制Cu(OH)2浊液,加热充分反应后,冷却,在上层清液中先滴加稀盐酸酸化,再滴加溴水,振荡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CaC2晶体的晶胞结构与NaCl晶体的相似(如图所示),但CaC2晶体中含有的哑铃形C2-的存在,使晶胞沿一个方向拉长(该晶胞为长方体)。下列关于CaC2晶体的说法中正确的是( )
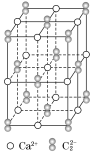
A.1个Ca2+周围距离最近且等距离的![]() 数目为6
数目为6
B.6.4 g CaC2晶体中含阴离子0.1 mol
C.该晶体中只有离子键
D.与每个Ca2+距离相等且最近的Ca2+共有12个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用亚硫酸盐(X)吸收烟气中的SO2。已知吸收过程中含硫组分物质的量分数(δ)与溶液pH的变化关系如图所示。下列说法中不正确的是( )
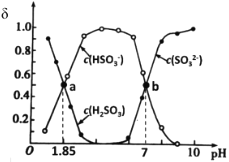
A.若X为(NH4)2SO3,图中b点溶液中n(HSO![]() )∶n(NH
)∶n(NH![]() )=1∶3
)=1∶3
B.若X为Na2SO3,当吸收液呈中性时:lgc(HSO![]() )-lgc(H2SO3)=5.15
)-lgc(H2SO3)=5.15
C.若X为(NH4)2SO3,(NH4)2SO3溶液呈碱性,说明水解程度:SO![]() >NH
>NH![]()
D.若X为Na2SO3,当吸收液pH=1.85时:c(Na+)=2c(HSO![]() )+c(SO
)+c(SO![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次 增大。在如图所示的物质转化关系中,p、q、 m.n分别是元素W、X、Y、Z的气体单质,p和 s均为有色气体,v的水溶液呈碱性。常温下,0.1 mol L -1 ,t 溶液与 0.1 mol L -1 u 溶液的pH均为1。下列说法不正确的是
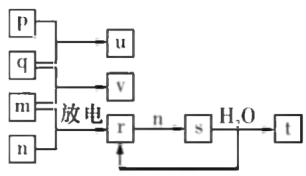
A.Y、W的兹高价氧化物对应的水化物均为强酸
B.元索的非金属性:Z>Y>X;原子半径:X<Z<Y
C.s溶于水的反应中,氧化剂与还原剂的物质的量之比为1:2
D.的电子式可表示为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚铁氰化钾(K4[Fe(CN)6])双称黄血盐,是一种重要的化工原料。检验三价铁发生的反应为:K4[Fe(CN)6]+FeCl3=KFe[Fe(CN)6]↓(滕氏蓝) +3KCl,回答问题:
(1)写出基态Fe3+的核外电子排布式_________。
(2)K4[Fe(CN)6]中的作用力除共价键外,还有______和________。含有12mol σ键的K4[Fe(CN)6的物质的量为________mol。
(3)黄血盐中N原子的杂化方式为______;C、N、O的第一电离能由大到小的排序为_____,电负性由大到小的排序为________。
(4)Fe、Na、K的晶体结构如图所示:
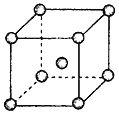
① 钠的熔点比钾更高,原因是__________________________。
② Fe原子半径是r cm,阿伏加德罗常数为NA,铁的相对原子质量为a,则铁单质的密度是_______g/cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科学院大连化物所的研究团队创新性提出锌碘单液流电池的概念, 实现锌碘单液流中电解液的利用率近 100%, 其原理如图所示。
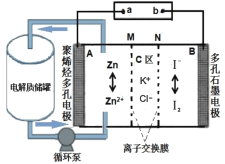
下列说法正确的是
A.放电时A电极反应式为:Zn+2e-=Zn2+B.放电时电解质储罐中离子总浓度减小
C.M为阴离子交换膜,N为阳离子交换膜D.充电时A极增重65g,C区增加离子数为2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com