
【题目】下列有关元素锶(38Sr,ⅡA族)的叙述最不可能的是
A. 其氯化物是离子化合物
B. 其最高价氧化物水化物为一种弱碱
C. 它比Ca更易置换水中的氢
D. 它的碳酸盐难溶于水
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】甲、乙两个实验小组分别进行“测定Na2CO3和NaCl混合物中Na2CO3含量”的实验。
甲组:沉淀分析法:用托盘天平称取w克混合物溶解于蒸馏水后,加入过量CaCl2,然后将所得沉淀过滤、洗涤、干燥、称量得m克,写出该反应的离子方程式________________________。其混合物中Na2CO3的质量分数为(写出表达式):___________。
乙组:气体分析法:把一定量的混合物与足量盐酸反应后,用如图装置测定产生的CO2气体的体积,为减小CO2的溶解,B中溶液应是_______。

A.氢氧化钠溶液 B.饱和碳酸钠溶液 C.饱和碳酸氢钠溶液
选用该溶液后实验结果还是不准确,原因是_____________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图象能直观地反映有关物理量的变化及规律,下列各图象与描述相符的是( )
A. 如图表示SO2氧化反应分别在有、无催化剂的情况下反应过程中的能量变化
如图表示SO2氧化反应分别在有、无催化剂的情况下反应过程中的能量变化
B. 如图表示0.1molMgCl26H2O在空气中充分加热时固体质量随时间的变化
如图表示0.1molMgCl26H2O在空气中充分加热时固体质量随时间的变化
C. 如图表示分别稀释1mLpH=2的盐酸和醋酸时溶液pH的变化,图中b>100mL
如图表示分别稀释1mLpH=2的盐酸和醋酸时溶液pH的变化,图中b>100mL
D.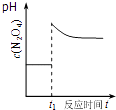 如图表示平衡2NO2(g)N2O4(g)在t1时迅速将体积缩小后c(N2O4)的变化
如图表示平衡2NO2(g)N2O4(g)在t1时迅速将体积缩小后c(N2O4)的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学研究发现,三种金属或两种金属可以组成准晶体。某准晶体样品M可能由铁、铜和铝中的三种或两种组成。
【实验目的】探究 ________________ 。
【提出假设】猜想1:M的成分是铁和铜;
猜想2:M的成分是铁和铝;
猜想3:M的成分是______;
猜想4:M的成分是铁、铜和铝
【设计实验】取两份质量均为m g的M样品,按图1和图2装置分别进行实验:实验前后条件都是常温、常压,待样品M充分反应后,按图1、图2实验方案完成实验并测得气体体积分别为V1 L和V2 L(所测定的气体体积已折合成标准状况)。
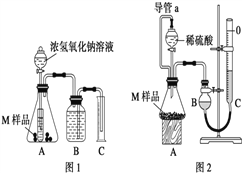
(1)完成实验目的和猜想填空内容。
(2)若该实验需要0.50mol/LNaOH溶液 180mL,按中学常用规格仪器配制时应称量____g NaOH(用托盘天平),若称量的NaOH固体中混有Na2O杂质会导致所配溶液浓度_____(填“偏大”、“偏小”或“无影响”)
(3)进行实验1前,B瓶中的水没有装满,使测得的气体体积 _______(填“偏大”、“偏小”或“无影响”),实验2中的导管a的作用为_____________并能防止因加入液体而排出锥形瓶内部分空气,导致测定的气体体积偏大。
(4)若V1≠0,则推测上述猜想 ________(填“1”、“2”、“3”或“4”)一定不成立,若猜想3成立,则V1 ________V2(填“>”、“<”或“=”)。
(5)若V1<V2≠0 ,则M样品中铁的质量为____________g(用含V1和V2式子表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X,Y,Z,W均为短周期元素,它们在元素周期表中的位置如下图所示.若Y原子的最外层电子数是次外层电子数的2倍,下列说法中正确的是( ) ![]()
A.氢化物稳定性:X>Y
B.最高价氧化物对应的水化物的酸性:W>Y
C.4种元素的单质中,W单质的熔、沸点最高
D.干燥的W单质具有漂白性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种元素,它们的原子序数依次增大,但均小于18,A和B在同一周期,A原子的电子式为 ![]() ,B原子L层的电子总数是K层的3倍;0.1mol C单质能从酸中置换出2.24L氢气(标准状况),同时它的电子层结构变成与氖原子的电子层结构相同;D离子的半径比C离子的小,D离子与B离子的电子层结构相同.
,B原子L层的电子总数是K层的3倍;0.1mol C单质能从酸中置换出2.24L氢气(标准状况),同时它的电子层结构变成与氖原子的电子层结构相同;D离子的半径比C离子的小,D离子与B离子的电子层结构相同.
(1)元素A、B、C、D分别是:A , B , C , D .
(2)D元素在周期表中属第周期族.
(3)用电子式表示A的气态氢化物的形成过程: .
(4)A和B的单质充分反应生成化合物的电子式是 .
(5)B与C形成的化合物是离子化合物还是共价化合物?如何证明; .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲苯氧化法制备苯甲酸的反应原理如下: 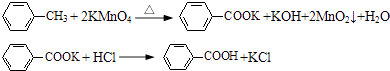
实验时将一定量的甲苯和KMnO4溶液置于图1装置中,在100℃时,反应一段时间,再停止反应,并按如下流程分离出苯甲酸和回收未反应的甲苯.
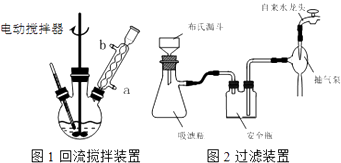
(1)实验室中实现操作Ⅰ所需的玻璃仪器有、烧杯;操作Ⅱ的名称为 .
(2)如果滤液呈紫色,要先加亚硫酸氢钾,然后再加入浓盐酸酸化,若无此操作会出现的危害是 .
(3)在操作Ⅲ中,抽滤前需快速冷却溶液,其原因是;如图2所示抽滤完毕,应先断开橡皮管.
(4)纯度测定:称取1.220g产品,配成100mL溶液,取其中25.00mL溶液,进行滴定,消耗KOH物质的量为2.4×10﹣3 mol.产品中苯甲酸质量分数为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式如图,下列说法正确的是( ) 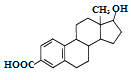
A.该有机物的分子式为C19H22O3
B.该分子中所有碳原子不可能在同一个平面内
C.能发生加成反应、取代反应、水解反应
D.能与Na、NaOH溶液反应,但不能与NaHCO3溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯化硼是一种重要的化工原料,某同学设计的三氯化硼制备装置如图. 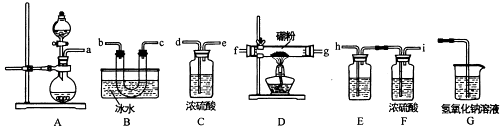
【查阅资料】
①BCl3:的熔点为﹣107.3℃,沸点为12.5℃
②2B+6HCl ![]() 2BCl3+3h2
2BCl3+3h2
③硼与侣的性质相似,也能与氢氧化钠溶液反应
请回答下列题:
(1)A装置可用高高锰酸钾固体与浓盐酸反应制氯气,反应的化学方程式为 .
(2)为了完成三氯化硼的制备,装置从左到右的接口连接顺序为 .
(3)装里E中的试剂为 . 如果拆去E装置,可能的后果是 .
(4)D装置中发生反应前先通入一段时间的氯气,其目的是 . 该装置中发生反应的化学方程式为 .
(5)三氯化硼与水能剧烈反应生成硼酸(H3BO3)和白雾,写出该反应的化学方程式 .
(6)请设计一个简易实验,验证制得的产品中是否含有硼粉 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com