
【题目】设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
A.0.1 molL﹣1醋酸溶液中含有醋酸分子的数目为0.1NA
B.25℃时,1 L pH=12的Na2CO3溶液中含有Na+的数目为0.2 NA
C.常温下,20 L pH=12的Na2CO3溶液中含有OH﹣数目为0.2 NA
D.某密闭容器盛有0.1 mol N2和0.3 mol H2 , 在一定条件下充分反应,转移电子数目为0.6 NA
【答案】C
【解析】解:A.溶液体积未知,无法计算微粒数目,故A错误;
B.25℃时,1L pH=12的Na2CO3溶液中,碳酸根离子部分水解溶液显示碱性,无法根据溶液中氢氧根离子的物质的量计算钠离子物质的量及数目,故B错误;
C.pH=12的Na2CO3溶液中c(H+)=10﹣12mol/L,故溶液中c(OH﹣)= ![]() =0.01mol/L,溶液中n(OH﹣)=20L×0.01mol/L=0.2mol,OH﹣离子数目为0.2mol×NAmol﹣1=0.2NA,故C正确;
=0.01mol/L,溶液中n(OH﹣)=20L×0.01mol/L=0.2mol,OH﹣离子数目为0.2mol×NAmol﹣1=0.2NA,故C正确;
D.氮气与氢气合成氨为可逆反应,可逆反应不能进行到底,某密闭容器盛有0.1 mol N2和0.3 mol H2,在一定条件下充分反应,转移电子数目小于0.6 NA,故D错误;
故选:C.


科目:高中化学 来源: 题型:
【题目】对于反应2SO2+O2![]() 2SO3,下列判断正确的是
2SO3,下列判断正确的是
A. 2 mol SO2和5 mol O2充分反应可生成2 mol SO3
B. 2 mol SO2和1mol O2达到化学平衡时SO2、O2、SO3的分子数之比一定为2∶1∶2
C. 达到化学平衡时SO2的消耗速率必定等于O2的生成速率的2倍
D. 三种物质的浓度相等时,说明反应达到了化学平衡。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学基本概念的说法正确的是
A.在水溶液中能电离出H+的化合物是酸
B.溶液与胶体的本质区别:分散质颗粒的直径大小
C.纯净物与混合物的区别:是否仅含有一种元素
D.根据不同的物质分类标准,纯碱可归类为碱、钠盐、碳酸盐等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图装置做相应实验,收集方法及所加试剂、现象、结论均正确的是
选项 | 气体 | 试剂 | 现象 | 结论 |
|
A | X | 酸性KMnO4溶液 | 溶液褪色 | X一定是SO2 气体 | |
B | NH3 | 酚酞溶液 | 溶液变红色 | 氨水呈碱性 | |
C | NO2 | 淀粉一KI溶液 | 溶液变蓝色 | NO2有还原性 | |
D | Cl2 | 紫色石蕊试液 | 溶液先变红后褪色 | 氯水有酸性和漂白性 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列叙述正确的是( )
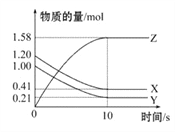
A. 反应开始到10 s,用Z表示的反应速率为0.158 mol·L-1·s-1
B. 10 s后,该反应停止进行
C. 反应的化学方程式为2X(g)+Y(g)![]() 2Z(g)
2Z(g)
D. 0~10 s的时间内的平均反应速率:v(X)=v(Y)=0.0395 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化铁是常见的水处理剂,工业上制备无水FeCl3的一种工艺如下: 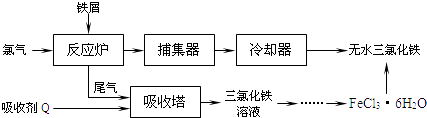
(1)试写出吸收塔中反应的离子方程式: .
(2)六水合氯化铁在水中的溶解度如下:
温度/℃ | 0 | 10 | 20 | 30 | 50 | 80 | 100 |
溶解度(g/100gH2O) | 74.4 | 81.9 | 91.8 | 106.8 | 315.1 | 525.8 | 535.7 |
从FeCl3溶液制得FeCl36H2O晶体的操作步骤是:加入少量盐酸、、、过滤、洗涤、干燥.
(3)常温下,若溶液的pH控制不当会使Fe3+沉淀,pH=4时,溶液中c(Fe3+)=molL﹣1 . (常温下Ksp[Fe(OH)3]=2.6×10﹣39).
(4)FeCl3的质量分数通常可用碘量法测定:称取mg无水氯化铁样品,溶于稀盐酸,再转移到100mL容量瓶,用蒸馏水定容;取出10.00mL,加入稍过量的KI溶液,充分反应后,滴入某一指示剂并用c molL﹣1 Na2S2O3溶液滴定用去V mL.(已知:I2+2S2O32﹣═2I﹣+S4O62﹣) ①滴定终点的现象是: .
②求样品中氯化铁的质量分数(写出计算过程) .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中符合如图图象的是( ) 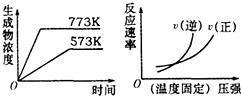
A.N2(g)+3H2(g)2NH3(g);△H=﹣Q1kJmol﹣1 (Q1>0)
B.2SO3(g)2SO2(g)+O2(g);△H=+Q2kJmol﹣1 (Q2>0)
C.4NH3(g)+5O2(g)4NO(g)+6H2O(g);△H=﹣Q3kJmol﹣1(Q3>0)
D.H2(g)+CO(g)C(s)+H2O(g);△H=+Q4kJmol﹣1﹣1(Q4>0)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组利用H2C2O4溶液和硫酸酸化的KMnO4溶液反应来探究“外界条件对化学反应速率的影响”。实验时通过测定酸性KMnO4溶液褪色所需时间来判断反应的快慢。该小组设计了如下方案。已知:KMnO4+H2C2O4+H2SO4→K2SO4+MnSO4+CO2↑+H2O (未配平)。
0.1mol·L-1KMnO4酸性溶液的体积/mL | 0. 6mol·L-1 H2C2O4溶液的体积/mL | H2O的积/mL | 实验温度/℃ | 溶液褪色时所需时间/min | |
实验1 | 10 | V1 | 35 | 25 | |
实验2 | 10 | 10 | 30 | 25 | |
实验3 | 10 | 10 | V2 | 50 |
(1)表中V1=___________mL , V2=___________mL。
(2)探究温度对化学反应速率影响的实验编号是________(填编号,下同),可探究反应物浓度对化学反应速率影响的实验编号是____________。
(3)实验①测得KMnO4溶液的褪色时间为2 min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(H2C2O4)=________________。
(4)已知50 ℃时c(MnO![]() )~反应时间t的变化曲线如图。若保持其他条件不变,请在坐标图中,画出25 ℃时c(MnO
)~反应时间t的变化曲线如图。若保持其他条件不变,请在坐标图中,画出25 ℃时c(MnO![]() )~t的变化曲线示意图________。
)~t的变化曲线示意图________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据元素周期表和元素周期律,判断下列叙述不正确的是

A. 气态氢化物的稳定性:H2O>NH3>SiH4
B. 氢元素与其他元素可形成共价化合物或离子化合物
C. 上图所示实验可证明元素的非金属性:Cl>C>Si
D. 用中文“![]() ”(ào)命名的第118号元素在周期表中位于第七周期0族
”(ào)命名的第118号元素在周期表中位于第七周期0族
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com