
【题目】某二元酸H2A在水中发生电离:H2A=H++HA-,HA-![]() H++A2-。下列叙述中不正确的是
H++A2-。下列叙述中不正确的是
A.在NaHA溶液中c(Na+)>c (HA-)> c(H+) >c (OH-)
B.在Na2A溶液中c (Na+)=2c (A2-)+2c(HA-)+2c (H2A)
C.在Na2A溶液中c (OH-) =c (HA-)+ c (H+)
D.在H2A溶液中c (H+)=c (HA-)+2c (A2-)+c (OH-)
 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:
【题目】Ga、N、Ni、As等元素常用于制造高科技材料。回答下列问题:
(1)基态As原子核外电子排布式为[ Ar] _____。
(2)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1变化趋势如图所示,其中除氮元素外,其他元素的E1自左向右依次增大的原因是___________;氮元素的E1呈现异常的原因是________。

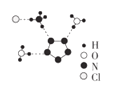
(3)我国科学家最近成功合成了世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl(用R表示)。经X射线衍射测得化合物R的晶体结构,其局部结构如图所示。图中虚线代表氢键,其表示式为(NH4+ )N— H…Cl、_______、_________。
(4)8-羟基喹啉铝(分子式为C27 H18AlN3O3)用于发光材料及电子传输材料,可由LiAlH与8-羟基喹啉(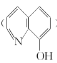 )合成。LiAlH中阴离子的空间构型为___ ;8- 羟基喹啉所含元素中电负性最大的是___(填元素符号),N、O的杂化方式依次为___、____。
)合成。LiAlH中阴离子的空间构型为___ ;8- 羟基喹啉所含元素中电负性最大的是___(填元素符号),N、O的杂化方式依次为___、____。
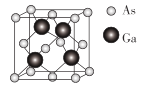
(5)GaAs的晶胞结构如图所示,其晶胞参数为a pm。设阿伏加德罗常数的值为NA,则GaAs的密度是_______g·cm-3(列出计算表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】淀粉水解的产物(C6H12O6)用硝酸氧化可以制备草酸,装置如图1所示(加热、搅拌和仪器固定装置均已略去):实验过程如下:
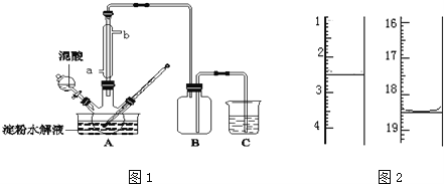
①将1:1的淀粉水乳液与少许硫酸(98%)加入烧杯中,水浴加热至85℃~90℃,保持30min,然后逐渐将温度降至60℃左右;
②将一定量的淀粉水解液加入三颈烧瓶中;
③控制反应液温度在55~60℃条件下,边搅拌边缓慢滴加一定量含有适量催化剂的混酸(65%HNO3与98%H2SO4的质量比为2:1.5)溶液;
④反应3h左右,冷却,减压过滤后再重结晶得草酸晶体,硝酸氧化淀粉水解液过程中可发生下列反应:
C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O
C6H12O6+8HNO3→6CO2+8NO↑+10H2O
3H2C2O4+2HNO3→6CO2+2NO↑+4H2O
请回答下列问题:
(1)实验①加入98%硫酸少许的作用是:_________;
(2)实验中若混酸滴加过快,将导致草酸产量下降,其原因是_________;
(3)检验淀粉是否水解完全所用的试剂为_________;
(4)草酸重结晶的减压过滤操作中,除烧杯、玻璃棒外,还必须使用属于硅酸盐材料的仪器有_________;
(5)将产品在恒温箱内约90℃以下烘干至恒重,得到二水合草酸.用KMnO4标准溶液滴定,该反应的离子方程式为:2MnO4﹣+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O称取该样品0.12g,加适量水完全溶解,然后用0.020molL﹣1的酸性KMnO4溶液滴定至终点(杂质不参与反应),此时溶液颜色变化为_________,滴定前后滴定管中的液面读数如图2所示,则该草酸晶体样品中二水合草酸的质量分数为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关.
(1)下列生活用品中,其主要材料属于天然纤维的是_________(填字母序号);
A.塑料保鲜薄 B.橡胶手套 C.棉布围裙
(2)我们常用的洗涤剂清洗餐具上的油污,这是因为洗涤剂具有_________的功能;
(3)食用水果、蔬菜主要补充人体所需的_________;
(4)国家禁止在面粉中添加增白剂过氧化钙CaO2,过氧化钙中氧元素的化合价为_______;
(5)农业上降低土壤酸性的是_________(填化学式);
(6)生活中要用到大量的钢铁,写出赤铁矿(主要成分Fe2O3)冶炼成铁的化学方程式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() 。
。![]() 时,
时,![]() 和
和![]() 的饱和溶液中,金属阳离子的物质的量浓度的负对数
的饱和溶液中,金属阳离子的物质的量浓度的负对数![]() 与溶液pH的变化关系如图所示。下列说法正确的是
与溶液pH的变化关系如图所示。下列说法正确的是
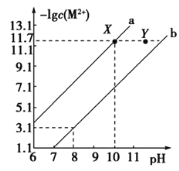
A.向等浓度的![]() 和
和![]() 的混合溶液中滴加
的混合溶液中滴加![]() 溶液,
溶液,![]() 先沉淀
先沉淀
B.当![]() 和
和![]() 沉淀共存时,溶液中:
沉淀共存时,溶液中:![]()
C.Y点对应的![]() 分散系是不稳定的体系
分散系是不稳定的体系
D.通过直接控制pH的方法可除去![]() 溶液中含有的量
溶液中含有的量![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酯类化合物与格氏试剂(![]() ,
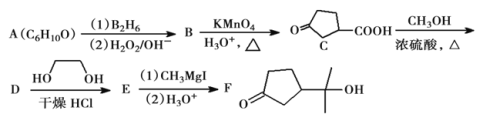
,![]() 、Br、I)的反应是合成叔醇类化合物的重要方法,可用于制备含氧多官能团化合物。化合物F的合成路线如下,回答下列问题:
、Br、I)的反应是合成叔醇类化合物的重要方法,可用于制备含氧多官能团化合物。化合物F的合成路线如下,回答下列问题:
已知:①![]()
②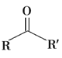
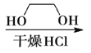
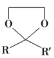
![]()
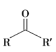
③![]()
![]()
![]()
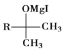
![]()
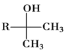
(1)A的结构简式为________;B中官能团的名称为________;![]() 的反应程式为________,其反应类型为________。
的反应程式为________,其反应类型为________。
(2)C与足量的![]() 反应后得到物质G,写出符合下列条件的G的同分异构体________(填结构简式,不考虑立体异构)。
反应后得到物质G,写出符合下列条件的G的同分异构体________(填结构简式,不考虑立体异构)。
①含有五元环结构;②能与![]() 溶液反应放出
溶液反应放出![]() 气体;
气体;
③![]() 与足量的钠反应,产生
与足量的钠反应,产生![]() 。
。
(3)碳原子上连有4个不同的原子或基团时,该碳称为手性碳。用“*”标出化合物F中的手性碳原子。__________
(4)写出以![]() 、格氏试剂和
、格氏试剂和![]() 为原料制备的合成
为原料制备的合成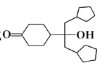 路线(其他试剂任选)。__________
路线(其他试剂任选)。__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2﹣羟基异丁酸乙酯能溶于水,是一种应用于有机合成和药物制造的化工原料。

(1)2﹣羟基异丁酸乙酯的分子式为_________,不同化学环境的氢在核磁共振氢谱图中有不同的吸收峰,则2﹣羟基异丁酸乙酯有_________个吸收峰;
(2)①②的反应类型分别为_________,_________;
(3)已知I为溴代烃,I→B的化学方程式为_________;
(4)缩聚产物F的结构简式为_________;
(5)下列关于![]() 和
和 的说法正确的有_________(双选,填字母);
的说法正确的有_________(双选,填字母);
A.后者遇到FeCl3溶液显紫色,而前者不可
B.两者都可以与NaHCO3溶液反应放出CO2
C.两者都可以与氢氧化钠溶液发生反应,当两者物质的量相等时,消耗氢氧化钠的量不相等
D.两者都可以与氢气发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】塑化剂DEHP的作用类似于人工荷尔蒙,会危害男性生殖能力并促使女性性早熟,长期大量摄取会导致肝癌.其毒性远高于三聚氰胺,会造成免疫力及生殖力下降.下列关于塑化剂邻苯二甲酸二正丁酯说法不正确的是( )
A.分子式为C16H22O4,可由石油化工原料通过取代,氧化,酯化反应制得
B.白酒中混有少量塑化剂,少量饮用对人体无害,可通过过滤方法除去
C.用核磁共振氢谱分析有6个吸收峰
D.邻苯二甲酸二正丁酯能发生加成,取代和氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A.1 mol/L的NH4Br溶液中通人适量氨气呈中性,此时溶液中NH4+的数目为NA
B.25 °C时,Ksp (BaCO3)=2.5×10-9 ,则BaCO3饱和溶液中Ba2+ 的浓度为5×10-5 mol/L
C.100g 17%双氧水中含有H原子的数目为NA
D.28g N2和CO的混合气体中含有的氧原子的数目为0.5NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com