
【题目】25 °C时,用浓度为0.1000 mol/L的NaOH溶液滴定体积均是20mL、浓度均为0.1000 mol/L的三种酸HX、HY、HZ,滴定曲线如图所示。下列说法正确的是( )
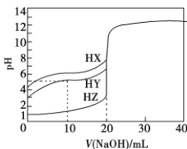
A.酸性强弱顺序是HX> HY> HZ
B.加入10 mL NaOH溶液时,HY溶液中c(Na+ )>c(Y -)
C.pH=2的HZ溶液加水稀释10倍,pH为3
D.加入20 mL NaOH溶液时,只有HY溶液达到滴定终点
【答案】C
【解析】
0.1000 mol/L的HZ,pH=1,c(H+)=0.1000 mol/L,则c(HZ)= c(H+),则HZ为一元强酸,HX和HY的pH都大于1,则HX和HY都是一元弱酸,同浓度的三种酸酸性强弱关系为:HX<HY<HZ,据此分析解答。
A.由分析可知,三种酸酸性强弱顺序是HX<HY<HZ,A错误;
B.加入10 mL NaOH溶液时,HY有一半被中和,此时溶质为等物质的量的HY和NaY,溶液中存在电荷守恒:c(Na+)+c(H+)=c(Y-)+c(OH-),由图可知,此时溶液呈酸性,c(H+)>c(OH-),所以,溶液c(Na+)<c(Y-),B错误;
C.HZ是强酸,加水稀释10倍,即101倍pH增大1,即pH=2的HZ溶液加水稀释10倍,pH为3,C正确;
D.加入20 mL NaOH溶液时,三种溶液pH均发生突变,说明三种溶液均达到滴定终点,D错误。
答案选C。


科目:高中化学 来源: 题型:
【题目】如图为苯和溴取代反应的改进实验装置。其中A为带支管的试管改制成的反应容器,在其下端开了一个小孔,塞好石棉绒,再加入少量铁屑。向反应容器A中逐滴加入溴和苯的混合液,几秒内就发生反应。
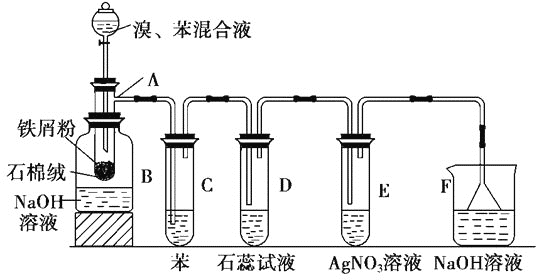
(1)试管C中苯的作用是_____;反应开始后,观察D试管,看到的现象为_____;能说明苯与溴发生的是取代反应而不是加成反应的现象为_____(只需写出一种)。
(2)装置中哪些部分能起到防倒吸的作用,请填序号________________。
(3)改进后的实验除①步骤简单,操作方便,成功率高;②各步现象明显;③对产品便于观察这三个优点外,还有一个优点是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下在一容积恒为2L的容器内发生反应:2A(g)+B(g2C(g),已知起始投入4molA(g)和2molB(g),经2s后测得C的浓度为0.6mol/L,并且2s后各组分浓度不再改变。下列说法正确的是
A.2 s 内用物质A 表示的平均反应速率为 0.6 mol/(Ls)
B.2 s 内用物质B 表示的平均反应速率为 0.15mol/(Ls)
C.2 s 后每有 0.6 mol 的物质B 生成,同时有 0.6 mol 物质C 生成
D.2 s 时物质B 的浓度为 0.7 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)基态Fe原子的简化电子排布式为______________________。
(2)常温下,Fe(CO)5为黄色液体,易溶于非极性溶剂。写出CO的电子式______________;Fe(CO)5分子中σ键与π键之比为______________。
(3)Ni能与类卤素(SCN)2反应生成Ni(SCN)2。Ni(SCN)2中第一电离能最大的元素是_____________;(SCN)2分子中硫原子的杂化方式是_____________;
(4)硝酸铜溶于氨水形成[Cu(NH3)4](NO3)2的深蓝色溶液。
①[Cu(NH3)4](NO3)2中阴离子的立体构型是_________________。
②与NH3互为等电子体的一种阴离子为_____________(填化学式);氨气在一定的压强下,测得的密度比该压强下理论密度略大,请解释原因__________。
(5)金属晶体可看成金属原子在三维空间中堆积而成,单质铝中铝原子采用铜型模式堆积,原子空间利用率为74%,则铝原子的配位数为________________。
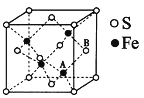
(6)铁和硫形成的某种晶胞结构如右图所示,晶胞参数a=xpm,则该物质的化学式为___________________;A原子距离B原子所在立方体侧面的最短距离为________________pm(用x表示); 该晶胞的密度为____________g·cm-3。(阿伏加德罗常数用NA表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2L容器中X、Y、Z三种气体物质的物质的量(n)随着时间(t)变化的曲线如图所示。由图中数据
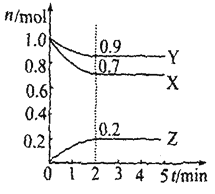
(1)该反应的化学方程式为_________________。
(2)反应开始至2min,用Z表示的平均反应速率为_____________。
(3)下列叙述能说明上述反应达到平衡状态的是_____________(填序号)。
A.X、Y、Z的物质的量之比为3∶1∶2
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗3molX,同时生成2molZ
D.混合气体的总质量不随时间的变化而变化
E.混合气体的总物质的量不随时间的变化而变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有甲、乙两个装置,下列说法错误的是( )
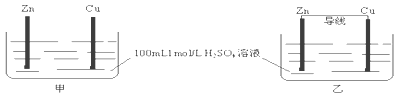
A. 甲、乙装置中,Zn的质量均减小B. 甲、乙装置中,Cu上均有气泡产生
C. 化学反应速率乙>甲D. 甲中H+移向Zn,乙中H+移向Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将下列物质进行分类(填序号)
①O2与O3②![]() C 与
C 与![]() C③白磷与红磷④冰与水⑤H2、D2、T2⑥乙醇与二甲醚⑦
C③白磷与红磷④冰与水⑤H2、D2、T2⑥乙醇与二甲醚⑦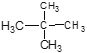 和
和![]()
(1)互为同位素的是_________。
(2)互为同素异形体的是_________。
(3)互为同分异构体的是_________。
(4)属于同一化合物的是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在利用镁条与醋酸的反应研究化学反应速率的影响因素的实验中,同学们记录了相同体积、不同浓度的醋酸与足量Mg条反应,产生H2体积随时间变化的数据,并以单位时间内产生H2的体积来表示反应速率,其反应速率随时间变化的图(如图所示)。
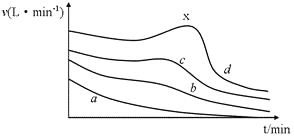
(1)在a、b、c、d四条曲线中,对应醋酸溶液的物质的量浓度最小的是_________,反应最后产生的H2在相同条件下体积最大的是_____________。
(2)在d曲线中,反应一段时间以后,反应速率出现反常的升高的现象(x点附近)。产生这种现象的原因主要是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油是工业的血液,与我们的生产、生活息息相关。
某烃A是重要的石油化工产品。其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,A可发生如图所示的一系列化学反应。回答下列问题。
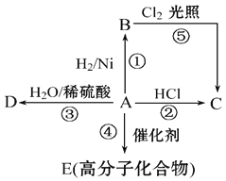
(1)物质A的工业制法是_____________________________。
(2)与A互为同系物的是______________________。(选填编号)
a CH3CH=CH2 b CH2=CHCH=CH2 c CH≡CH d CH3CH3
(3)高分子化合物E可用于制食品包装袋,写出其结构简式为_____________________;D是酒的主要成分,写出其结构简式为___________________________________。
(4)写出②⑤两步反应的化学方程式,并注明反应类型(有机物写结构简式)。
②__________________________________________反应类型________________
⑤__________________________________________反应类型________________
(5)苯是一种特殊的不饱和烃。若要鉴别苯与烯烃,可选用的试剂是______________。
(6)聚氯乙烯,简称PVC是一种在建筑材料、工业制品等方面广泛应用的通用塑料,若以乙炔为原料合成聚氯乙烯,请在方框内填写相应的物质,有机物写结构简式。
CH≡CH PVC
PVC
_____________________、_______________________
(7)异戊二烯是重要的有机化工原料,其结构简式为CH2=C(CH3)CH=CH2,它与溴水反应最多可以得到_________种产物。若烃X与异戊二烯具有相同的分子式,与Br2/CCl4反应后得到3-甲基-1,1,2,2-四溴丁烷,则烃X的结构简式为________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com