
【题目】(1)已知常温下,Ksp[Fe(OH)3]=4.0×10-38, 在FeCl3溶液中加入NaHCO3溶液产生沉淀和气体,反应的离子方程式为:____________;若将所得悬浊液的pH调整为4,则溶液中Fe3+浓度为_________molL-1
(2)常温下,浓度均为0.1molL-1的下列五种钠盐溶液的PH如下表
溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
PH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
上述盐溶液中的阴离子,结合H+能力最强的是__________。根据表中数据,浓度均为0.01 molL-1的下列四种酸的溶液分别稀释100倍,PH变化最大的是___________(填编号)。
A.HCN B.HClO C.CH3COOH D.H2CO3
(3) 下列说法不正确的是___ ___ ___ (填序号)
A.某温度下纯水中的c(H+)=10-6,故显酸性
B.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小
C.相同温度下,0.1mol/LNH4Cl溶液中NH4+的浓度比0.1mol/L氨水中NH4+的浓度大
D.相同温度下,PH均为8的Na2CO3和NaHCO3溶液,前者物质的量浓度大
E.向饱和石灰水中加入CaO固体,溶液中Ca2+、OH-的物质的量均减小
【答案】(l)Fe3++3HCO3-=Fe(OH)3↓+3CO2↑;4.0×10-8(2)CO32-;C(3)AD
【解析】
试题分析:(1)在FeCl3溶液中加入NaHCO3溶液产生沉淀和气体,沉淀是氢氧化铁,气体是CO2,反应的离子方程式为Fe3++3HCO3-=Fe(OH)3↓+3CO2↑;若将所得悬浊液的pH调整为4,溶液中氢氧根浓度是10-10mol/L,则根据氢氧化铁的溶度积常数可知溶液中Fe3+浓度为![]() =4.0×10-8molL-1。
=4.0×10-8molL-1。
(2)越容易水解的盐,越容易结合氢离子,相同浓度的钠盐溶液,pH越大则盐的水解程度越大,所以最容易水解的盐是碳酸钠,因此最容易结合氢离子的阴离子为CO32- ;浓度相同的酸稀释相同倍数后,酸性越强的酸其pH变化越大,四种酸的酸性大小顺序为醋酸最强,其次为碳酸,然后次氯酸,最弱的为HCN,所以溶液变化最大的为醋酸,答案选C。
(3)A.任何温度下纯水均显中性,A错误;B.盐酸抑制氯化银的溶解,所以用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小,B正确;C.一水合氨是弱电解质,氯化铵是强电解质,相同温度下,0.1mol/LNH4Cl溶液中NH4+的浓度比0.1mol/L氨水中NH4+的浓度大,C正确;D.碳酸根的水解程度大于碳酸氢根,因此相同温度下,pH均为8的Na2CO3和NaHCO3溶液,前者物质的量浓度小,D错误;E.向饱和石灰水中加入CaO固体,氧化钙和水反应生成氢氧化钙,温度不变,溶解度不变,因此有氢氧化钙晶体析出,溶液中Ca2+、OH-的物质的量浓度不变,但物质的量均减小,E正确,答案选AD。


 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案科目:高中化学 来源: 题型:
【题目】在下列条件下,一定能大量共存的离子组是
A.无色透明的水溶液中:K+、Mg2+、I-、MnO4-
B.有SO42-存在的溶液中:Na+、Mg2+、Ca2+、I-
C.在强碱溶液中:Na+、K+、CO32-、NO3-
D.在强酸性溶液中:K+、HCO3-、SO42-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)是一种强氧化性漂白剂,广泛用于纺织、印染和食品工业。它在碱性环境中稳定存在。某同学查阅资料后设计生产NaClO2的主要流程如下。
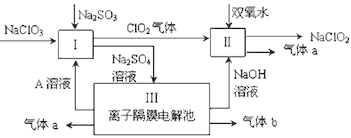
⑴ Ⅰ中发生反应的化学方程式是________________________,氧化剂与还原剂的物质的量之比是____________________;
⑵ Ⅱ中反应的离子方程式是_________________________;
⑶ 装置Ⅲ中阳极的反应是_________________________;
⑷ ClO2是一种高效水处理剂,可用亚氯酸钠和稀盐酸为原料制备:
5NaClO2+4HCl=5NaCl+4ClO2↑+2H2O
① 该反应中盐酸的作用是__________;② 写出实验室制氯气的离子方程式______________;说明上述两反应中盐酸作用不同的原因___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新能源汽车如(比亚迪秦、唐)相对传统汽车。有一系列的优点。如:环保、加速快(比亚迪唐0-100km/h加速时间仅需4.9秒)。而新能源汽车一个核心部件为锂离子电池,下图是我国科学家报道的某种水溶液锂离子电池体系。下列叙述错误的是
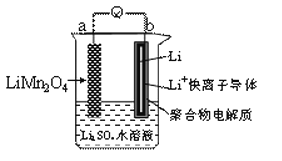
A. a为电池的正极
B. 电池充电反应为LiMn2O4=Li1-xMn2O4+xLi
C. 放电时,a极锂的化合价发生变化
D. 放电时,溶液中Li+从b向a迁移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用酸性氢氧燃料电池为电源进行电解的实验装置如图所示,下列说法正确的是( )
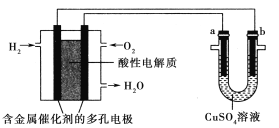
A.燃料电池工作时,正极反应为O2+2H2O+4e-=4OH-
B.电解精炼铜时,若转移1mol电子,a极质量减少32g
C.铁表面镀铜时,a为铁,b为Cu,工作一段时间要使右池溶液复原可加入适量的CuO
D.若a、b两极均为石墨时,在相同条件下,a极产生的气体与电池中消耗的O2体积相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
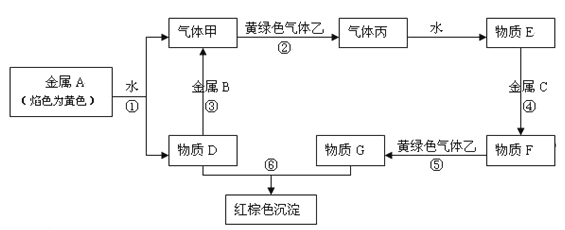
请根据以上信息回答下列问题:
(1)写出金属元素A的原子结构示意图:_______________。
(2)写出下列反应的离子方程式:
反应③___________;反应⑤____________________
(3)检验物质G中阳离子的操作方法_____________________。
(4)实验室制取黄绿色气体乙的化学方程式为__________________,在该反应中如有0.5 mol乙生成,转移的电子的物质的量是_____mol。制取完毕,多余的乙将用D的水溶液来吸收,其离子方程式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学-选修3:物质结构与性质】氟及其氟产品在工农业生产中应用非常广泛,回答下列问题;
(l)基态氟原子核外电子的运动状态有______种,这些电子的电子云形状有_________种,氟原子的价电子排布式为______________。
(2)NaHF2(氟化氢钠)电解可制氟气,NaHF2晶体中所含作用力的类型有_______;与HF2-互为等电子体的分子有______(举一例)。
(3)三氟化硼乙醚(![]() )熔点-58℃,沸点126~129℃,它属于_____________晶体。
)熔点-58℃,沸点126~129℃,它属于_____________晶体。
(4)氟化钙晶胞结构如下图所示,晶胞参数a=0.555 nm。
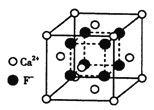
①Ca2+、F-的配位数分别为___________和___________。
②列式表示氟化钙晶体的密度________g/cm3(不必计算出结果)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com