
【题目】以高硫铝土矿(主要成分为Al2O3、Fe2O3、SiO2,少量FeS2和金属硫酸盐)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如图:
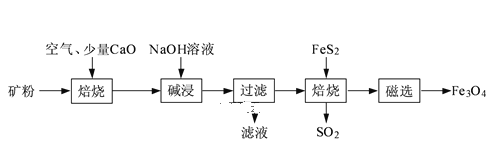
(1)焙烧过程均会产生SO2,用NaOH溶液吸收过量SO2的离子方程式为____。
(2)添加1%CaO和不添加CaO的矿粉焙烧,其硫去除率随温度变化曲线如题图所示。
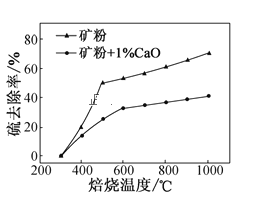
已知:多数金属硫酸盐的分解温度都高于600℃
硫去除率=(1![]() )×100%
)×100%
①不添加CaO的矿粉在低于500℃焙烧时,去除的硫元素主要来源于____。
②700℃焙烧时,添加1%CaO的矿粉硫去除率比不添加CaO的矿粉硫去除率低,其主要原因是___。
(3)向“过滤”得到的滤液中通入过量CO2,铝元素存在的形式由___(填化学式)转化为____(填化学式)。
(4)“过滤”得到的滤渣中含大量的Fe2O3。Fe2O3与Al混合在高温下发生的反应方程式____。
【答案】SO2+OH=HSO3 FeS2 硫元素转化为CaSO4而留在矿粉中 NaAlO2 Al(OH)3 2Al+Fe2O3![]() 2Fe+Al2O3
2Fe+Al2O3
【解析】
高硫铝土矿(主要成分为Al2O3、Fe2O3、SiO2,少量FeS2和金属硫酸盐)粉碎后通入空气、加入氧化钙焙烧,氧化钙和二氧化硫反应生成亚硫酸钙,亚硫酸钙氧化成硫酸钙和二氧化硅反应生成硅酸钙,产物加入氢氧化钠溶液碱浸,氧化铝溶解生成偏铝酸钠溶液,过滤得到溶液X为四羟基合铝酸钠溶液,经操作Ⅰ得到的固体中含大量的Fe2O3.Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2。
(1)用NaOH溶液吸收过量SO2生成亚硫酸氢钠;
(2)①不添加CaO的矿粉中S元素来源是FeS2和金属硫酸盐,金属硫酸盐的分解温度较高;
②700℃焙烧时,添加1%CaO的矿粉硫去除率比不添加CaO的矿粉硫去除率低,考虑加入CaO可能使S转化为CaSO4,形成的硫酸盐分解温度较高;
(3)过滤前使用NaOH溶液进行碱浸,Al2O3转化为NaAlO2,“过滤”得到的滤液中主要含有AlO2-,向“过滤”得到的滤液中通入过量CO2,可以将AlO2-转化为Al(OH)3;
(4)“过滤”得到的滤渣中含大量的Fe2O3,Fe2O3和铝发生铝热反应生成三氧化二铝和铁。
(1)焙烧过程均会产生SO2,是酸性氧化物,用NaOH溶液吸收过量SO2生成亚硫酸氢钠,离子方程式为:SO2+OH=HSO3;
(2)①不添加CaO的矿粉中S元素来源是FeS2和金属硫酸盐,金属硫酸盐的分解温度较高,所以可判断焙烧过程中S元素主要来源是FeS2;
②700℃焙烧时,添加1%CaO的矿粉硫去除率比不添加CaO的矿粉硫去除率低,考虑加入CaO可能使S转化为CaSO4,形成的硫酸盐分解温度较高,所以会导致S的脱除率降低;
(3)过滤前使用NaOH溶液进行碱浸,Al2O3转化为NaAlO2,再向“过滤”得到的滤液中通入过量CO2,可以将AlO2-转化为Al(OH)3,Al(OH)3再加热分解生成Al2O3;
(4)“过滤”得到的滤渣中含大量的Fe2O3,Fe2O3和铝发生铝热反应生成三氧化二铝和铁,2Al+Fe2O3![]() 2Fe+Al2O3。
2Fe+Al2O3。


科目:高中化学 来源: 题型:
【题目】硫代硫酸钠(![]() )是一种解毒药,用于氰化物、砷、汞、铅、铋、碘等中毒,临床常用于治疗荨麻疹,皮肤瘙痒等病症。硫代硫酸钠在中性或碱性环境中稳定,在酸性溶液中分解产生
)是一种解毒药,用于氰化物、砷、汞、铅、铋、碘等中毒,临床常用于治疗荨麻疹,皮肤瘙痒等病症。硫代硫酸钠在中性或碱性环境中稳定,在酸性溶液中分解产生![]() 和
和![]() 。
。
实验Ⅰ.![]() 的制备。工业上可用反应:
的制备。工业上可用反应:![]() 制得,实验室模拟该工业过程的装置如图所示。
制得,实验室模拟该工业过程的装置如图所示。

(1)仪器a的名称是__________,仪器b的名称是_____________。b中利用质量分数为70%~80%的![]() 溶液与
溶液与![]() 固体反应制备
固体反应制备![]() 反应的化学方程式为_______________________。c中试剂为________。
反应的化学方程式为_______________________。c中试剂为________。
(2)实验中要控制![]() 的生成速率,可以采取的措施有_________________________(写出一条)。
的生成速率,可以采取的措施有_________________________(写出一条)。
(3)为了保证硫代硫酸钠的产量,实验中通入的![]() 不能过量,原因是_________________________。
不能过量,原因是_________________________。
实验Ⅱ.探究![]() 与金属阳离子的氧化还原反应。
与金属阳离子的氧化还原反应。
资料:![]() (紫黑色)
(紫黑色)
装置 | 试剂X | 实验现象 |
|
| 混合后溶液先变成紫黑色,30s后溶液几乎变为无色 |
(4)根据上述实验现象,初步判断最终![]() 被
被![]() 还原为
还原为![]() ,通过________________________(填操作、试剂和现象),进一步证实生成了
,通过________________________(填操作、试剂和现象),进一步证实生成了![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美托洛尔可治疗各型高血压及作血管扩张剂,它的一种合成路线如下:

已知:![]() +
+![]()
![]()
![]() +HCl
+HCl
(1)A的化学名称是 _________,B的结构简式为__________,美托洛尔中含氧官能团的名称是_____________。
(2)A合成B的反应中,加人K2CO3的作用可能是 _________。
(3)B合成C的反应类型是________ 。
(4)F生成G的化学方程式为________ 。
(5)氯甲基环氧乙烷(![]() ) 是合成有机化合物的重要原料,实验室检验卤代烃中氯原子的常用试剂是______。
) 是合成有机化合物的重要原料,实验室检验卤代烃中氯原子的常用试剂是______。
(6)芳香族化合物M是F的同分异构体.则符合下列条件的M共有___种(不含立体异构)。
①苯环上只有2个取代基
②1molM与足量 Na 充分反应能生成1mol H2
③能与FeCl3溶液发生显色反应。
其中核磁共振氢谱为5组峰同分异构体的结构简式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮、硫、氯及其化合物是中学化学重要的组成部分。
(1)氨气燃料电池使用的电解质溶液是KOH溶液,电池反应为:4NH3+3O2=2N2+6H2O。该电池负极的电极反应式为____;用该电池进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,以CuSO4溶液为电解质溶液,下列说法正确的是____。
a.电能全部转化为化学能
b.SO42﹣的物质的量浓度不变(不考虑溶液体积变化)
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
e.若阳极质量减少64g,则转移电子数为2NA个
(2)①将SO2通入到BaCl2溶液中,出现了异常现象,看到了明显的白色沉淀,为探究该白色沉淀的成分,他设计了如下实验流程:所得悬浊液![]() 白色沉淀
白色沉淀![]() 观察现象并判断,则试剂A的化学式为_____。实验表明,加入试剂A后,白色沉淀未见溶解,产生该白色沉淀的离子方程式是____。
观察现象并判断,则试剂A的化学式为_____。实验表明,加入试剂A后,白色沉淀未见溶解,产生该白色沉淀的离子方程式是____。
②利用如图所示电化学装置吸收工业尾气中SO2,阴极上生成Cu。写出装置中阳极的电极反应式_____。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组采用如图所示装置,对浓硝酸与木炭的反应进行探究(已知:4HNO3![]() 4NO2↑+O2↑+2H2O)。
4NO2↑+O2↑+2H2O)。
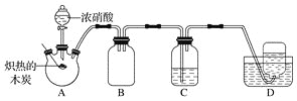
请回答下列问题:
(1)检查装置气密性后,将燃烧匙中的木炭在酒精灯上加热至炽热状态,伸入三颈烧瓶中,生成的气体的颜色为__,产生该气体的反应的化学方程式是__。
(2)装置C中盛有足量Ba(OH)2溶液,炽热的木炭与浓硝酸反应后可观察到C中出现白色沉淀,该白色沉淀为__(填化学式)。
(3)装置B的作用是__。
(4)装置D中收集到了无色气体,有同学认为是NO,还有同学认为是O2。
①下列对该气体的检验方法合适的是__(填字母)。
A.敞口观察装置D中集气瓶内气体的颜色变化
B.将湿润的蓝色石蕊试纸伸入集气瓶内,观察蓝色石蕊试纸是否变红
C.将带火星的木条伸入集气瓶中,观察木条是否复燃
②如果D中集气瓶内收集到的无色气体是氧气,则氧气的来源是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为![]() 。下列说法正确的是
。下列说法正确的是
A. 1L0.1mol·![]() NH4Cl溶液中,
NH4Cl溶液中, ![]() 的数量为0.1
的数量为0.1![]()
B. 2.4gMg与H2SO4完全反应,转移的电子数为0.1![]()
C. 标准状况下,2.24LN2和O2的混合气体中分子数为0.2![]()
D. 0.1mol H2和0.1mol I2于密闭容器中充分反应后,其分子总数为0.2![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是( )
A. NaCl(aq)![]() Cl2(g)
Cl2(g)![]() FeCl2(s)
FeCl2(s)
B. AlCl3(aq)![]() Al(OH)3(s)
Al(OH)3(s)![]() Al2O3(s)
Al2O3(s)
C. S(s)![]() SO3(g)
SO3(g)![]() H2SO4(aq)
H2SO4(aq)
D. N2(g)![]() NH3(g)
NH3(g)![]() NaHCO3(s)
NaHCO3(s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素A、B、C、D、E的原子序数依次增大,A和C同族,B和D同族,C离子和B离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,C和E形成的化合物是日常生活中的常用调味品。回答下列问题:
(1)五种元素中,原子半径最大的是________,非金属性最强的是________(填元素符号)。
(2)由A分别和B、D、E所形成的共价型化合物中,热稳定性最差的是__________(用化学式表示)。
(3)A、B、E形成的离子化合物电子式为____________,其中存在的化学键类型为____________。
(4)D最高价氧化物的水化物的化学式为________________。
(5)单质D在充足的单质E中燃烧,反应的化学方程式为__________________;D在不充足的E中燃烧,生成的主要产物的化学式为__________。
(6)单质E与水反应的离子方程式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酯类物质是极为重要的有机合成产品或中间产物,结构简式为(![]() )的酯类有机物 E(核磁共振氢谱有3 个峰)是一种重要的塑化剂,工业上合成 E 的路线如下图所示:
)的酯类有机物 E(核磁共振氢谱有3 个峰)是一种重要的塑化剂,工业上合成 E 的路线如下图所示:
⑴烃 A 的名称_________,E 的分子式为_____,C 中官能团的结构简式为_____。
⑵④的反应条件为_____,上述转化中属于取代反应的是_____。
⑶②的化学方程式为_____。
⑷B 有很多同分异构体,其中苯环上有三个取代基且遇 FeCl3 溶液显紫色的物质共有_____种;写出分子中有 5 种不同化学环境的氢原子的结构简式__________________________________。
⑸已知R-CH=CH2 ![]() RCH2CHO,写出以CH2=CH2和H218O为原料(其他无机试剂任选)合成
RCH2CHO,写出以CH2=CH2和H218O为原料(其他无机试剂任选)合成![]() 的合成路线图______________________________________________(仿照题目中形式,不要编号)
的合成路线图______________________________________________(仿照题目中形式,不要编号)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com