
【题目】为确定某铝热剂(含氧化铁和铝)的组成,分别进行下列实验:
(1)若取a g样品,向其中加入足量的NaOH溶液,测得生成的气体(标准状况,下同)体积为b L。反应的化学方程式是________________________;样品中铝的质量为________g。
(2)另取a g样品将其点燃,恰好完全反应,该反应的化学方程式是2Al+Fe2O3![]() 2Fe+Al2O3,氧化铁与铝的质量比是________。
2Fe+Al2O3,氧化铁与铝的质量比是________。
(3)待(2)中反应产物冷却后,加入足量盐酸,测得生成的气体体积为c L,该气体与(1)中所得气体的体积比c∶b=________。
【答案】2Al+2NaOH+2H2O===2NaAlO2+3H2↑ 9b/11.2 80:27 2:3
【解析】
(1)氧化铁和氢氧化钠溶液不反应,铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,反应方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,根据方程式知,铝的质量=![]() ×
×![]() ×27g/mol=
×27g/mol=![]() g;
g;
(2)铝与氧铁在高温下生成铁与氧化铝,反应方程式为:2Al+Fe2O3![]() 2Fe+Al2O3;由二者恰好反应,根据方程式可知,质量之比等于总的相对分子质量之比,则样品中氧化铁与铝的质量比为(56×2+16×3):2×27=80:27;
2Fe+Al2O3;由二者恰好反应,根据方程式可知,质量之比等于总的相对分子质量之比,则样品中氧化铁与铝的质量比为(56×2+16×3):2×27=80:27;
(3)由方程式2Al+Fe2O3![]() 2Fe+Al2O3可知,(2)中生成的n(Fe)等于铝热剂中n(Al),与盐酸反应生成的氢气体积之比等于金属提供的电子的物质的量之比,所以(3)中生成的氢气与(1)中生成氢气体积之比c:b=2n(Fe):3n(Al)=2:3。
2Fe+Al2O3可知,(2)中生成的n(Fe)等于铝热剂中n(Al),与盐酸反应生成的氢气体积之比等于金属提供的电子的物质的量之比,所以(3)中生成的氢气与(1)中生成氢气体积之比c:b=2n(Fe):3n(Al)=2:3。


 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源: 题型:
【题目】12.0g某液态有机化合物A完全燃烧后,生成14.4g H2O和26.4g CO2。测得有机化合物A的蒸气对H2的相对密度是30,求:
(1)有机物A的分子式_______________________。(写出计算过程)
(2)用如图所示装置测定有机物A的分子结构,实验数据如下(实验数据均已换算为标准状况):a mL(密度为ρ g/cm3)的有机物A与足量钠完全反应后,量筒液面读数为b mL,若1mol A分子中有x mol氢原子能跟金属钠反应,则x的计算式为____________(可以不化简,写出计算过程)。

(3)已知该有机物能够与金属钠或钾发生反应,并对有机物进行核磁共振操作,发现核磁共振氢谱图上有三组吸收峰,且峰面积之比为6:1:1,请写出该物质的结构简式:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷酸二氢钾在工农业和医学领域具有广泛的应用。以下是工业上制备磷酸二氢钾的三种方法。回答下列问题:
I.直接法

(1)气体X为___________(填化学式);
(2)“浸取”步骤,浓硫酸能与KCl能发生化学反应的原因是___________________;
(3)“转化”步骤发生反应的离子反应方程式_______________(已知:Ca3(PO4)2难溶于水);
(4)滤液①中加入甲醇的作用是__________________________;
(5)“操作I”是___________________________________;
II.中和反应法
(6)氢氧化钾溶液与高纯度磷酸在反应器中发生中和反应制备磷酸二氢钾。写出此反应的离子反应方程式_______________________________;由下图判断制备磷酸二氢钾(达80%)的最佳pH范围______________________;

Ⅲ.电解法制取KH2PO4的原理如上图所示。一定条件下,还可得到NaClO3。
(7)在_____室(填标号)可得到KH2PO4;写出产生ClO3-的电极反应式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,杠杆 AB 两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠 杆并使其在水中保持平衡,然后小心地向烧杯中央滴入浓 CuSO4 溶液,一段时间后,下列 有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化)

A. 杠杆为导体和绝缘体时,均为 A 端高 B 端低
B. 杠杆为导体和绝缘体时,均为 A 端低 B 端高
C. 当杠杆为绝缘体时,A 端低 B 端高;为导体时,A 端高 B 端低
D. 当杠杆为绝缘体时,A 端高 B 端低;为导体时,A 端低 B 端高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国古代青铜器工艺精湛,有很高的艺术价值和历史价值,但出土的青铜器大多受到环境腐蚀,故对其进行修复和防护具有重要意义。
(1)原子序数为29的铜元素位于元素周期表中第_______周期。
(2)某青铜器中Sn、Pb的质量分别为119g、20.7g,则该青铜器中Sn和Pb原子的数目之比为__________。
(3)研究发现,腐蚀严重的青铜器表面大都存在CuCl。关于CuCl在青铜器腐蚀过程中的催化作用,下列叙述正确的是________。
A.降低了反应的活化能 B.增大了反应的速率
C.降低了反应的焓变 D.增大了反应的平衡常数
(4)采用“局部封闭法”可以防止青铜器进一步被腐蚀。如将糊状Ag2O涂在被腐蚀部位,Ag2O与有害组分CuCl发生复分解反应,该化学方程式为_________________。
(5)如图为青铜器在潮湿环境中发生的电化学腐蚀的示意图。

①腐蚀过程中,负极是________(填图中字母“a”或“b”或“c”);
②环境中的Cl﹣扩散到孔口,并与正极反应产物及负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl,其离子方程式为_____________________;
③若生成4.29gCu2(OH)3Cl,则理论上耗氧体积为___________L(标准状况)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期金属元素甲~戊在元素周期表中的相对位置如右表所示,下面判断正确的是
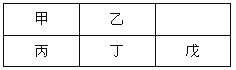
A. 原子半径:丙<丁<戊B. 金属性:甲>丙
C. 氢氧化物碱性:丙>丁>戊D. 最外层电子数:甲>乙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于下列化学用语,有关说法不正确的是
①SO2②Fe3+③KMnO4④![]() ⑤
⑤![]()
A.①表示的是两种元素组成的化合物
B.②中数字的含义:一个铁离子带3个单位的正电荷
C.③中锰元素的化合价为+7价
D.④⑤表示的是同一种元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为按树状分类法对一组物质进行的分类。回答下列问题。

(1)类别1为_________,类别2为____________。
(2)上述物质中属于电解质的是_______________。
(3)Ba(OH)2溶于水时的电离方程式为________________。向Ba(OH)2溶液中滴加稀硫酸,所发生反应的离子方程式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物X、Y的转化如下,下列说法不正确的是

A. X转化为Y的反应属于氧化反应
B. ![]() 与Y互为同分异构体
与Y互为同分异构体
C. Y分子苯环上的二氯代物有5种
D. X、Y分子的所有原子可能共平面
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com