
����Ŀ��±�ص����ڼ�����Һ���������绯��Ӧ���绯�IJ�������Ӧ�¶ȵIJ�ͬ����ͬ��
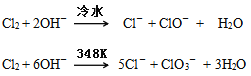
��ͼΪ��ȡ����������ء��������ƺͼ����������ʵ���ʵ��װ�ã�

װ����ʢװ��ҩƷ���£������õι���װ��5mLŨ�������֧���Թ���װ��1.5gKMnO4������֧���Թ���װ��2~3mLŨ�����U�η�Ӧ����װ��30%KOH��Һ����U�η�Ӧ����װ��2mol/LNaOH��Һ��������˫U�η�Ӧ���зֱ�װ��0.1mol/LKI-������Һ��KBr��Һ����β�������ý���0.5mol/LNa2S2O3��Һ�������Ḳ��ס

��1������װ�������Լ��ķ���_________________________��
��2��Ϊ��ʹװ���������еķ�Ӧ˳����ɣ�Ӧ�ÿ��Ƶķ�Ӧ�����ֱ�Ϊ________________________________��
��3��װ�����������ܹ��۲쵽��ʵ������ֱ���____________________��
��4�������װ���������е��Լ�����λ�ã����ܷ�֤����������Cl2>I2��______����ܡ����ܡ����������ǣ�______________��
��5����֪����غ��Ȼ��ص��ܽ����������ͼ��ʾ����Ӧ������װ��������ȡ����ؾ����ʵ�������_____________��
��6��β������ʱ������Ӧ�����ӷ���ʽΪ____________________��
��7��ѡ����ʵ��װ�õ��ŵ���___________________������д���㣩��
���𰸡� ���Ӻ�ʵ��װ�ã��ɢർ�����װ���м�ˮ�������γ�һ���ȶ���ˮ������װ�õ����������ã�����������Ҳ�ɵ÷֣� װ�âܷ���348K(��75��)��ˮԡ�У�װ�âݷ����ˮԡ�� װ�â�����Һ������װ�â�����Һ��ɳ�ɫ �� ������װ�â������е��Լ���Cl2��KBr��Ӧ����Br2���ӷ�������KI��Ӧ��Ҳ����֤��Cl2��������ǿ��I2 ��ȴ�ᾧ������ S2O32- + 4Cl2 + 5H2O = 2SO42- + 8Cl- + 10H+ ��ʵ��װ�á���Լ�ɱ����Լ������١���Դ�����٣���ʡ�ռ䣬����ʵ��ʱ�䣻������Ⱦ��
��������������������⿼��Cl2��ʵ�����Ʊ���Cl2������ʵ�飬KClO3��NaClO���Ʊ���
��1������װ�������Եļ����Һ��������ǣ����Ӻ�ʵ��װ�ã�������������װ���м�ˮ�������γ�һ���ȶ���ˮ������װ�õ�������������
��2������ʵ��Ŀ�ģ�װ������ʢ��30%KOH��Һ��װ�����з����ķ�ӦΪ3Cl2+6KOH![]() KClO3+5KCl+3H2O��װ���������Ʊ�KClO3��װ������ʢ��2mol/LNaOH��Һ��װ�����з����ķ�ӦΪCl2+2NaOH=NaCl+NaClO+H2O��װ���������Ʊ�NaClO�����������Ϣ��ʹװ�����з�Ӧ˳����ɣ�װ��������348K��ˮԡ�У�ʹװ�����з�Ӧ˳����ɣ�װ���������ˮԡ�С�
KClO3+5KCl+3H2O��װ���������Ʊ�KClO3��װ������ʢ��2mol/LNaOH��Һ��װ�����з����ķ�ӦΪCl2+2NaOH=NaCl+NaClO+H2O��װ���������Ʊ�NaClO�����������Ϣ��ʹװ�����з�Ӧ˳����ɣ�װ��������348K��ˮԡ�У�ʹװ�����з�Ӧ˳����ɣ�װ���������ˮԡ�С�
��3��װ������ʢ��KI-������Һ��ͨ��Cl2������Ӧ��Cl2+2KI=2KCl+I2��I2�����۳���ɫ��װ������ʵ�������ǣ���Һ������װ������ʢ��KBr��Һ��ͨ��Cl2������Ӧ��Cl2+2KBr=2KCl+Br2��װ������ʵ�������ǣ���Һ��ɳ�ɫ��
��4�������װ���������е��Լ�����λ�ã�װ������ʢ��KBr��Һ��װ�����з�����Ӧ��Cl2+2KBr=2KCl+Br2���ɴ˵ó������ԣ�Cl2![]() Br2��װ������ʢ��KI-������Һ������Cl2����װ�����лӷ�������Br2��g��������KI��Ӧ����I2����˵��Cl2��Br2��g����������ǿ��I2�����װ�����н���Ҳ��֤��Cl2��������ǿ��I2��װ�����������Լ�����λ�ã�����֤�������ԣ�Cl2
Br2��װ������ʢ��KI-������Һ������Cl2����װ�����лӷ�������Br2��g��������KI��Ӧ����I2����˵��Cl2��Br2��g����������ǿ��I2�����װ�����н���Ҳ��֤��Cl2��������ǿ��I2��װ�����������Լ�����λ�ã�����֤�������ԣ�Cl2![]() I2��
I2��
��5�������ܽ�����ߣ�KClO3���ܽ�����¶�������������KCl�ڵ���ʱ�ܽ�ȴ���KClO3������ʱ�ܽ��С��KClO3����װ��������ȡKClO3�����ʵ�����������Һ��ȴ�ᾧ�����ˣ�ϴ�ӣ����
��6��β����0.5mol/LNa2S2O3��Һ���գ�Cl2��S2O32-������SO42-��Cl2����ԭ��Cl-����Ӧд��Cl2+S2O32-��SO42-+Cl-�����ݵ�ʧ�����غ���ƽ��4Cl2+S2O32-��2SO42-+8Cl-������ԭ���غ�͵���غ㣬β������ʱ�����ӷ���ʽΪ4Cl2+S2O32-+5H2O=2SO42-+8Cl-+10H+��
��7��ѡ����ʵ��װ�õ��ŵ��У���ʵ��װ�á���Լ�ɱ����Լ������١���Դ�����٣���ʡ�ռ䣬����ʵ��ʱ�䣻������Ⱦ����


 �ƸԾ���Ȥζ����ϵ�д�
�ƸԾ���Ȥζ����ϵ�д� ����С����ҵ��ϵ�д�
����С����ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)��ͼI��ʾ10mL��Ͳ��Һ���λ��,A��B,B��C�̶ȼ����1mL,����̶�A��ֵΪ4,����Ͳ��Һ�������Ǣ�,���ڷ���λ�ò�������ʱ����,��������ֵΪ����٢ڵ���ȷ��ֵΪ__________________
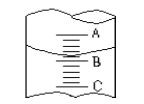
A��3.2mL����С��3.2mL B.��4.8mL���ڴ���4.8mL
C.��3.2mL���ڴ���3.2ml D.��4.8mL����С��4.8mL
��ʵ����������1mol��L-1��NaOH��Һ220mL,����������ƽ��ȡNaOH����ʱ,��ƽ����Ϊ________�����,��ͬ)��
A.����8.8g B.��8.8g C.8.8g
��2����ʾ��ҺŨ�ȵķ���ͨ��������;��Һ�����ʵ���������(W)�����ʵ���Ũ�� (c),�����������Һʱ,���ݲ�ͬ����Ҫ,�в�ͬ�����Ʒ������������������⡣
��.��10%(�ܶ�Ϊ1.01g��cm3-)������������Һ���Ƴ�27.5g 2%������������Һ��
�ټ���:��_________g10%(�ܶ�Ϊ1.01g��cm3-)������������Һ
����ȡ:����Ͳ��ȡ10%������������Һ_________mL
��.��98%(�ܶ�Ϊ1.84g��cm3-)��Ũ����ϡ�ͳ�2mol/L��ϡ����100ml,�ش���������:
����Ҫ��ȡŨ����_______ mL
������ʵ�����ʹ���Ƶ���ҺŨ��ƫ�͵���__________
A.����ƿϴ�Ӻ�δ����
B.��ȡ��Һʱ,���ӿ̶���
C.װ���Լ�ƿʱ,��������Һ����
D.û��ϴ���ձ��Ͳ�����
E.����ʱ,��ˮ���������̶���,�ֵ���һЩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�������Һ�е���Ũ�ȹ�ϵ����ȷ����
A. pH��8.3��ij��ʽ��NaHB��ˮ��Һ����c (Na+) > c (HB��) > c (H2B) > c (B2��)
B. �����ʵ���Ũ�ȵ�Na2S��NaHS��Һ����c (Na+)��2c (S2��) + c (HS��)
C. NH4HSO4��Һ�еμ�NaOH��Һ��ǡ�ó�������c (Na+) > c (SO42��) > c (NH4+) > c (OH��)��c (H+)
D. 0.1 mol / L NaH2PO4��Һ����c (Na+)��c (PO43��) + c (HPO4����) + c (H2PO4��) + c (H3PO4)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Al2 (SO4 )3 ��K2 SO4 �������Ļ����Һ��,���c(SO4 2- )����0.2 mol/L,������������0.2 mol/L ��KOH��Һʱ,���ɵij���ǡ���ܽ�,��ԭ�����Һ��K + �����ʵ���Ũ��Ϊ
A. 0.2 mol/L B. 0.25 mol/L C. 0.45 mol/L D. 0.225 mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ϩ�ͱ���������ʺϳ�I���ϳ�·�����£�
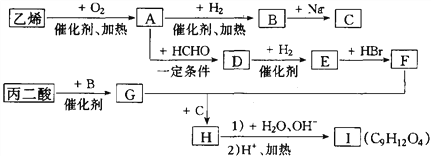
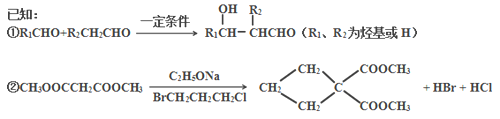
��ش��������⣺
��1��������Ľṹ��ʽ��_________��
��2���л���D�ķ���ʽΪC5H10O4��������ŵ�������__________��
��3��д��A��B�Ļ�ѧ��Ӧ����ʽ______________________________________��
��4��E��F�ķ�Ӧ������______________��
��5����һ�������£����������Ҷ���ͨ���������۷�Ӧ���ɸ߷��ӻ����д���ø߷��ӻ�����Ļ�ѧʽ______________��
��6��I��ͬ���칹�������ڷ����廯����������������������_____�֡�
�ٱ�������4��ȡ����������FeCl3��Һ������ɫ��Ӧ����ÿ��ͬ���칹��1 mol����1 mol̼���Ʒ�����Ӧ��Ҳ�������������Ʒ�Ӧ����2molH2����һ��̼ԭ������2����2�������ǻ����ȶ���
���б����ϵ�һ�ȴ���ֻ��һ�ֵ���___________________��(д������һ�ֵĽṹ��ʽ)
��7�������������ϩ����ȩΪԭ���Ƶã��������Լ���ѡ������ģ�²������ϳ�·��ͼ��___________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У���Ϊͬ���칹�����
A.���Ǻ���ѿ��B.���ۺ�������
C.���ۺ���ά��D.���Ǻ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һС������Ʒ���ˮ�У�����������ȷ���ǣ� ��
A.Na����ˮ����
B.Na��ˮ�����ζ�
C.Na����ˮ����
D.Na�۳ɹ�����С��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ͻ���һ����;�㷺�Ľ������ϣ����������У������ںϽ���ǣ� ��
A.̼�ظ�
B.ˮ��
C.��ͭ
D.��ͭ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com