
【题目】据统计,我国每年报废的手机超过1亿部,若不进行有效回收利用,会造成巨大的浪费和污染。某种手机电路板中含有以下金属:Sn、Pb、Fe、Cu、Au、Ag、Ni(镍,银白色)、Pd (钯,银白色)。如图是某工厂回收其中部分金属的流程图.(假设流程图中各反应均恰好完全反应.己知:2Cu+O2+2H2SO4![]() 2CuSO4+2H2O)
2CuSO4+2H2O)

(1)步骤②中产生的气体是________(写化学式)。
(2)滤渣2中含有的金属是________
(3)步骤⑤反应的化学方程式________。
(4)步骤⑥回收的纯净物B是________ (写化学式).
(5) 金属Fe、Ni、Pd在溶液中的活动性由强到弱的顺序依次是________。
【答案】 H2 Sn、Pb、Ni Fe+CuSO4=FeSO4+Cu FeSO4 Fe、Ni、Pd
【解析】金属板加入足量的稀硫酸得到滤渣1和滤液1,滤渣1中加入稀硫酸、氧气控制温度加热,得到银、金、钯和滤液3,滤液3中加入铁粉会生成红色固体A,所以A是铜,滤渣1中含有银、金、钯、铜,滤液3是硫酸铜,滤液4是硫酸亚铁,所以铁、锡、铅、镍排在氢之前,滤液1中加铁得到硫酸亚铁和滤渣2,所以滤渣2中是锡、镍和铅,则
(1)根据以上分析可知步骤②中产生的气体是氢气;(2)滤渣2中含有的金属是:Sn、Pb、Ni;(3)步骤⑤的反应是铁和硫酸铜反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO4=FeSO4+Cu;(4)通过推导可知,步骤⑥回收的纯净物B是FeSO4;(5)根据以上分析可知金属Fe、Ni、Pd在溶液中的活动性由强到弱的顺序依次是:Fe、Ni、Pd。


科目:高中化学 来源: 题型:
【题目】用接触法制5t98%的浓硫酸,在理论上需要含FeS2 75%(杂质不含硫元素)的硫铁矿为 ( )
A. 4.3t B. 8t C. 4t D. 5.6t
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯化硼的熔点为-107.3 ℃,沸点为12.5 ℃,易水解生成硼酸(H3BO3),可用于制造高纯硼、有机合成催化剂等。实验室制取三氯化硼的原理为B2O3+3C+3Cl2![]() 2BCl3+3CO。
2BCl3+3CO。
(1)甲组同学拟用下列装置制取纯净干燥的氯气(不用收集)。

①装置B中盛放的试剂是__,装置C的作用是___________________。
②装置A中发生反应的离子方程式为 _____________________________。
(2)乙组同学选用甲组实验中的装置A、B、C和下列装置(装置可重复使用)制取BCl3并验证反应中有CO生成。
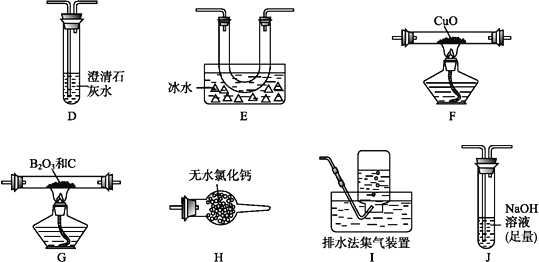
①乙组同学的实验装置中,依次连接的合理顺序为
A→B→C→G→__→__→__→__→F→D→I。
②能证明反应中有CO生成的现象是___________________________。
③开始实验时,先点燃____(填“A” 或“G”)处的酒精灯。
④请写出BCl3水解的化学方程式__________________________。
⑤硼酸是一元弱酸,其钠盐化学式为Na [B(OH)4],则硼酸在水中电离方程式是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.写出下列反应的离子方程式:
(1)将鸡蛋壳在醋酸中溶解有气泡产生:_____________________________________________;
(2)CuSO4溶液与Ba(OH)2溶液混合:________________________________________。
Ⅱ.对一份稀溶液作初步分析后发现,溶液无色、澄清,其可能含有![]() 、Na+、
、Na+、![]() 、H+、
、H+、![]() 、
、![]() 、Cl等离子中的若干种。然后又作了如下分析,以确定这些离子是否存在。
、Cl等离子中的若干种。然后又作了如下分析,以确定这些离子是否存在。
①用石蕊试液检测该溶液时,溶液显红色。
②取2 mL溶液用BaCl2溶液和稀硝酸进行检验,结果生成了白色沉淀。
③对②中所得的混合物充分静置后,取其上层澄清的液体用AgNO3溶液和稀硝酸进行检验,结果又生成了白色沉淀。
请回答下列问题:
(1)原溶液中一定存在的离子是__________,一定不存在的离子是____________。
(2)在上述实验操作中,有错误的步骤是(填代号)______。对该错误改正的方法是(要作较详细的说明)_________________________________________________________。
(3)到目前为止,不能肯定在原溶液中是否存在的离子是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(12分)化合物D是硅橡胶的稳定剂,其合成路线如下图

(1)B的分子式为 ; C中官能团名称 。
(2)C→D的反应类型为 。
(3)B→C的化学方程式为 。
(4)化合物D可能具有的性质有 (选填序号)。
a.加成反应 b.与FeCl3溶液发生显色反应
c.消去反应 d.酯化反应
(5)化合物B经3步反应可制备 ,反应类型依次是 (选填序号)。
,反应类型依次是 (选填序号)。
a.加成 、 取代、 消去
b.取代、消去、加成
c.消去、加成、取代
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】离子方程式BaCO3 + 2H+ = CO2↑ + H2O + Ba2+ 中的H+不能代表的物质是( )
①HCl;②H2SO4;③HNO3;④NaHSO4;⑤CH3COOH
A.①③ B.①④⑤ C.②④⑤ D.①⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属厲钨(W)可做灯泡的灯丝,钨合金材料非常坚硬和耐磨、耐热。用黑钨矿(含有FeWO4)与Na2CO3混合在空气中焙烧可以得到Na2WO4,Na2WO4与热的浓盐酸反应生成H2WO4,H2WO4受热分解生成H2O和WO3。
(1)钨合金材料属于__________。(填选项)
A.单质 B.化合物 C.纯净物 D.混合物
(2)4FeWO4+4Na2CO3+O2![]() 4Na2WO4+2Fe2O3+4______。H2WO4读作_______。H2WO4中钨元素的化合价为_______。
4Na2WO4+2Fe2O3+4______。H2WO4读作_______。H2WO4中钨元素的化合价为_______。
(3)H2与WO3在1000℃条件下发生反应可得到金属W,其反应方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是 ( )
A. 1mol NaCl分子中含有1mol Na+和1mol Cl-
B. 离子化合物和共价化合物溶于水都能导电
C. 离子键的形成一定有电子的得失
D. KOH溶于水电离出K+ 和OH- 不是化学变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com