
����Ŀ�����Ṥҵβ���ж�������ĺ�������0.05%(�������)ʱ�辭����������ŷš�ijУ��ȤС�����ⶨ���Ṥҵβ���ж�������ĺ������������·�����
��������ͼ��ʾ��ͼ������������B����ȷ����ͨ��β�����������β��ͨ��һ�������֪Ũ�ȵĵ�ˮ�вⶨSO2�ĺ�������ϴ��ƿC����Һ��ɫ��ʧʱ�������رջ���A��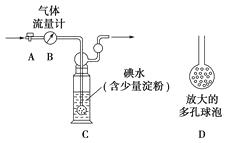
��1��ϴ��ƿC�е���ĩ������һ���������D���������ʵ���ȷ�ȣ��������ǣ���
��2��ϴ��ƿC�е���Һ�����������Լ����������ٳ�һ�֣�
��3��ϴ��ƿC����Һ��ɫ��ʧ��û�м�ʱ�رջ���A����õ�SO2����(�ƫ�ߡ�����ƫ�͡�����Ӱ�족)��
��4��д��������з�Ӧ�Ļ�ѧ����ʽ��
��5���������ϴ�ӳ����ķ�������
��6��ͨ����β�����ΪV L(�ѻ���ɱ�״��)ʱ����β���ж�������ĺ���(�������)Ϊ(�ú���V��m�Ĵ���ʽ��ʾ)��
�����������ҷ����в����ʡ�ԣ�ֱ�ӽ�β��ͨ�����Ba(OH)2��Һ�У����ಽ�����ҷ�����ͬ��
��7������Ϊ�������Ƿ������˵�����ɣ� ��
���𰸡�
��1��������������Һ�ĽӴ������������SO2���ˮ��ַ�Ӧ
��2��
���Ը��������Һ(������������)
��3��ƫ��?
��4��H2SO4��Ba(OH)2=BaSO4����2H2O
��5����©����ע������ˮ��ʹˮ��û���������ˮ�������ظ�����2��3��
��6��![]() ��
�� ![]() %
%
��7�������������������ᱵ�ɱ�(�����е�����)����Ϊ���ᱵ
��������(1)�������õ�ԭ��Ϊ��SO2��I2��2H2OH2SO4��2HI��ϴ��ƿC�е���ĩ������һ���������D����������SO2���ˮ�ĽӴ������ʹSO2�͵�ˮ��ַ�Ӧ��(2)ϴ��ƿC�е���Һ�����������Ը��������Һ����ˮ�ȴ��档(3)ϴ��ƿC����Һ��ɫ��ʧ��û�м�ʱ�رջ���A����ͨ��β��������������SO2����ƫ�͡�(4)�ҷ������õ�ԭ��Ϊ��SO2��H2O2=H2SO4 �� H2SO4��Ba(OH)2=BaSO4����2H2O��(5)�������ϴ�ӳ���ʱ��Ҫ�ظ�ϴ��2��3�Ρ�(6)����SO2��BaSO4 �� ��β���ж�����������Ϊ ![]() ��22.4 L����β���ж�������ĺ���Ϊ
��22.4 L����β���ж�������ĺ���Ϊ 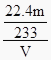 ��100%��
��100%�� ![]() %��(7)���������õ�ԭ����SO2��Ba(OH)2=BaSO3����H2O������BaSO3���ױ������е���������ΪBaSO4 �� ���BaSO3������m����ֵ��ȷ���ʸ÷�����������
%��(7)���������õ�ԭ����SO2��Ba(OH)2=BaSO3����H2O������BaSO3���ױ������е���������ΪBaSO4 �� ���BaSO3������m����ֵ��ȷ���ʸ÷�����������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ѧ��ʵ��Ҫע�ⰲȫ������Ⱦ���������ԡ��������շ�����ԭ�������õײ���С���Թ��Ƽ������巢����(����ͼ)�����ر�K����ʹ��Ӧֹͣ���ɽ��Թܴ��ձ���ȡ��(���в���������ɢ)�������������ȡ��ʹ�ø�װ�õ��� (����) 
A.�ö�������(��ĩ)��˫��ˮ������
B.��п����ϡ����������
C.��������(��״)������������
D.��̼���(��״)��ϡ�����ƶ�����̼
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ȡ�������ʵ���ʵ�飺 ������ֽ�����ĸ��ʵ���С�ij����Σ�Ȼ����Щ��ֽ���÷�ʿ��ճ�ڼ���ƿ�ڲ���
�ڽ�����NaI��NaBr��Na2S��Ʒ����Һ(1��2��)������ͼ��ʾ����ֽ�ϡ�
������ƿ�ڼ�1.5 g KClO3 �� �õι���ȡԼ2 mLŨ���ᣬȻ�ι�װ��˫�����ϣ����Ѹ�˫�������ڼ���ƿ�ϣ���ͼ��ʾ��
���õι���©���м�NaOH��Һ��ע������NaOH��ҺӦ�Ըպ�װ��©���¶˵���ܴ�Ϊ��(NaOH��Һ�ڴ���Һ������ͬʱ���м�ѹ����)
�ݼ�ѹ��ͷ�ι�����ƿ�м�Ũ���ᡣ
��������������õι���©���м�NaOH��Һ����β����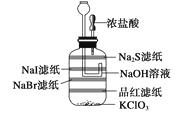
��1����ʵ�����Ҫ���� ��
��2����ʵ��Ļ�ѧ����ʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����в����У����ᷢ��������ɫ�仯����
A. �Ȼ�ͭ��������ˮ�� B. ��������Һ�еμ����������Һ
C. �Ȼ�������Һ�м���ͭ�� D. ����������Һ��ͨ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A.1molOH����������17gB.������Ħ��������2g
C.Ħ�������ʵ������ĵ�λD.����Ħ�����ԼΪ22.4L/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�ֽ����ڵ�Ӿʱ�����Ľ����������ƶ������⽺���зֱ�����������ʣ����Ҵ���Һ�����Ȼ�����Һ�����������������������壬���ᷢ���۳�����
A.�٢�B.�٢�C.�ڢ�D.�ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л����ϵͳ����������ǣ� ��
A.2������2��4������ϩ
B.4������1����Ȳ
C.2������6���һ�����
D.1��3��5�����ױ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ж������������У�����ȷ����
A. ������ʹʪ��ĺ첼����ɫ��������������Ư����
B. ��������ʹʪ�����ɫʯ����ֽ�ȱ�����ɫ
C. ͭ������ȼ�ղ����ػ�ɫ����
D. �����ǻ���ɫ�ģ�����������ɫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ļ�����Һ���ܴ������������������ ��
A. K����Na����NO3 ����MnO4�� B. Naʮ��Ca2����NO3 ����Cl��
C. K����Naʮ��SO42����NH4�� D. K����Na����HCO3����SO42��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com