
【题目】下列操作中,不会发生明显颜色变化的是
A. 氯化铜固体溶于水中 B. 硫酸铁溶液中滴加硫氰酸钾溶液
C. 氯化亚铁溶液中加入铜粉 D. 硫酸亚铁溶液中通入氯气
科目:高中化学 来源: 题型:
【题目】在周期表中1~36号之间的W、X、Y、Z、Q六种元素,它们的原子序数依次增大,已知W与其余五种元素既不同周期也不同主族,X原子的L层p轨道中有2个电子,Y元素原子的最外层有3个自旋方向相同的未成对电子,Z元素原子基态时,核外电子排布在3个能级上,且有2个未成对电子.Q元素在第四周期,原子的K层电子数与最外层电子数之比为2:1,其d轨道处于全充满状态.
(1)按电子排布,Q元素在周期表中属区.
(2)第一电离能YZ,电负性YZ(填“>”,“=”或“<”).
(3)W与Z形成的常见化合物有W2Z、W2Z2 , W与Y能形成多种二元化合物,如YW3、Y2W4、Y3W5、Y4W6…,W2Z分子中Z原子的杂化类型为 , YW3分子的立体构型为 , YW3极易溶于W2Z的主要原因有 .
(4)若向含有Q2+的硫酸盐溶液中滴加过量氨水,得到深蓝色溶液后再加乙醇,有深蓝色晶体析出,该晶体阳离子中含有的化学键有 .
(5)Q+与Y3﹣形成的晶胞结构如图所示,阴、阳离子间的核间距为 a pm,阿伏伽德罗常数用NA 表示,则晶体的密度为gcm﹣3 . 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下图所示装置和操作,回答下列有关问题。 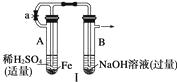
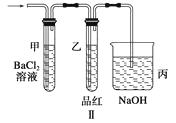
(1)按图Ⅰ所示装置,用两种不同的操作分别进行实验,观察B管中的现象。 ①操作1:先夹紧止水夹a,再使A管开始反应,实验中观察到B管中的现象是
。
②操作2:打开止水夹a,使A管反应一段时间后再夹紧止水夹a,实验中观察到B管
中的现象是。
③请说明造成两种操作现象不同的原因(如两种现象相同,此小题不用回答):
。
(2)上述装置实验结束后,取A管内反应所得的溶液,隔绝空气小心蒸干后,再高温煅 烧(有关装置和操作均已略去),最后留下红色固体,将分解时产生的气体按图Ⅱ所示装置依次通过洗气装置,结果试管甲内出现白色沉淀,试管乙内品红溶液红色褪去,回答:
① 用方程式表示试管甲产生白色沉淀的原因。
②根据实验现象写出A管内溶液蒸干后,在高温煅烧分解时所发生的化学反应方程式
。
③图Ⅱ中丙装置的作用是。
实验结束时,在装置丙中观察到的现象是。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质的量的叙述中,正确的是
A.1mol任何物质都含有6.02×1023个分子B.0.012gC-12中约含有6.02×1023个碳原子
C.1mol水中含有2mol氢和1mol氧D.1molH2分子中含有2molH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向mg镁和铝的混合物重加入适量的稀硫酸,恰好完全反应生成标准状况下的气体bL.向反应后的溶液中加入cmol/L氢氧化钾溶液VmL,使金属离子刚好沉淀完全,得到的沉淀质量为ng.再将得到的沉淀灼烧至质量不再改变为止,得到固体pg.则下列关系不正确的是
A. c=![]() B. p=m+
B. p=m+![]() C. n=m+17Vc D.
C. n=m+17Vc D. ![]() m<p<
m<p<![]() m
m
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸工业尾气中二氧化硫的含量超过0.05%(体积分数)时需经处理后才能排放。某校兴趣小组欲测定硫酸工业尾气中二氧化硫的含量,采用以下方案:
甲方案:如图所示,图中气体流量计B用于准确测量通过尾气的体积。将尾气通入一定体积已知浓度的碘水中测定SO2的含量。当洗气瓶C中溶液蓝色消失时,立即关闭活塞A。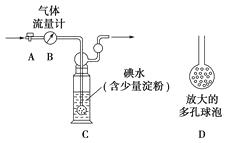
(1)洗气瓶C中导管末端连接一个多孔球泡D,可以提高实验的准确度,其理由是:。
(2)洗气瓶C中的溶液可以用其他试剂替代,请你举出一种?
(3)洗气瓶C中溶液蓝色消失后,没有及时关闭活塞A,测得的SO2含量(填“偏高”、“偏低”或“无影响”)。
(4)写出步骤②中反应的化学方程式。
(5)步骤③中洗涤沉淀的方法是。
(6)通过的尾气体积为V L(已换算成标准状况)时,该尾气中二氧化硫的含量(体积分数)为(用含有V、m的代数式表示)。
丙方案:将乙方案中步骤①省略,直接将尾气通入过量Ba(OH)2溶液中,其余步骤与乙方案相同。
(7)你认为丙方案是否合理,说明理由: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某厂的酸性工业废水中含有一定量的Fe3+、Cu2+、Au3+等离子,有人设计了图中的工艺流程,从废水中回收金,并生产一定量的铁红和氧化铜(图中标号处只利用工业生产中的常用的酸、碱和废铁屑). 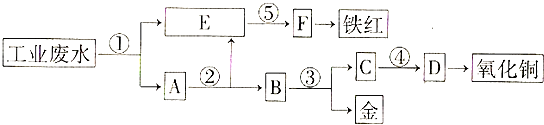
(1)图中标号处需加入的相应物质分别是①、②、③、④、⑤;
(2)写出①处所有可能发生的离子方程式
(3)写出③处发生反应的化学方程式;
(4)铁红的化学式为;写出铁红在工业上的一种主要用途 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在T℃ 时,将a g NH3完全溶于水,得到V mL溶液,假设该溶液的密度为ρ gcm﹣3 , 溶质的质量分数为w,其中含NH3的物质的量为b mol.下列叙述中正确的是( )
A.溶质的质量分数为w= ![]() ×100%
×100%
B.溶质的物质的量浓度c= ![]() ?mol?L﹣1
?mol?L﹣1
C.溶液中c(OH﹣)= ![]() ?mol?L﹣1
?mol?L﹣1
D.上述溶液中再加入V mL水后,所得溶液溶质的质量分数大于0.5w
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com