
【题目】Cu2O,辉铜矿的主要成分是Cu2S,将赤铜矿与辉铜矿按一定比例混合加热可制得铜:2Cu2O+Cu2S====6Cu+SO2↑。对于该反应,下列说法中正确的是( )
A. 该反应中的氧化剂只有Cu2O B. Cu2S在反应中既是氧化剂又是还原剂
C. Cu既是氧化产物又是还原产物 D. 氧化产物和还原产物的物质的量之比为6:1
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】CO2的有效利用可以缓解温室效应和能源短缺问题。
(1)固态 CO2(干冰)所属晶体类型___________,所含化学键类型为__________(填“非极性键”或“极性键”或“离子键,下同)。CO2与Na2O2反应过程形成化学键类型为______________________________。
(2)中科院的科研人员在Na-Fe3O4和HMCM-22 的表面将CO2转化为烷烃,其过程如下图。
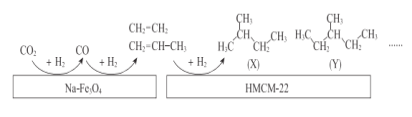
①Na-Fe3O4和HMCM-22 在反应中的作用为_______________。
②写出(X)的所有同分异构体结构简式_______________。
③关于X与Y的说法正确的是__________(填序号〕。
a.最简式相同 b.都有4种一氯代物
c.都易使酸性KMnO4溶液褪色 d.X与Y互称同系物
(3)同温同压下,蒸气密度是氢气15倍的烷烃(M),写出其与氯气反应生成一氯代烃的方程式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别向等体积1mol/L盐酸和1mol/L醋酸溶液中加入等量的镁条,反应时间与溶液pH变化关系如右图。下列说法中不正确的是( )

A. Y代表盐酸与镁条的反应
B. a点时反应Y消耗镁条的量少
C. b点表示此时两溶液pH相等
D. c点表示此时反应结束
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2,黄绿色易溶于水的气体)是一种安全稳定、高效低毒的消毒剂。工业上通过惰性电极电解氯化铵和盐酸的方法制备,其原理如图所示:

下列说法不正确的是
A. b电极接电源的负极,在b极区流出的Y溶液是稀盐酸
B. 二氧化氯发生器中排出的X溶液中溶质主要为NaCl和NaOH
C. 电解过程中二氧化氯发生器中产生2.24L(标准状况)NH3,则b极产生0.6gH2
D. 电解池a极的电极反应式为NH4+-6e-+4OH-+3Cl-=NCl3+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的值。下列说法正确的是
A. 一定条件下,1molN2和3molH2混合后,反应转移的电子数目为6NA
B. 1.0L0.1mol/LNa2S溶液中含有的S2-数为0.1NA
C. 1molCu与含2molH2SO4的浓硫酸充分反应,生成的SO2的分子个数为NA
D. 向含有FeI2的溶液中通入适量氧气,当有1molFe2+被氧化时,该反应转移的电子数目至少为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ZrO2常用作陶瓷材料,可由锆英砂(主要成分为ZrSiO4,也可表示为ZrO2·SiO2,还含少量Fe2O3、Al2O3、SiO2等杂质)通过如下方法制取:
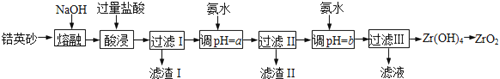
已知:①ZrO2能与烧碱反应生成可溶于水的Na2ZrO3,Na2ZrO3与酸反应生成ZrO2+。
②部分金属离子在实验条件下开始沉淀和完全沉淀的pH如下表。
金属离子 | Fe3+ | Al3+ | ZrO2+ |
开始沉淀时pH | 1.9 | 3.3 | 6.2 |
沉淀完全时pH | 3.2 | 5.2 | 8.0 |
(1)熔融时ZrSiO4发生反应的化学方程式为 ,滤渣I的化学式为 。
(2)为使滤液I的杂质离子沉淀完全,需用氨水调pH=a,则a的范围是 ;继续加氨水至pH=b时,所发生反应的离子方程式为 。
(3)向过滤III所得滤液中加入CaCO3粉末并加热,得到两种气体。该反应的离子方程式为 。
(4)为得到纯净的ZrO2,Zr(OH)4需要洗涤,检验Zr(OH)4是否洗涤干净的方法是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活息息相关,在各个方面都起着重要的作用。
(1)材料是经济和生态文明建设的重要物质基础。
合成塑料在生活中广泛应用,乙烯形成聚乙烯的方程式:_____________________。该反应的反应类型:_________________.橡胶是制造轮胎的重要原料,橡胶属于____________________填字母。
A金属材料 B无机非金属材料 C有机高分子材料
铝热反应在工业生产中的重要用途之一是焊接钢轨,其反应的化学方程式为:______________________________________;钢铁制品在潮湿的空气中能发生腐蚀,发生该腐蚀时的负极反应式为__________________________________。
(2)“三高症”是指高血糖糖尿病、高血脂和高血压症,是现代社会中的“富贵病”。
①血糖是指血液中的葡萄糖。葡萄糖的结构简式是__________________________。在加热条件下,加入氢氧化钠溶液,调节溶液为碱性,此时葡萄糖与新制的氢氧化铜发生反应,观察到的现象是________________此方法曾经用于检测糖尿病。
②血脂是血液中所含脂类物质的总称。油脂对人体的作用之一是________,但过量摄入,可能引起肥胖、高血脂、高血压。油脂在碱性条件下水解反应称为_____________.
③高血压可由肥胖、糖尿病、摄入过多钠盐等引起,而摄入过量的蛋白质也会造成脂肪堆积。蛋白质水解的最终产物是________,蛋白质的组成元素除C、H、O外,还含有_______(填一种)。
(3)石油在生活中的应用广泛。石油是由多种碳氢化合物组成的混合物,从原油中分离出汽油、煤油、柴油等轻质油的方法是____________________(填操作名称).分离出的汽油_______(填“是”或者“否”)可作萃取剂。汽油是C5~C11的混合烃,其中含有5个碳原子的烷烃存在________种同分异构体,其中一种同分异构体的一氯代物只有一种,则该同分异构体与氯气发生取代反应生成一氯代物的化学方程式为:___________________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期主族元素 W、M、X、Y、Z 原子序数依次增大,请结合表中信息回答下列问题:
元素 | W | M | X | Y | Z |
结构或性质 | 最高价含氧 酸与其气态 氢化物能发 生化合反应 | 氢化物的水 溶液能刻蚀 玻璃 | 焰色反应火 焰呈黄色 | 同周期主族元 素形成的简单 离子中,其离子 半径最小 | 最高正价与 最低负价代 数和为 6 |
(1)M元素在周期表中的位置为_____。
(2)M、X、Z元素所对应简单离子半径由大到小的顺序为_____________________(用离子符号表示)。
(3)W最高价含氧酸与其气态氢化物发生化合反应生成的物质中含有的化学键类型为___________________________________。
(4)下列可作为比较M和Z的非金属性强弱的依据是_________(填序号)。
A.单质与H2反应的难易程度
B.氢化物的稳定性
C.最高价氧化物的水化物酸性强弱
D.将M的单质通入Z的钠盐溶液观察是否有Z逸出
(5)W能形成多种氢化物,其中一种氢化物可作为火箭燃料,该物质中W与氢元素的质量比为7:1,写出该氢化物的电子式______。该氢化物和 O2 在碱性条件下可形成燃料电池,产生两种无毒物质,写出其负极的电极反应式___________.
(6)Y元素和W元素形成的化合物YW一种新型无机材料,可与过量烧碱溶液反应产生使湿润的红色石蕊试纸变蓝的气体,写出有关的化学方程式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作不正确的是
A. 蒸发时,残留的少量水让余热蒸干
B. 分液时,下层液体从下端放出,上层液体从上端倒出
C. 蒸馏时,冷水从冷凝管上口进下口出
D. 过滤时,漏斗下端紧贴烧杯内壁
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com