
| ���� | ʵ����� | Ԥ������ | ���� |
| ������������ | ______ | ______ | ______ |
| ������������Ҫ��һ��̽�� | ______ | ______ | ______ |
| ||
| ||
| ���� | ʵ����� | Ԥ������ | ���� |
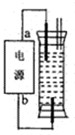
| ���ձ�ȡ��������Һ����һ�Ź��������������ձ�������һ��ʱ�� | ��������������� | ��������ʴ | |
| ���Թ�ȡ������ʵ��٣����ݺ����Һ���μ�������1mol/L�������ữ�����õιܵμӼ���20%��KSCN��Һ | ��Һ����ɫ����Һ��Ѫ��ɫ | ��������δ����ʴҲ���ܱ���ʴ |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

- 4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
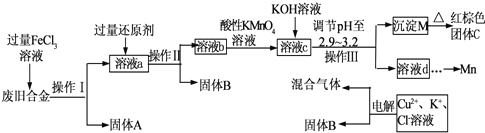
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
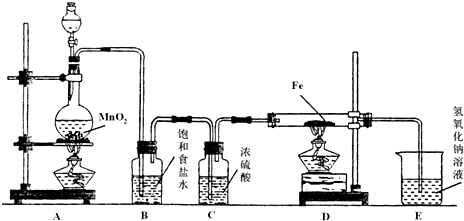
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
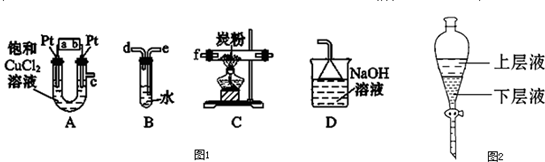
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com